Toets voor nascholing (verlopen)
Aan dit leerartikel was een toets gekoppeld waarmee je nascholingspunten kon verdienen.
Samenvatting
De afgelopen jaren is veel onderzoek verricht naar de interactie tussen clopidogrel en protonpompremmers.
Studies naar de invloed van protonpompremmers op bloedplaatjesreactiviteit en op klinische eindpunten bij met clopidogrel behandelde patiënten hebben tegenstrijdige resultaten opgeleverd.
Gelijktijdig gebruik van omeprazol en clopidogrel leidt tot een halvering van de blootstelling aan de actieve metaboliet van clopidogrel en tot een sterk verhoogde bloedplaatjesreactiviteit, als gevolg van remming van CYP2C19, een cytochroom P450(CYP)-enzym, door omeprazol.
Pantoprazol heeft een veel geringer effect op de farmacokinetiek en de trombocytenaggregatie bij gelijktijdig gebruik van clopidogrel.
De effecten van de overige protonpompremmers bij gelijktijdig gebruik van clopidogrel zijn nog niet in adequaat gerandomiseerde studies onderzocht.
Registratieautoriteiten geven aan dat de combinatie van clopidogrel met omeprazol of esomeprazol (beide CYP2C19-remmers) vermeden dient te worden.
Op dit moment is voor geen enkele protonpompremmer overtuigend een klinisch relevante interactie met clopidogrel aangetoond.
artikel
Clopidogrel in combinatie met acetylsalicylzuur wordt gebruikt ter preventie van trombotische complicaties na een acuut coronair syndroom en na een percutane coronaire interventie (PCI).1 Deze middelen remmen de trombocytenaggregatie. Ter bescherming tegen gastro-intestinale complicaties van deze medicatie kan een protonpompremmer worden voorgeschreven.2 Zowel trombotische complicaties als bloedingen gaan gepaard met aanzienlijke morbiditeit en mortaliteit.3 De prodrug clopidogrel wordt door cytochroom-P450-(CYP)-enzymen gemetaboliseerd tot de actieve metaboliet, waarbij met name CYP2C19 een belangrijke rol speelt.4,5 Omeprazol en esomeprazol zijn sterke CYP2C19-remmers.6-8
Veel studies, met tegenstrijdige resultaten, zijn over de interactie tussen protonpompremmers en clopidogrel gepubliceerd. Dit artikel geeft een overzicht van de literatuur en beschrijft de waarschuwingen van registratieautoriteiten.
Literatuuronderzoek
Wij voerden in Pubmed de zoekopdracht: ‘clopidogrel’ and ‘proton pump inhibitors’ or ‘pantoprazole’ or ‘omeprazole’ or ‘esomeprazole’ or ‘lansoprazole’ or ‘rabeprazole’, tot 23 november 2010 uit. Daaruit selecteerden wij artikelen met als eindpunt plasmaconcentraties van clopidogrels actieve metaboliet, bloedplaatjesreactiviteit of trombotische complicaties.
Naast de waarschuwingen van het College ter Beoordeling van Geneesmiddelen (CBG), de European Medicines Agency (EMA) en Amerikaanse Food and Drug Administration (FDA), vonden wij 184 publicaties, waarvan er 30 voldeden aan de selectiecriteria (figuur).
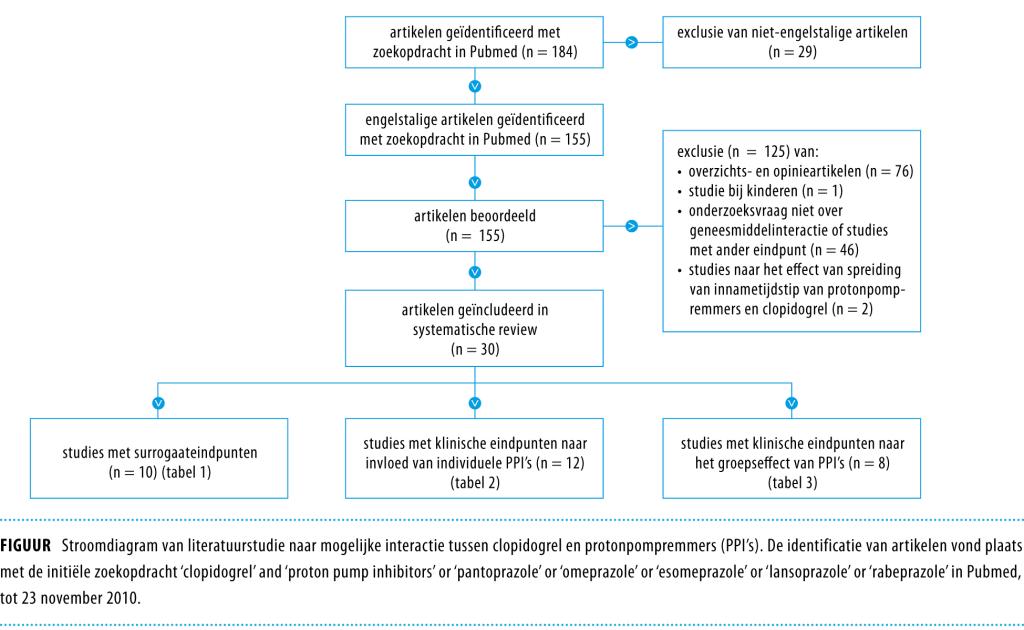
Bloedplaatjesreactiviteit en actieve metaboliet
Het effect van protonpompremmers op de trombocytenaggregatieremmende werking van clopidogrel werd onderzocht door de reactiviteit van bloedplaatjes ex vivo met plaatjesfunctietesten te meten. Diverse observationele studies toonden aan dat een verhoogde bloedplaatjesreactiviteit tijdens clopidogrelgebruik gerelateerd is met het optreden van trombotische complicaties.9,10 Patiënten met een bloedplaatjesreactiviteit van meer dan 64,5%, gemeten met lichtaggregometrie na stimulatie met ADP 20 µmol/l, hebben een 2,1 maal grotere kans op het gecombineerde eindpunt van overlijden, myocardinfarct, stenttrombose en beroerte na een PCI dan patiënten met een bloedplaatjesreactiviteit kleiner dan 64,5%.10 Bijna 40% van de clopidogrelgebruikers heeft een bloedplaatjesreactiviteit van meer dan 64,5%.10 Deze patiënten worden beschouwd als ‘clopidogrel-resistent’.
Gerandomiseerde, prospectieve studies
De studies met surrogaateindpunten staan samengevat in tabel 1. In een gerandomiseerde, dubbelblinde, placebogecontroleerde studie met patiënten die een geplande PCI ondergingen, werd een 1,3 maal hogere bloedplaatjesreactiviteit gezien bij patiënten die gedurende 1 week gecombineerd clopidogrel en omeprazol 20 mg gebruikten, dan bij de groep die placebo had ontvangen.11 Een placebogecontroleerde cross-overstudie bij gezonde proefpersonen liet een 1,2 maal hogere bloedplaatjesreactiviteit bij gebruik van omeprazol 20 mg zien, vergeleken met de placebogroep.12
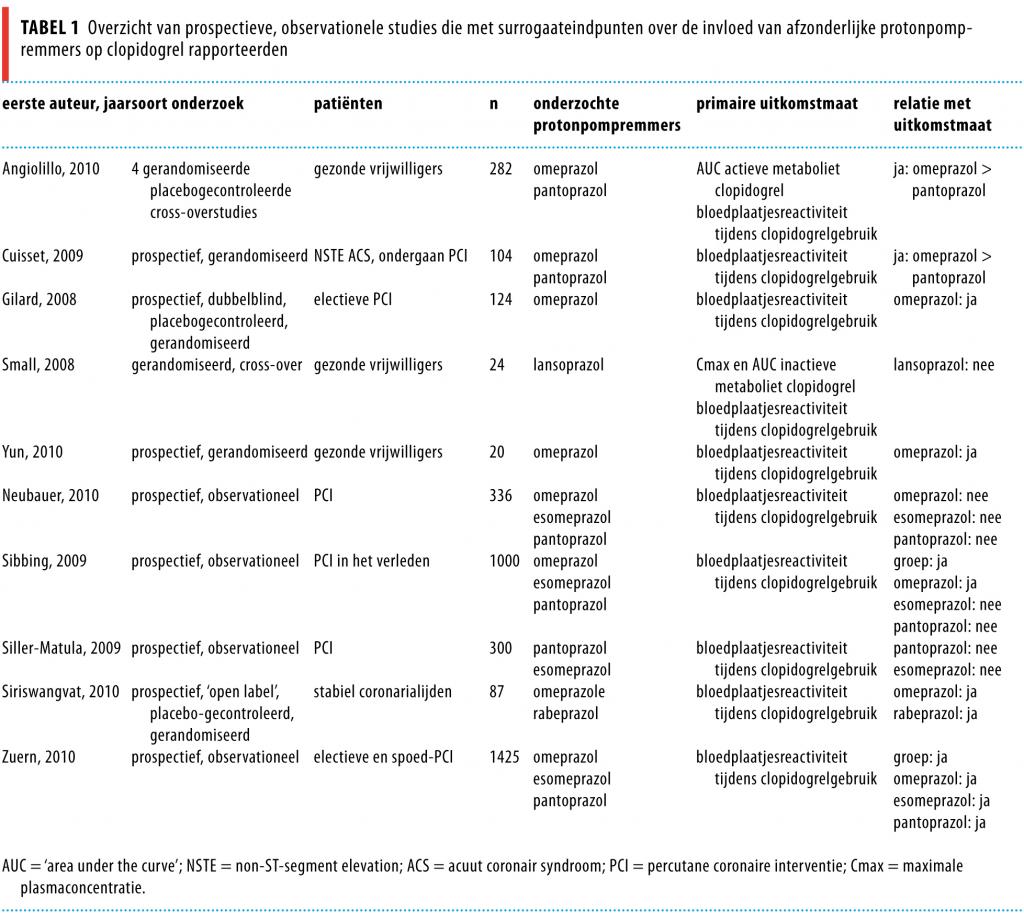
In een studie waarbij patiënten gerandomiseerd werden naar behandeling met pantoprazol 20 mg of met omeprazol 20 mg, hadden omeprazolgebruikers een 1,3 maal hogere bloedplaatjesreactiviteit dan pantoprazolgebruikers.13
In een gerandomiseerde cross-overstudie ontvingen 72 gezonde proefpersonen clopidogrel (300 mg op de eerste dag, gevolgd door 75 mg per dag) met en zonder omeprazol (80 mg per dag, gelijktijdig met clopidogrel toegediend).14 In combinatie met omeprazol was de blootstelling (‘area under the curve’ (AUC)) aan de actieve metaboliet van clopidogrel 47% (dag 2) en 40% (dag 5) lager dan wanneer omeprazol niet werd gebruikt. Verder werd de trombocytenaggregatie 42% (dag 2) en 31% (dag 5) minder geremd bij omeprazolgebruik. In een tweede studie ontvingen 72 gezonde proefpersonen dezelfde doses clopidogrel en omeprazol als in de eerste studie, maar dan ingenomen met een tijdsinterval van 12 h tussen clopidogrel en omeprazol. Er werd een vergelijkbare invloed van omeprazol op de blootstelling aan de actieve metaboliet en op de trombocytenaggregatie gevonden.14 Hieruit blijkt dat spreiding van de toedientijdstippen geen oplossing is voor de interactie.
In dezelfde publicatie werd een gerandomiseerde cross-overstudie beschreven waarin 66 gezonde proefpersonen clopidogrel (300 mg op de eerste dag, gevolgd door 75 mg per dag) met en zonder pantoprazol 80 mg ontvingen.14 Clopidogrels actieve metaboliet werd minder beïnvloed door gelijktijdig gebruik van pantoprazol dan door gelijktijdig gebruik van omeprazol: de verlaging van de AUC op dag 2 bedroeg 20% en op dag 5 14%. Ook de invloed op trombocytenaggregatieremming was minder groot bij pantoprazol- dan bij omeprazolgebruik (pantoprazol: 16% op dag 2 en 11% op dag 5).14
Lansoprazol had in een gerandomiseerde cross-overstudie met 24 gezonde proefpersonen geen significant effect op de trombocytenaggregatieremmende werking van clopidogrel.15 In een studie waarin patiënten met stabiel coronairlijden werden gerandomiseerd naar behandeling met omeprazol 20 mg of rabeprazol 20 mg, naast de standaardbehandeling met clopidogrel, was gebruik van beide protonpompremmers gerelateerd aan een significante verhoging van de bloedplaatjesreactiviteit onder het clopidogrelgebruik.16
Prospectieve, observationele studies
4 observationele studies beschrijven de invloed van individuele protonpompremmers (zie tabel 1).17-20 In 2 studies werd met verschillende plaatjesfunctietesten aangetoond dat clopidogrelgebruikers gemiddeld een 1,2 maal hogere bloedplaatjesreactiviteit tijdens omeprazolgebruik hadden dan patiënten zonder protonpompremmers.17,19
De invloed van esomeprazol op de trombocytenaggregatieremmende werking van clopidogrel is in de 4 studies onderzocht.17-20 In de grootste studie was esomeprazolgebruik gerelateerd aan een hogere bloedplaatjesreactiviteit tijdens clopidogrelgebruik.18 In de 3 kleinere studies werden geen relaties gevonden.17,18,20 Echter, in een van de studies was de power om een 1,3 maal hogere bloedplaatjesreactiviteit tijdens esomeprazolgebruik te detecteren slechts 57%.17
De invloed van pantoprazolgebruik op de bloedplaatjesreactiviteit is ook in de 4 observationele studies onderzocht.17-20 In 1 studie hadden clopidogrelgebruikers een hogere bloedplaatjesreactiviteit tijdens pantoprazolgebruik dan patiënten zonder protonpompremmers.19 In de 3 overige studies werd geen effect gevonden voor pantoprazol,17,18,20 terwijl in 1 van deze studies het gebruik van omeprazol wel gerelateerd was met een significant hogere bloedplaatjesreactiviteit.
De invloed van lansoprazol- en rabeprazolgebruik werd in deze studies niet onderzocht.
Studies met klinische eindpunten
De invloed van individuele protonpompremmers op cardiovasculaire eindpunten bij clopidogrelgebruik is in 12 studies onderzocht (tabel 2).22-33 Studies die uitsluitend het groepseffect van protonpompremmers beschrijven, zijn samengevat in tabel 3.33-41 In 5 retrospectieve cohortstudies was het gebruik van zowel omeprazol, esomeprazol, pantoprazol als lansoprazol, naast clopidogrelgebruik, gerelateerd aan het optreden van cardiovasculaire complicaties.23,24,31-33 In 1 van deze studies was bij myocardinfarctpatiënten het gebruik van protonpompremmers ook gerelateerd aan een hoger risico op cardiovasculaire complicaties in de subgroep van patiënten die geen clopidogrel gebruikten.33
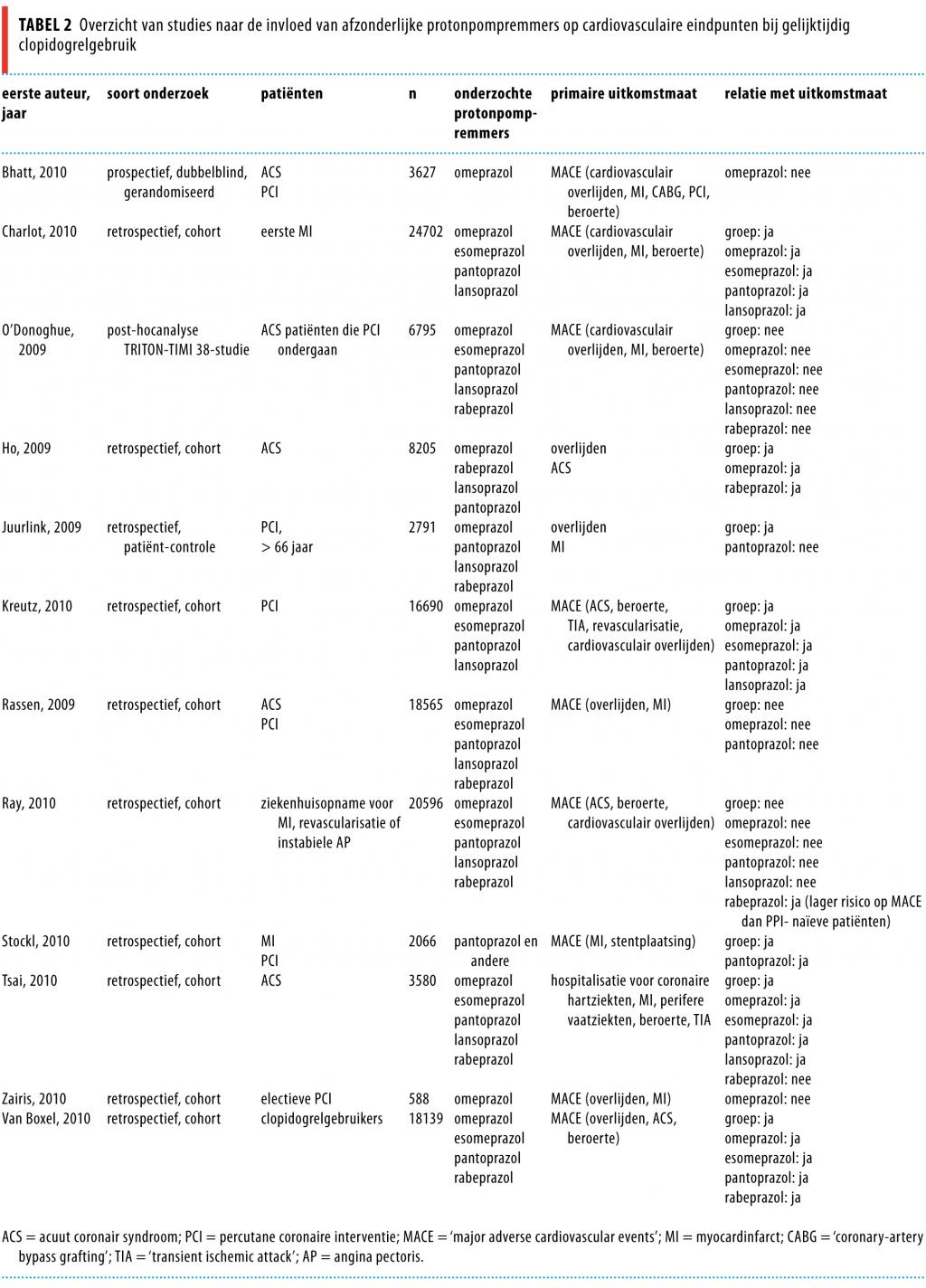
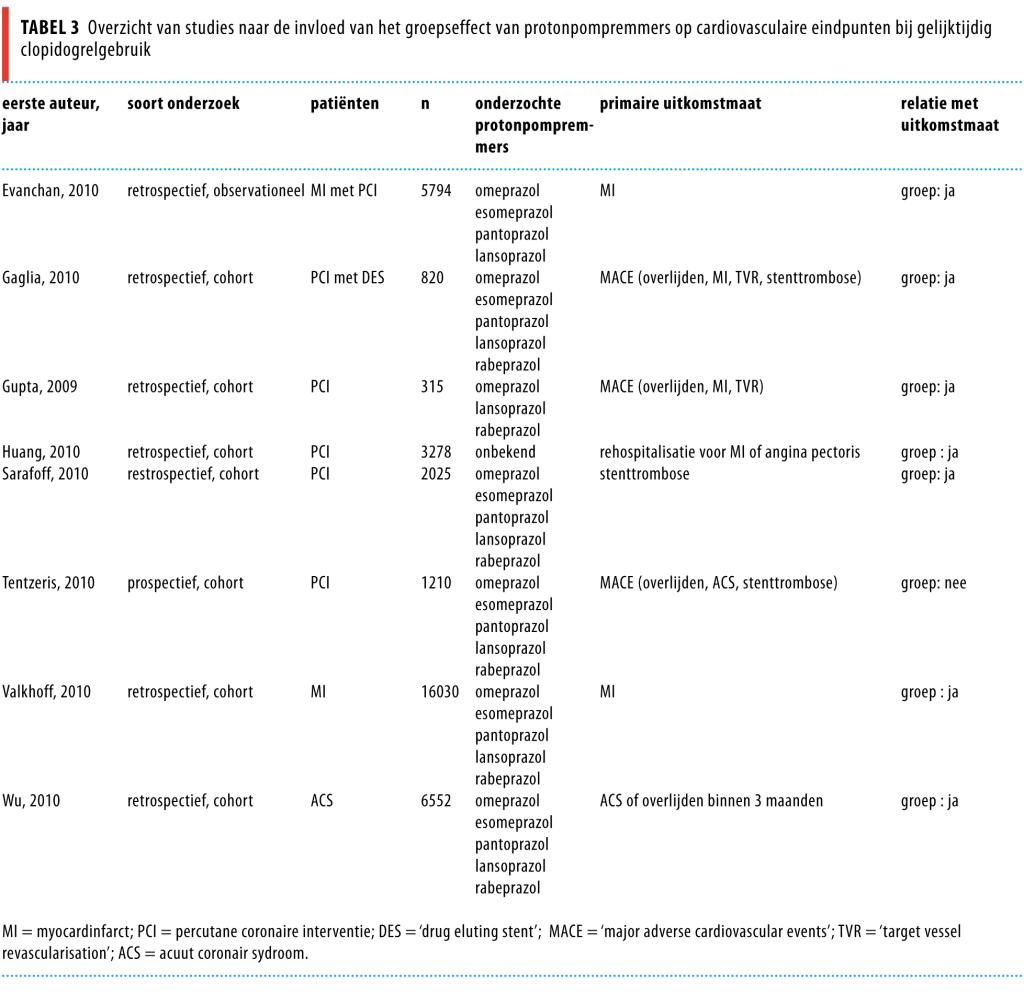
In een grote studie hadden omeprazol-, lansoprazol- en rabeprazolgebruikers die een PCI hadden ondergaan en gelijktijdig clopidogrel gebruikten, een verhoogd risico op het optreden van een myocardinfarct of op overlijden binnen 90 dagen, terwijl pantoprazolgebruik niet gerelateerd was met het eindpunt.29 In 3 andere studies bij clopidogrelgebruikers werd geen verband gevonden tussen het gebruik van protonpompremmers (als groep en individueel) en het optreden van cardiovasculaire complicaties.22,25,26
In de TRITON-TIMI 38-studie werden patiënten met een acuut coronair syndroom die een geplande PCI ondergingen gerandomiseerd naar een behandeling met clopidogrel of prasugrel. Van de met clopidogrel behandelde patiënten gebruikte 33% tevens omeprazol, pantoprazol, esomeprazol of lansoprazol.27 Het gebruik van protonpompremmers (als groep en individueel) was niet gerelateerd aan een verhoogd risico op het gecombineerde eindpunt van overlijden als gevolg van cardiovasculaire complicaties, het optreden van een myocardinfarct of van een beroerte in een periode van 15 maanden.27 Echter, patiënten in deze studie waren jonger, hadden minder comorbiditeiten en de ‘event rates’ waren lager dan in de retrospectieve observationele studies.
In de vroegtijdig gestaakte COGENT-studie werden patiënten gerandomiseerd naar het gebruik van omeprazol.30 Patiënten ontvingen na een acuut coronair syndroom of een PCI met stentplaatsing, naast acetylsalicylzuur, ook clopidogrel 75 mg of een combinatiepreparaat met clopidogrel 75 mg en omeprazol 20 mg. De data van de reeds geïncludeerde patiënten werden geanalyseerd. Omeprazol was effectief in het voorkómen van gastro-intestinale complicaties, maar omeprazolgebruik was niet gerelateerd aan een verhoogd risico op het gecombineerde eindpunt van cardiovasculaire dood, myocardinfarct, revascularisatie en beroerte gedurende een mediane follow-up van 106 dagen.30
Waarschuwingen registratieautoriteiten
De registratieautoriteiten EMA, FDA en CBG stellen dat het gecombineerd gebruik van omeprazol of esomeprazol met clopidogrel vermeden dient te worden. (www.ema.europa.eu, zoek op WC500076346; www.fda.gov, zoek op ucm190848 en klik op ‘Clopidogrel and Omeprazole - Drug Interaction’; en www.cbg-meb.nl/CBG/nl/humane-geneesmiddelen/actueel/20101216-Herzien-standpunt-interactie-clopidogrel-met-protonpompremmers/default.htm).
Beschouwing
De verschillende studies laten tegenstrijdige resultaten zien. Het is duidelijk aangetoond dat omeprazol de vorming van de actieve metaboliet van clopidogrel bijna halveert door remming van het enzym CYP2C19. Deze farmacokinetische interactie gaat gepaard met een vermindering van de remming van de trombocytenaggregatie met meer dan 30%.14 Ondanks deze uitkomsten blijkt omeprazol in de gerandomiseerde COGENT-studie geen afname van het effect van clopidogrel op cardiovasculaire eindpunten te geven.30
Aangezien esomeprazol net als omeprazol een CYP2C19-remmer is en vergelijkbare effecten heeft op het metabolisme van andere CYP2C19-substraten,7,8 lijkt het redelijk te veronderstellen dat esomeprazol een vergelijkbare interactie zal hebben met clopidogrel.
De andere protonpompremmers geven weinig tot geen remming van CYP2C19 en ook zijn er geen aanwijzingen dat deze protonpompremmers op een andere wijze de kinetiek en effecten van clopidogrel beïnvloeden.7
Confounding In de TRITON-TIMI 38-studie bleken protonpompremmers de effectiviteit van clopidogrel niet te beïnvloeden.27 De interpretatie van de resultaten van deze studie wordt echter bemoeilijkt doordat er niet op het protonpompremmergebruik gerandomiseerd was. In de observationele studies en de hierop gebaseerde meta-analyses werden tegenstrijdige effecten op klinisch relevante eindpunten waargenomen.42,43 Omdat het goed mogelijk is dat in deze studies de protonpompremmers selectief zijn voorgeschreven aan patiënten met ernstigere cardiovasculaire ziekten en in deze studies niet goed is gecorrigeerd voor vertekening door confounding, hebben deze studies minder bewijskracht dan de COGENT-studie.
COGENT-studie Bij de studie-uitkomst van het COGENT-onderzoek is een aantal kanttekeningen te plaatsen. Ten eerste gebruikte 70% van de patiënten voorafgaand aan de studie al clopidogrel gedurende maximaal 21 dagen.30 Het is onduidelijk of en wanneer deze patiënten een PCI ondergingen. Indien de interactie tussen omeprazol en clopidogrel zich vooral voordoet in de eerste periode na een PCI, doordat vooral dan de kans op trombotische complicaties hoog is, kan deze interactie zijn gemist. Ten tweede is niet duidelijk hoeveel patiënten een PCI ondergingen terwijl ze de combinatie van clopidogrel en omeprazol gebruikten. Verder werden patiënten die een indicatie hadden voor behandeling met een protonpompremmer geëxcludeerd. Het is daardoor mogelijk dat patiënten met ernstige cardiovasculaire ziekten werden geëxcludeerd, omdat men deze patiënten geen protonpompremmer kon onthouden. Een recente meta-analyse concludeert dat een klinisch relevante interactie tussen protonpompremmers en clopidogrel vooral optreedt bij hoogrisicopatiënten (bij een 1-jaarsincidentie van ‘major adverse cardiovascular events’ (MACE) groter dan 10%), maar niet in studies met laagrisicopatiënten (MACE < 10%).43 Verder was het aantal events in de COGENT-studie beperkt. Er is berekend dat een toename in het risico op trombotische complicaties van 44% of minder door te lage statistische power gemist kan zijn.44 Ten slotte is bekend dat genetische variaties van CYP2C19 de effectiviteit van clopidogrel doen afnemen.35 Het is mogelijk dat het CYP2C19-genotype de farmacokinetische interactie tussen omeprazol en clopidogrel beïnvloedt en dat er een subgroep van patiënten bestaat bij wie er wel een klinisch relevante geneesmiddelinteractie is. In de COGENT-studie is een dergelijke analyse niet uitgevoerd.
Consensusdocument De multidisciplinaire werkgroep van het American College of Cardiology Foundation, het American College of Gastroenterology en de American Heart Association (ACCF-ACG-AHA) heeft een consensusdocument uitgebracht met adviezen over de geneesmiddelinteractie.44 Er wordt geadviseerd per patiënt de risico’s en baten van de toevoeging van een protonpompremmer aan de combinatie van clopidogrel en acetylsalicylzuur af te wegen. Protonpompremmers zouden moeten worden voorgeschreven aan patiënten met een gastro-intestinale bloeding in het verleden en patiënten met risicofactoren hiervoor, zoals hoge leeftijd, gebruik van coumarines, behandeling met glucocorticoïden of NSAID’s, of een Helicobacter pylori-infectie. Andere patiënten krijgen door toevoeging van een protonpompremmer aan de behandeling een geringe reductie van het absolute risico op gastro-intestinale bloedingen; bij deze patiëntengroep zou de risico-batenbalans neigen naar het gebruik van trombocytenaggregatieremmers zonder protonpompremmer. De H2-receptorantagonist ranitidine zou bij deze patiënten een plaats kunnen hebben. In het consensusdocument wordt geen uitspraak gedaan welke protonpompremmers de voorkeur hebben bij met clopidogrel behandelde patiënten.44
Interactiestudies Databases voor de registratie van klinische studies laten zien dat momenteel veel interactiestudies met clopidogrel en de verschillende protonpompremmers worden uitgevoerd. Zo wordt in de gerandomiseerde ‘Evaluation of the influence of statins and proton pump inhibitors on clopidogrel antiplatelet effects’(SPICE)-trial (http://clinicaltrials.gov zoeken op: NCT00930670) het effect van individuele protonpompremmers en van ranitidine op plaatjesfunctie onderzocht bij 320 met acetylsalicylzuur en clopidogrel behandelde patiënten die een PCI hebben ondergaan. Ook het effect van CYP2C19*2 op de interactie en het optreden van ‘major adverse cardiovascular events’ 1 jaar na PCI wordt onderzocht. In de nabije toekomst zullen dus aanvullende gegevens ten aanzien van de interactie tussen clopidogrel en protonpompremmers beschikbaar komen.
Conclusie
Omeprazol verlaagt de concentratie van de actieve metaboliet van clopidogrel aanzienlijk en vermindert de trombocytenaggregatieremmende werking. Pantoprazol heeft een veel geringer effect op de farmacokinetiek en de trombocytenaggregatie bij gelijktijdig gebruik van clopidogrel. De effecten van de overige protonpompremmers zijn nog niet in adequaat gerandomiseerde studies onderzocht.
De European Medicines Agency (EMA), de Amerikaanse Food and Drug Administration (FDA) en het College ter Beoordeling van Geneesmiddelen (CBG) waarschuwen dat de combinatie van clopidogrel met omeprazol of esomeprazol, ook een CYP2C19-remmer, vermeden dient te worden. Op dit moment is overigens voor geen enkele protonpompremmer overtuigend een klinisch relevante interactie met clopidogrel aangetoond. Echter, het is niet uit te sluiten dat de interactie in subgroepen van patiënten relevant is.
Leerpunten
Clopidogrel wordt, in combinatie met acetylsalicylzuur, gebruikt ter preventie van trombotische complicaties na een acuut coronair syndroom en na een percutane coronaire interventie (PCI).
Ter bescherming tegen gastro-intestinale complicaties van deze medicatie wordt vaak een protonpompremmer voorgeschreven. Studies naar de interactie tussen protonpompremmers en clopidogrel laten tegenstrijdige resultaten zien.
Clopidogrel wordt door cytochroom P450 (CYP)-enzymen gemetaboliseerd tot de actieve metaboliet; met name CYP2C19 speelt daarbij een belangrijke rol.
Omeprazol en esomeprazol zijn sterke CYP2C19-remmers.
Gelijktijdig gebruik van omeprazol en clopidogrel leidt tot een halvering van de blootstelling aan de actieve metaboliet van clopidogrel en tot een sterk verhoogde trombocytenreactiviteit.
Registratieautoriteiten hebben een waarschuwing geformuleerd en geven aan dat de combinatie van clopidogrel met omeprazol of esomeprazol vermeden dient te worden.
Op dit moment is overigens voor geen enkele protonpompremmer overtuigend een klinisch relevante interactie met clopidogrel aangetoond.
Literatuur
Yusuf S, Zhao F, Mehta SR, Chrolavicius S, Tognoni G, Fox KK. Effects of clopidogrel in addition to aspirin in patients with acute coronary syndromes without ST-segment elevation. N Engl J Med. 2001;345:494-502.
Bhatt DL, Scheiman J, Abraham NS et al. ACCF/ACG/AHA 2008 expert consensus document on reducing the gastrointestinal risks of antiplatelet therapy and NSAID use: a report of the American College of Cardiology Foundation Task Force on Clinical Expert Consensus Documents. J Am Coll Cardiol. 2008;52:1502-17.
Barkun AN, Bardou M, Kuipers EJ et al. International consensus recommendations on the management of patients with nonvariceal upper gastrointestinal bleeding. Ann Intern Med. 2010;152:101-13.
Pereillo JM, Maftouh M, Andrieu A et al. Structure and stereochemistry of the active metabolite of clopidogrel. Drug Metab Dispos. 2002;30:1288-95.
Mega JL, Close SL, Wiviott SD et al. Cytochrome p-450 polymorphisms and response to clopidogrel. N Engl J Med. 2009;360:354-62.
Li XQ, Andersson TB, Ahlstrom M, Weidolf L. Comparison of inhibitory effects of the proton pump-inhibiting drugs omeprazole, esomeprazole, lansoprazole, pantoprazole, and rabeprazole on human cytochrome P450 activities. Drug Metab Dispos. 2004;32:821-7.
Blume H, Donath F, Warnke A, Schug BS. Pharmacokinetic drug interaction profiles of proton pump inhibitors. Drug Saf. 2006;29:769-84.
Andersson T, Hassan-Alin M, Hasselgren G, Rohss K. Drug interaction studies with esomeprazole, the (S)-isomer of omeprazole. Clin Pharmacokinet. 2001;40:523-37.
Frere C, Cuisset T, Quilici J et al. ADP-induced platelet aggregation and platelet reactivity index VASP are good predictive markers for clinical outcomes in non-ST elevation acute coronary syndrome. Thromb Haemost. 2007;98:838-43.
Breet NJ, van Werkum JW, Bouman HJ et al. Comparison of platelet function tests in predicting clinical outcome in patients undergoing coronary stent implantation. Jama. 2010;303:754-62.
Gilard M, Arnaud B, Cornily JC et al. Influence of omeprazole on the antiplatelet action of clopidogrel associated with aspirin: the randomized, double-blind OCLA (Omeprazole CLopidogrel Aspirin) study. J Am Coll Cardiol. 2008;51:256-60.
Yun KH, Rhee SJ, Park HY et al. Effects of omeprazole on the antiplatelet activity of clopidogrel. Int Heart J. 2010;51:13-6.
Cuisset T, Frere C, Quilici J et al. Comparison of omeprazole and pantoprazole influence on a high 150-mg clopidogrel maintenance dose the PACA (Proton Pump Inhibitors And Clopidogrel Association) prospective randomized study. J Am Coll Cardiol. 2009;54:1149-53.
Angiolillo DJ, Gibson CM, Cheng S et al. Differential Effects of Omeprazole and Pantoprazole on the Pharmacodynamics and Pharmacokinetics of Clopidogrel in Healthy Subjects: Randomized, Placebo-Controlled, Crossover Comparison Studies. Clin Pharmacol Ther. 2010;89:65-74.
Small DS, Farid NA, Payne CD et al. Effects of the proton pump inhibitor lansoprazole on the pharmacokinetics and pharmacodynamics of prasugrel and clopidogrel. J Clin Pharmacol. 2008;48:475-84.
Siriswangvat S, Sansanayudh N, Nathisuwan S, Panomvana D. Comparison between the effect of omeprazole and rabeprazole on the antiplatelet action of clopidogrel. Circ J. 2010;74:2187-92.
Sibbing D, Morath T, Stegherr J et al. Impact of proton pump inhibitors on the antiplatelet effects of clopidogrel. Thromb Haemost. 2009;101:714-9.
Siller-Matula JM, Spiel AO, Lang IM, Kreiner G, Christ G, Jilma B. Effects of pantoprazole and esomeprazole on platelet inhibition by clopidogrel. Am Heart J. 2009;157:148.e1-5.
Zuern CS, Geisler T, Lutilsky N, Winter S, Schwab M, Gawaz M. Effect of comedication with proton pump inhibitors (PPIs) on post-interventional residual platelet aggregation in patients undergoing coronary stenting treated by dual antiplatelet therapy. Thromb Res. 2009;125:e51-54.
Neubauer H, Engelhardt A, Kruger JC et al. Pantoprazole does not influence the antiplatelet effect of clopidogrel-a whole blood aggregometry study after coronary stenting. J Cardiovasc Pharmacol. 2010;56:91-7.
Zuern CS, Geisler T, Lutilsky N, Winter S, Schwab M, Gawaz M. Effect of comedication with proton pump inhibitors (PPIs) on post-interventional residual platelet aggregation in patients undergoing coronary stenting treated by dual antiplatelet therapy. Thromb Res. 2010;125:e51-4.
Zairis MN, Tsiaousis GZ, Patsourakos NG et al. The impact of treatment with omeprazole on the effectiveness of clopidogrel drug therapy during the first year after successful coronary stenting. Can J Cardiol. 2010;26:e54-57.
Tsai YW, Wen YW, Huang WF, Chen PF, Kuo KN, Hsiao FY. Cardiovascular and gastrointestinal events of three antiplatelet therapies: clopidogrel, clopidogrel plus proton-pump inhibitors, and aspirin plus proton-pump inhibitors in patients with previous gastrointestinal bleeding. J Gastroenterol. 2010;46:39-45.
Stockl KM, Le L, Zakharyan A et al. Risk of rehospitalization for patients using clopidogrel with a proton pump inhibitor. Arch Intern Med. 2010;170:704-10.
Rassen JA, Choudhry NK, Avorn J, Schneeweiss S. Cardiovascular outcomes and mortality in patients using clopidogrel with proton pump inhibitors after percutaneous coronary intervention or acute coronary syndrome. Circulation. 2009;120:2322-9.
Ray WA, Murray KT, Griffin MR et al. Outcomes with concurrent use of clopidogrel and proton-pump inhibitors: a cohort study. Ann Intern Med. 2010;152:337-45.
O’Donoghue ML, Braunwald E, Antman EM et al. Pharmacodynamic effect and clinical efficacy of clopidogrel and prasugrel with or without a proton-pump inhibitor: an analysis of two randomised trials. Lancet. 2009;374:989-97.
Ho PM, Maddox TM, Wang L et al. Risk of adverse outcomes associated with concomitant use of clopidogrel and proton pump inhibitors following acute coronary syndrome. JAMA. 2009;301:937-44.
Juurlink DN, Gomes T, Ko DT et al. A population-based study of the drug interaction between proton pump inhibitors and clopidogrel. CMAJ. 2009;180:713-8.
Bhatt DL, Cryer BL, Contant CF et al. Clopidogrel with or without omeprazole in coronary artery disease. NEJM. 2010;363:1909-17.
Kreutz RP, Stanek EJ, Aubert R et al. Impact of proton pump inhibitors on the effectiveness of clopidogrel after coronary stent placement: the clopidogrel medco outcomes study. Pharmacotherapy. 2010;30:787-96.
van Boxel OS, van Oijen MG, Hagenaars MP, Smout AJ, Siersema PD. Cardiovascular and Gastrointestinal Outcomes in Clopidogrel Users on Proton Pump Inhibitors: Results of a Large Dutch Cohort Study. Am J Gastroenterol. 2010;105:2430-6.
Charlot M, Ahlehoff O, Norgaard ML et al. Proton-pump inhibitors are associated with increased cardiovascular risk independent of clopidogrel use. Ann Intern Med.2010;153:378-86.
Evanchan J, Donnally MR, Binkley P, Mazzaferri E. Recurrence of acute myocardial infarction in patients discharged on clopidogrel and a proton pump inhibitor after stent placement for acute myocardial infarction. Clin Cardiol. 2010;33:168-71.
Gaglia MA, Torguson R, Hanna N et al. Relation of proton pump inhibitor use after percutaneous coronary intervention with drug-eluting stents to outcomes. Am J Cardiol. 2010;105:833-8.
Gupta E, Bansal D, Sotos J, Olden K. Risk of adverse clinical outcomes with concomitant use of clopidogrel and proton pump inhibitors following percutaneous coronary intervention. Dig Dis Sci. 2010;55:1964-8.
Huang CC, Chen YC, Leu HB et al. Risk of adverse outcomes in Taiwan associated with concomitant use of clopidogrel and proton pump inhibitors in patients who received percutaneous coronary intervention. Am J Cardiol. 2010;105:1705-9.
Sarafoff N, Sibbing D, Sonntag U et al. Risk of drug-eluting stent thrombosis in patients receiving proton pump inhibitors. Thromb Haemost. 2010;104:626-32.
Tentzeris I, Jarai R, Farhan S et al. Impact of concomitant treatment with proton pump inhibitors and clopidogrel on clinical outcome in patients after coronary stent implantation. Thromb Haemost. 2010;104:1211-8.
Valkhoff VE, ’t Jong GW, Van Soest EM, Kuipers EJ, Sturkenboom MC. Risk of recurrent myocardial infarction with the concomitant use of clopidogrel and proton pump inhibitors. Aliment Pharmacol Ther. 2011;33:77-88.
Wu CY, Chan FK, Wu MS et al. Histamine2-receptor antagonists are an alternative to proton pump inhibitor in patients receiving clopidogrel. Gastroenterology. 2010;139:1165-71.
Siller-Matula JM, Jilma B, Schror K, Christ G, Huber K. Effect of proton pump inhibitors on clinical outcome in patients treated with clopidogrel: a systematic review and meta-analysis. J Thromb Haemost. 2010;8:2624-41.
Hulot JS, Collet JP, Silvain J et al. Cardiovascular risk in clopidogrel-treated patients according to cytochrome P450 2C19*2 loss-of-function allele or proton pump inhibitor coadministration: a systematic meta-analysis. J Am Coll Cardiol. 2010;56:134-43.
American College of Cardiology Foundation Task Force on Expert Consensus Documents. ACCF/ACG/AHA 2010 Expert Consensus Document on the Concomitant Use of Proton Pump Inhibitors and Thienopyridines: A Focused Update of the AACF/ACG/AHA 2008 Expert Consensus Document on Reducing the Gastrointestinal Risks of Antiplatelet Therapy and NSAID Use. J Am Coll Cardiol. 2010;56:2051-66.







Reacties