Samenvatting
In Nederland lopen landelijke screeningsprogramma’s naar borst- en baarmoederhalskanker, terwijl die voor darmkanker in voorbereiding is. Experimentele studies naar het effect van screening op prostaatkanker en longkanker zijn inmiddels uitgevoerd.
Met deze bevolkingsonderzoeken wordt de sterfte aan deze vormen van kanker verminderd. Maar de programma’s hebben ook nadelen, bijvoorbeeld de achteraf gebleken onnodige verwijzingen voor definitieve diagnostiek in het ziekenhuis.
Een gemiddeld ziekenhuis zal op jaarbasis te maken krijgen met 156 vrouwen verwezen via de screening voor borstkanker, 79 voor baarmoederhalskanker en bijna 1100 personen voor colorectale kanker.
Een gemiddelde huisartspraktijk krijgt te maken met 3 positieve screeningsadviezen per jaar in verband met mammacarcinoom, jaarlijks bijna 1 verwezene voor cervixcarcinoom of een voorstadium daarvan en 2-jaarlijks een patiënte met CIN III. Bij colorectumkanker gaat het om een aantal van circa 22 verwezenen, van wie er 8 adenoom of kanker zullen hebben.
artikel
Van de Nederlanders krijgt 1 op de 3 vroeg of laat een vorm van kanker.1,2 En ondanks therapie overlijdt 1 op de 6 Nederlanders aan kanker. Qua ziektelast betreft het vooral kanker van het colon en rectum, long, borst en prostaat (bron: Nederlandse Kankerregistratie 2011: www.ikcnet.nl).
De laatste decennia is de prognose verbeterd doordat enerzijds behandelingen zijn verbeterd en anderzijds kanker vaker in een vroeg ziektestadium wordt gediagnosticeerd. De stadiumverschuiving bij baarmoederhals- en borstkanker is vooral teweeggebracht door de georganiseerde bevolkingsonderzoeken.3,4
In dit artikel gaan wij in op de balans van voor- en nadelen in maat en getal van onze lopende en beoogde bevolkingsonderzoeken.
Gepubliceerd bewijs voor sterftevermindering
Wetenschappelijk bewijs voor de effectiviteit van screening, maar ook voor de ongewenste effecten, komt bij voorkeur uit gerandomiseerde studies.
Borstkanker Voor screening op borstkanker met mammografie heeft een groot aantal trials plaatsgevonden in de jaren 70 en 80 van de vorige eeuw. De gecombineerde resultaten van deze trials laten een verlaging van de borstkankersterfte zien van ongeveer 25%.5,6 De niet-gerandomiseerde Nederlandse studies leverden in de beginjaren maar ook nu nog bewijs voor de effectiviteit van dit programma.7,8 Daarnaast levert de continue evaluatie van het huidige landelijke bevolkingsonderzoek een belangrijke bijdrage.9
Deze uitkomsten gaven en geven aanleiding tot een stevige discussie of screening daadwerkelijk levens spaart.10-12 Het is daarbij de vraag of de winst in overleving door de verbeterde behandeling screening wellicht overbodig zou maken.13 Echter, juist de combinatie van screening – en daarmee detectie in een vroeg stadium – en adequate behandeling in dit vroege stadium maken de screening tot een succes.14
Baarmoederhalskanker Hoe anders is dit verlopen voor de screening op baarmoederhalskanker.15 Er is nimmer gerandomiseerd onderzoek uitgevoerd naar de effectiviteit. In Nederland werden weliswaar halverwege de jaren 70 van de vorige eeuw 3 proefbevolkingsonderzoeken gestart, maar de uitkomsten hiervan werden onder politieke druk niet afgewacht.16 Ook in andere landen is wetenschappelijk bewijs over een gunstig effect op de ziektelast uitsluitend vergaard met observationeel onderzoek. Dit in tegenstelling tot de zorgvuldigheid waarmee op dit moment nieuwe technieken – zoals de dunnelaagcytologie en de test voor hoogrisico-humaan-papillomavirus (hrHPV-test) – worden vergeleken met cytologisch onderzoek als primaire screeningstest.
Darmkanker Recent is in een aantal Europese landen bevolkingsonderzoek naar darmkanker geïntroduceerd. De basis hiervoor werd gelegd in 4 gerandomiseerde trials waarin werd aangetoond dat sterfte aan darmkanker met 11-18% kan worden verminderd via een aanbod van een test op fecaal occult bloed elke 2 jaar.17 Voor darmkanker is in Nederland recent het besluit genomen om de screening vanaf 2013 in te voeren met een test die op immunologische basis onzichtbare bloedsporen vaststelt (immunochemische fecaal-occultbloedtest (iFOBT)). Er zijn voor darmkanker veel verschillende screeningsmethoden beschikbaar (ontlastingstesten, sigmoïdoscopie, colografie, coloscopie), die verschillen in onder andere gevoeligheid en belasting voor en acceptatie door de doelgroep. Voor elk van deze screeningsmethoden zijn of worden gerandomiseerde trials uitgevoerd.
Prostaatkanker Een andere kandidaat voor bevolkingsonderzoek is prostaatkanker. Echter, de meeste mannen gaan mét prostaatkanker dood, niet áán prostaatkanker. Dat betekent dat overdiagnose en daarmee gepaard gaande overbehandeling een serieus probleem vormen. Daarnaast wordt de bloedtest op prostaatspecifiek antigeen (PSA) gekenmerkt door een lage specificiteit. Dit betekent dat veel mannen nadeel zullen ondervinden vanwege foutpositieve screeningsuitslagen. De meeste gerandomiseerde trials die tot dusverre zijn uitgevoerd, waren zwak van opzet en vonden geen effect van screening op overlijden door prostaatkanker.18 Dit in tegenstelling tot de door de Erasmus Universiteit gecoördineerde ‘European randomized study for screening of prostate cancer’ (ERSPC), die in 2009 rapporteerde dat 4-jaarlijkse screening met PSA-test tot een sterftereductie van minimaal 20% leidt.19 De screening gaat echter gepaard met een onacceptabele mate van overdiagnostiek en overbehandeling. 1410 mannen zouden moeten worden gescreend en 48 behandeld om 1 overlijden aan prostaatkanker te voorkomen.19
Longkanker De laatste actuele kandidaatziekte betreft longkanker. Waar in 2008 in een Commentaar in het Tijdschrift nog huiver bestond jegens CT-screening,20 laat de Amerikaanse ‘National lung cancer screening trial’ gunstige resultaten zien.21 In dit onderzoek zijn ruim 53.000 rokers (48%) en ex-rokers (52%) gerandomiseerd voor 3 maal een jaarlijkse lage-dosis-CT-scan of röntgenfoto van de thorax. Een 20% lagere longkankersterfte werd gevonden in de CT-groep. Echter, bijna een kwart van de CT-onderzoeken had een positieve uitslag, waarvan ruim 96% fout-positief. Daarnaast werden 13% meer tumoren gediagnosticeerd in de CT-groep, waarbij het vooralsnog onduidelijk is of dit ‘overdiagnostiek’ of ‘vroege diagnostiek’ betreft. Vooralsnog wordt afgeraden om spiraal-CT te laten verrichten als screeningstest bij personen zonder enige verdenking op longkanker. Wanneer rokers om deze screeningstest vragen, kan de huisarts dit met hen bespreken, maar ook dat rokers hun sterfterisico met 50% in plaats van 20% kunnen verlagen door te stoppen met roken.
Zoeken naar asymptomatisch carcinoom
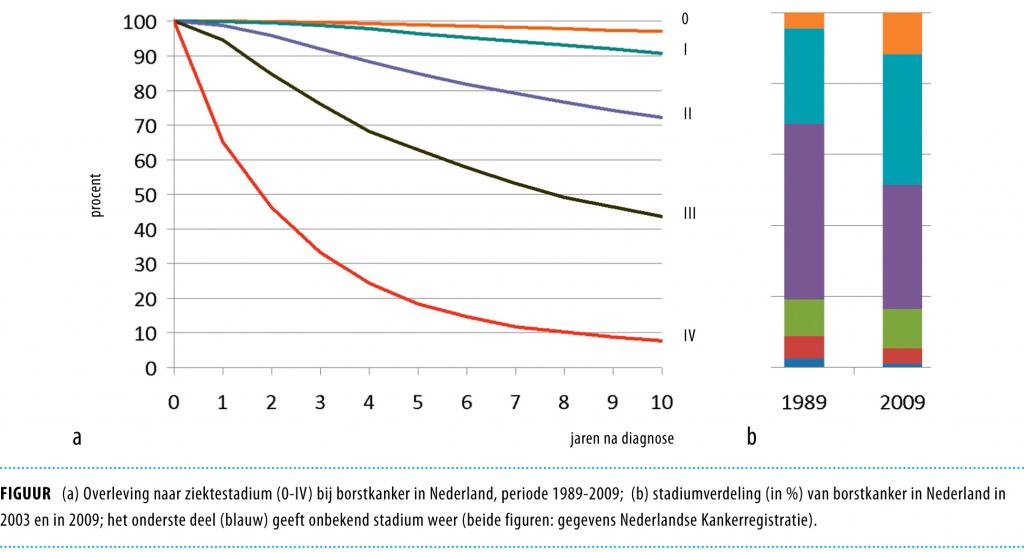
Er is een belangrijke relatie tussen het ziektestadium bij diagnose en de overleving na behandeling van het carcinoom.22 Dit is gevisualiseerd in figuur 1 met de relatieve overlevingscurve naar ziektestadium bij borstkanker. ‘Relatief’ wil in dit verband zeggen: gecorrigeerd voor andere sterfteoorzaken die vooral op oudere leeftijd een rol spelen. Mede door het landelijke bevolkingsonderzoek dat in 1989 in Nederland van start is gegaan, heeft een belangrijke ‘linksverschuiving’ naar vroege stadia plaatsgevonden. Onder de assumptie dat er een directe relatie is tussen ziektestadium en overleving is een schatting te maken van het effect van vroege diagnostiek – oftewel verschuiving van de diagnose naar een vroeger ziektestadium – op de vermindering van de sterfte. Daarbovenop komt het effect van het ontdekken van borstkanker in het asymptomatische stadium.
Deelnemer – huisarts – ziekenhuis
Dankzij de bevolkingsonderzoeken zal verdere verschuiving in ziektestadium optreden door ontdekking van carcinomen die niet tot symptomen hebben geleid. Voor de beide lopende bevolkingsonderzoeken naar borstkanker en baarmoederhalskanker en het aanstaande naar colorectumcarcinoom zijn de screeningsuitkomsten in de tabel getalsmatig weergegeven.
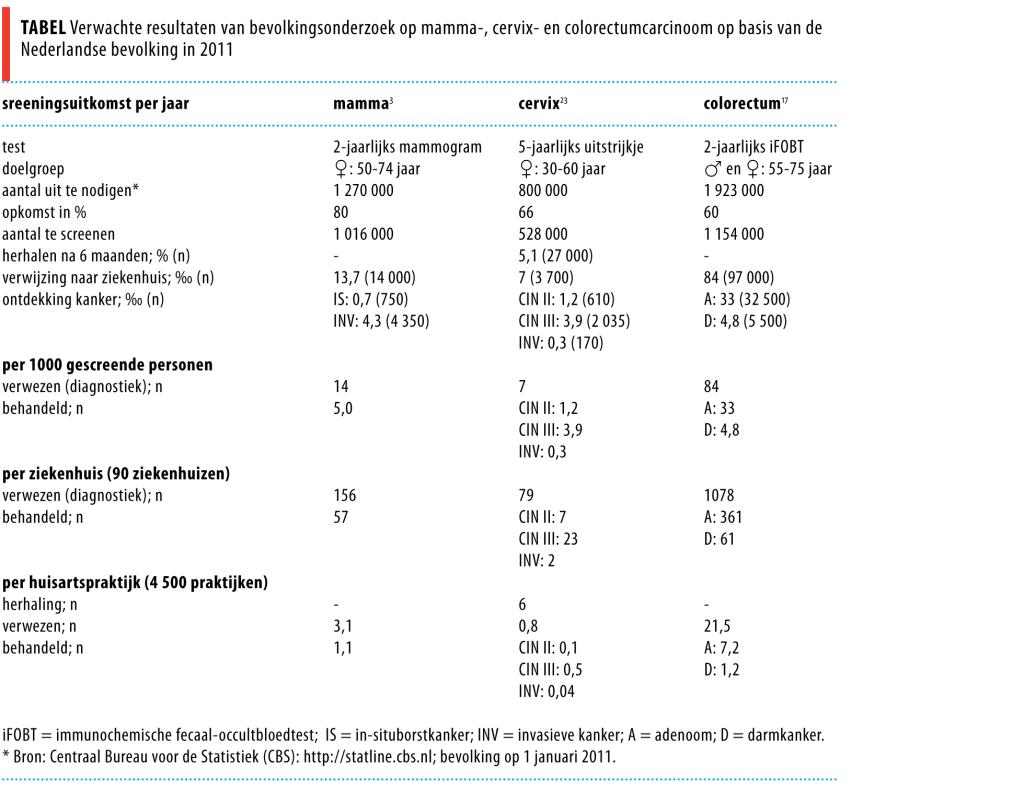
Bij de mammascreening zullen van de 1000 gescreende vrouwen 14 via de huisarts naar het ziekenhuis worden verwezen voor nadere diagnostiek. Bij 5 van de 14 zal kanker worden vastgesteld, bij 9 niet. Vanuit de cervixscreening worden minder vrouwen verwezen, maar bij vergelijkbare aantallen wordt CIN II of hoger gediagnosticeerd. Screening op colorectale kanker kent hogere verwijsaantallen door de geringere specificiteit van iFOBT: van de 1000 mannen en vrouwen zullen naar verwachting 84 personen het advies voor nadere diagnostiek in het ziekenhuis krijgen.
Uitgaande van 90 ziekenhuizen in Nederland betekenen deze aantallen dat een gemiddeld ziekenhuis op jaarbasis te maken krijgen met 156 via de screening verwezen vrouwen voor borstkanker respectievelijk 79 voor baarmoederhalskanker en bijna 1100 personen voor colorectale kanker.
Een gemiddelde huisartspraktijk krijgt te maken met 3 positieve screeningsadviezen per jaar in verband met mammacarcinoom, waarvan 1 kanker zal zijn. Voor cervixcarcinoom of een voorstadium daarvan is er jaarlijks bijna 1 verwezene en 2-jaarlijks een patiënte met CIN III. Wel zal de huisarts jaarlijks bij 6 patiënten een nieuw uitstrijkje maken. Bij colorectumkanker gaat het om een aantal van afgerond 22 verwezenen, van wie er 8 adenoom of kanker zullen hebben.
Dilemma’s bij kankerscreening
Vroege ontdekking niet altijd gunstiger Ontdekking en verwijdering van een woekering in een beginstadium resulteert vaak in genezing. Maar vroege ontdekking van het carcinoom is problematisch. Een tumor van 1 cm diameter is minder dan 0,1‰ van de totale lichaamsomvang. Daar komt bij dat vroege kankercellen nog veel lijken op onveranderde cellen. En zelfs als het carcinoom vroeg is ontdekt en behandeld, dan hoeft dit nog geen genezing te betekenen. Ook al is het carcinoom in het latente stadium van de ontwikkeling, uitzaaiingen elders in het lichaam, hoe klein ook en niet ontdekt, kunnen later gaan opspelen. Er is heel weinig bekend over de progressiekans van een vroeg ontdekte afwijking tot een infauste maligniteit binnen de huidige levensverwachting.
Daarnaast is geen enkele vorm van vroege diagnostiek perfect. Behalve terechtpositieve uitslagen zullen er ook altijd foutpositieve en foutnegatieve screeningsuitkomsten zijn. Zelfs de terechtpositieve screeningsuitkomsten (detectie van kanker) zijn niet altijd pure winst. Want ook de vroege detectie kan blijken toch een niet-tijdige detectie te zijn geweest, betrokkene kan komen te overlijden aan iets anders (multimorbiditeit) en de behandeling van de tumor in het symptomatische ziektestadium zou al afdoende geweest kunnen zijn.
Leeftijdsgrenzen Een ander dilemma betreft de leeftijdsgrenzen, die thans met name bij borstkanker ter discussie staan. De onderste leeftijdsgrens is vooral ingegeven door de mindere testeigenschappen van de screeningsmammografie bij premenopauzale vrouwen. De incidentie neemt echter fors toe, met name in de groep van 45-49 jaar, terwijl inmiddels met de digitale mammografie een betere test voorhanden is. De bovenste leeftijdsgrens is ingegeven doordat minder levensjaren te winnen zijn, maar veel vrouwen van 75 jaar en ouder zijn in uitstekende conditie en hebben nog een levensverwachting van minimaal 13 jaar.
Nieuwe ontwikkelingen bij screeningtests
Deze dilemma’s dient men ook in ogenschouw te nemen bij nieuwe technologische ontwikkelingen voor screeningstests. De perfecte screeningstest detecteert alle kanker en voorstadia ervan die een betere prognose hebben bij vroeg ingrijpen, en geeft een negatieve uitslag in alle andere gevallen. Zo’n test bestaat echter voor geen enkele vorm van kanker. Mondiaal vindt daarom enorm veel onderzoek plaats naar nieuwe biomarkers en beeldvormende technieken met nog beter discriminerend vermogen. Treffend wordt dit geïllustreerd bij het bevolkingsonderzoek naar baarmoederhalskanker. De Gezondheidsraad heeft op 24 mei 2011 de Minister geadviseerd om het onderzoek uit te breiden met een test op hrHPV, de veroorzaker van baarmoederhalskanker.16 Een uitstrijkje wordt dan eerst beoordeeld op aanwezigheid van hrHPV. Alleen wanneer deze test positief is zal als tweede test het uitstrijkje cytologisch worden beoordeeld. Bij een positieve cytologische uitslag (Pap2 of hoger) volgt verwijzing naar de gynaecoloog. Bij een negatieve cytologische uitslag wordt een controle-uitstrijkje (voor cytologisch onderzoek) over 6 maanden geadviseerd; ook het aantal screeningsmomenten voor een vrouw zal dan teruggebracht kunnen worden van 7 naar 5, namelijk op de leeftijd 30, 35, 40, 50 en 60 jaar.
De PSA-test bij prostaatkankerscreening gaat gepaard met circa 50% overdiagnostiek.19 Mondiaal wordt daarom naarstig gezocht naar nieuwe biomarkers die de klinisch relevante prostaatcarcinomen opsporen, maar die ongevoelig zijn voor de onschuldige tumoren. Een goede kandidaat leek de in Nijmegen en Baltimore ontwikkelde PCA3-urinetest, maar ook deze test zal te veel overdiagnostiek geven.24 Ook andere biomarkers, zoals een fusieproduct van de genen TMPRSS en ERG gemeten in de urine, kunnen vooralsnog onvoldoende onderscheid maken tussen onschuldige en agressieve prostaattumoren.
Risicostratificatie
Naast de zoektocht naar nieuwe, betere screeningtests is het wellicht mogelijk om het screeningsprotocol aan te passen aan het risico op kanker van verschillende groepen van de populatie.
Alternatieven voor leeftijd Lang was leeftijd in feite de enige risicofactor die de definitie van de doelgroep bepaalde. Maar het voorspellend vermogen daarvan is uitermate beperkt. Het genoemde advies van de Gezondheidsraad om cytologisch onderzoek van het uitstrijkje als eerste test te vervangen door de hrHPV-test is een voorbeeld van risicostratificatie. In het bevolkingsonderzoek op borstkanker zijn plannen voor een gerandomiseerde studie ter evaluatie van de kosten en baten van een MRI voor de vrouwen die bij een mammogram dicht borstweefsel blijken te hebben (de DENSE-trial). En mogelijk wordt in de nabije toekomst voor die subgroep van vrouwen ook 3-dimensionale echografie (‘automated breast volume scanning’ (ABVS)) als tweede screeningstest geëvalueerd.
Risico-allelen Sinds 2007 zijn in genoomwijde associatiestudies honderden nieuwe genetische gevoeligheidsmarkers geïdentificeerd, alleen voor prostaatkanker zijn dit er al ongeveer 40. Het extra risico voor een man met het hoogrisico-allel van een van deze markers is zeer gering. Maar de combinatie van enkele tientallen hoogrisico-allelen is een betere voorspeller voor prostaatkanker dan bijvoorbeeld leeftijd. Er wordt gesuggereerd dat bepaling van het genetisch profiel van een man als voorscreening gebruikt zou kunnen worden.17 Maar het lijkt vooralsnog niet logisch om de gehele mannelijke bevolking te genotyperen voor de identificatie van een kleine groep waarvoor screening wel of niet nuttig zou zijn. Voor de grote groep van mannen die niet in de extremen van de risicodistributie terecht komt, brengt de genotypering grote onduidelijkheid met zich mee. Daarnaast voorspellen de tot dusverre geïdentificeerde markers weliswaar prostaatkanker op zich, maar niet de agressiviteit van de tumor.
Maatschappelijke aspecten
Voor invoering van bevolkingsonderzoek is het essentieel dat de balans tussen voor- en nadelen bekend en voldoende gunstig is. Wetenschappelijk bewijs voor de effectiviteit van screening, maar ook voor de ongewenste effecten ervan, komt bij voorkeur uit gerandomiseerde klinische trials. Dergelijk resultaat rechtvaardigt dan bijvoorbeeld een terughoudend beleid van artsen in het aanbieden van een PSA-test aan mannen zonder klachten. Echter, de consument heeft hierin ook een eigen stem. Steeds meer testen worden aangeboden in een commerciële setting of zijn zelfs gewoon bij de drogist of via internet verkrijgbaar,25 onder het mom van: ‘baat het niet, dan schaadt het niet’. Maar dit gaat voor de meeste bevolkingsonderzoeken niet op.
De effectiviteit van een screeningsprogramma is een noodzakelijke, maar geen voldoende voorwaarde voor het implementeren van een programma georganiseerd en bekostigd door de overheid. De mate van effectiviteit op populatieniveau hangt sterk af van de deelnamegraad. Een effectief programma is dus niet per definitie ook een doelmatig programma en bij beperkte middelen moet men keuzes maken. Een belangrijke maat voor doelmatigheid is de kosteneffectiviteit, waarbij de gezondheidswinst (levensverwachting, kwaliteit van leven) wordt afgewogen tegen de kosten en besparingen.26
Veelal zet men voor dit soort analyses simulatiemodellen in om verschillende screeningstrategieën door te rekenen op hun effectiviteit en gerelateerde kosten. Omdat elk model wordt gevoed door aannames van de onderzoekers, kunnen de uitkomsten van modellen verschillen. Voor de huidige bevolkingsonderzoeken naar baarmoederhalskanker en borstkanker liggen de kosten ruim onder de grenswaarde van 20.000 euro per gewonnen levensjaar, gecorrigeerd voor de kwaliteit van leven.11-13
Conclusie
Bevolkingsonderzoek impliceert allerlei individuele, maatschappelijke en zorgeconomische overwegingen. Mammascreening inclusief het natraject kost per jaar 100 miljoen euro, cervixscreening kost 30 miljoen per jaar, en in 2013 zal eindelijk een start worden gemaakt met het bevolkingsonderzoek op darmkanker tegen enkele tientallen miljoenen per jaar. In 2009 had de minister al positief gereageerd op het Gezondheidsraadadvies, maar hij implementeerde het niet vanwege gebrek aan financiële middelen. Die financiële situatie is op zich niet veranderd, maar de minister heeft vanwege de urgentie van het onderwerp toch besloten tot een geleidelijke invoering. De benodigde middelen zijn gevonden uit de beëindiging van de financiering van campagnes voor en onderzoek naar gezonde leefstijl (sic).
Leerpunten
Dankzij periodieke screening op borstkanker, baarmoederhalskanker en colorectale kanker worden deze aandoeningen eerder behandeld en is de sterfte navenant verminderd.
Door onvolkomenheden van screeningstests blijft vroege ontdekking van kanker problematisch, met foutpositieve testuitslagen tot gevolg. De frequentie hiervan bedraagt voor borst- en baarmoederhalskankerscreening minder dan 0,5% en voor colorectumkanker 5%.
Lopende gerandomiseerde studies naar de effecten van prostaatkanker- en longkankerscreening laten zien dat de nadelen, in de zin van foutpositieve screening plus overdiagnose, de voordelen nog overschaduwen.
Literatuur
Kiemeney LALM, Lemmers FAMO, Verhoeven RHA, et al. De kans op kanker voor Nederlanders. Ned Tijdschr Geneeskd. 2008;152:2233-41. Medline. Medline
Signaleringscommissie Kanker van KWF Kankerbestrijding. Kanker in Nederland tot 2020: Trends en prognose. Oisterwijk: VDB Almedeon; 2011.
Landelijk Evaluatie Team voor Bevolkingsonderzoek naar Borstkanker (LETB). Landelijke evaluatie van bevolkingsonderzoek naar borstkanker in Nederland 1990-2007 (LETB XII). Rotterdam: LETB; 2009 link.
Peto J, Gilham C, Fletcher O, Matthews FE. The cervical cancer epidemic that screening has prevented in the UK. Lancet. 2004; 364:249-56 Medline.
Nyström L, Andersson I, Bjurstam N, Frisell J, Nordenskjöld B, Rutqvist LE. Long-term effects of mammography screening: updated overview of the Swedish randomised trials. Lancet. 2002;359:909-19 Medline.
Gøtzsche PC, Nielsen M. Screening for breast cancer with mammography. Cochrane Database Syst Rev. 2011;1: CD001877 Medline.
Verbeek ALM, Hendriks JHCL, Holland R, Mravunac M, Sturmans F, Day NE. Reduction of breast cancer mortality through mass screening with modern mammography. First results of the Nijmegen project, 1975-1981. Lancet. 1984;323:1222-4 Medline.
Collette HJ, Day NE, Rombach JJ, de Waard F. Evaluation of screening for breast cancer in a non-randomised study (the DOM project) by means of a case-control study. Lancet. 1984;323:1224-6 Medline.
Otten JD, Broeders MJ, Fracheboud J, Otto SJ, de Koning HJ, Verbeek AL. Impressive time-related influence of the Dutch screening programme on breast cancer incidence and mortality, 1975-2006. Int J Cancer. 2008;123:1929-34 Medline.
Tabár L, Vitak B, Chen TH, Yen AM, Cohen A, Tot T, Chiu SY, Chen SL, Fann JC, Rosell J, Fohlin H, Smith RA, Duffy SW. Swedish Two-County Trial: Impact of mammographic screening on breast cancer mortality during 3 decades. Radiology. 2011;260:658-63 Medline.
Kopans DB, Smith RA, Duffy SW. Mammographic screening and "overdiagnosis". Radiology. 2011;260:616-20. Medline.
Jørgensen KJ, Keen JD, Gøtzsche PC. Is mammographic screening justifiable considering its substantial overdiagnosis rate and minor effect on mortality? Radiology. 2011;260:621-7 Medline.
Fletcher SW, Elmore JG. More on screening mammography. N Engl J Med. 2011;364:285-6. Medline.
Mook S, Van ‘t Veer LJ, Rutgers EJ, Ravdin PM, van de Velde AO, van Leeuwen FE, Visser O, Schmidt MK. Independent prognostic value of screen detection in invasive breast cancer. J Natl Cancer Inst. 2011;103:585-97 Medline.
Gezondheidsraad. Jaarbericht bevolkingsonderzoek 2006. Den Haag: Gezondheidsraad; 2006 link.
Gezondheidsraad. Screening op baarmoederhalskanker. Den Haag: Gezondheidsraad; 2011 link.
Gezondheidsraad. Bevolkingsonderzoek naar darmkanker. Den Haag: Gezondheidsraad; 2009 link.
Djulbegovic M, Beyth RJ, Neuberger MM, Stoffs TL, Vieweg J, Djulbegovic B, Dahm P. Screening for prostate cancer: systemic review and meta-analysis of randomised controlled trials. BMJ. 2010;341:c4543 Medline.
Schröder FH, Hugosson J, Roobol MJ, Tammela TL, Ciatto S, Nelen V, et al. Screening and prostate-cancer mortality in a randomized European study. N Engl J Med. 2009; 360:1320-8 Medline.
Van Klaveren RJ, Oudkerk M, Mali WPThM, de de Koning HJ. Screenen op longkanker met de multidetector-CT: voorlopig nog af te raden. Ned Tijdschr Geneeskd. 2008;152:125-8 Medline.
National Lung Screening Trial Research Team, Aberle DR, Adams AM, Berg CD, Black WC, Clapp JD, Fagerstrom RM, Gareen IF, Gatsonis C, Marcus PM, Sicks JD. Reduced lung-cancer mortality with low-dose computed tomographic screening. N Engl J Med. 2011;365:395-409 Medline.
Autier P, Héry C, Haukka J, Boniol M, Byrnes G. Advanced breast cancer and breast cancer mortality in randomized controlled trials on mammography screening. J Clin Oncol. 2009;27:5919-23 Medline.
Landelijk Evaluatie Bevolkingsonderzoek Baarmoederhalskanker. LEBA rapportage 2009. Rotterdam: Erasmus MC; 2009 link.
Roobol M. Is prostate cancer screening good or bad? Summary of a debate at the innovation in urology meeting, september 17-19, 2010, Milan, Italy. Eur Urol. 2011;59:359-62 Medline.
Aly M, Wiklund F, Grönberg H. Early detection of prostate cancer with emphasis on genetic markers. Acta Oncol. 2011;50 (Suppl 1):18-23 Medline.
Gezondheidsraad. Screening: tussen hoop en hype. Den Haag: Gezondheidsraad; 2008 link.




Verantwoord screenen op kanker
Wie het artikel van Verbeek et al. over kankerscreening leest, zou ook het stukje van collega Susan Bewley in een recent nummer van de BMJ moeten lezen (BMJ 2011;343:d6894). Om de vraag te beantwoorden of zij aan mammascreening mee moest doen, ging zij op zoek naar wetenschappelijke informatie en kwam tot de ontdekking dat de stellige informatie over dit preventieve onderzoek in de aan haar gercihte oproep maar ook in sommige wetenschappelijke artikelen geen recht doet aan de feitelijke situatie. Haar conclusies:
- De 'winst' van kankerscreening wordt overtrokken; die is er wel maar veel minder dan geclaimd en steeds meer onderzoek laat zien dat het profijt marginaal is.
- Er is zowel van overdiagnostiek als overbehandeling sprake. Die is beduidender dan de voorstanders van screening willen toegeven.
Kankerscreening is een geen simpele diagnostiek maar een interventie waarvan de beoordeling van de effecten, zowel positief als negatief en op korte zowel als lange termijn, uiterst complex is. Niet alleen 'blote' getallen maar ook de (veelal subjectieve) belevingswaarde die men daaraan toekent is van belang.
Niet alleen in ons land, maar bijvoorbeeld ook in de UK, is de discussie over nut en noodzaak van kankerscreening ontaard in een loopgravenoorlog.
Wat nodig is bij dit vraagstuk is niet alleen het beschrijven van 'the big picture' maar ook dat de angst voor kanker mensen ertoe aanspoort maar liever mee te willen doen. Zij denken dan: baat het niet, het schaadt toch ook niet? De actuele stand van borstkankerscreening is feitelijk dat het marginaal baat en dat het zeker schaadt.
Dit NTvG-themanummer gaat over de 'oorlog' tegen kanker. Dat is een begrijpelijke maar ongepaste metafoor. Objectiviteit is altijd het eerste slachtoffer van oorlog. Het thema screening gaat over een eeuwenoud en problematisch kennistheoretisch dillema: hoe stel ik oorzakelijkheidsrelaties vast? Daarnaast blijkt dat bij het zoeken naar een eenduidig antwoord op de vraag 'doet screening de sterfte aan kanker dalen?' dit een te beperkte probleemstelling is. Daarom spreken Bewley's vragen me meer aan dan de stellige taal van Verbeek et al. Aristoteles zei het al: in de geneeskunde eindigt de filosofie meestal waar die juist zou moeten beginnen.
Raimond Giard, patholoog, klinisch epidemioloog
Verantwoord screenen op kanker?
"betrokkene kan komen te overlijden aan iets anders (multimorbiditeit)". Dit is het enige zinnetje in het artikel van Verbeek cs over 'verantwoord screenen' dat zou kunnen wijzen op het probleem dat bij screening 30 - 50 % meer kanker wordt gevonden dan anders bij leven zichtbaar zou zijn geweest.
Giard sprak en spreekt voor zich zelf, maar dit zinnetje van hem uit 2004 mag hier worden herhaald: "De auteurs (1) berekenen dan ook dat een op de drie met screening ontdekte mammacarcinomen nooit manifest zou zijn geworden zonder screening." Wat eenmaal is ontdekt, moet worden behandeld. Dit betekent dat de schade van kankerscreening enorm is. De mate waarin deze schade niet wordt vermeld of in eufemismen en terzijdes terloops wordt afgedaan, is onthutsend en onprofesioneel.
Hans Schilder, SEH arts, psychodramatherapeut/ psycho-oncoloog
Zahl PH, Strand BH, Maehlen J. Incidence of breast cancerin Norway and Sweden during introduction of nationwidescreening prospectivecohort study. BMJ 2004;328:921-4.