Toets voor nascholing (verlopen)
Aan dit leerartikel was een toets gekoppeld waarmee je nascholingspunten kon verdienen.
Samenvatting
Lithium is de effectiefste onderhoudsbehandeling voor patiënten met een bipolaire stoornis.
Belangrijke renale bijwerkingen van chronisch lithiumgebruik zijn nefrogene diabetes insipidus (prevalentie: circa 20%) en chronische nierinsufficiëntie (prevalentie: circa 10-20% na 5-9 jaar gebruik).
Chronisch lithiumgebruik is gerelateerd aan langzaam progressieve nierinsufficiëntie, die zelden leidt tot terminaal nierfalen (prevalentie: 0,5-1,5%).
Het is op dit moment niet goed te voorspellen welke patiënten vatbaar zijn voor de renale bijwerkingen van lithium. De belangrijkste risicofactoren voor deze bijwerkingen zijn leeftijd, duur van het lithiumgebruik en chronische blootstelling aan hoog-therapeutische lithiumspiegels.
Voor de meeste patiënten met chronische nierinsufficiëntie is het onduidelijk of het staken van lithium voordelen oplevert.
Op basis van gedeelde besluitvorming kan voortzetting van de lithiumbehandeling, ondanks renale complicaties, een keuze zijn.
Vervolgonderzoek kan zich richten op mogelijke determinanten van een goede lithiumrespons, mogelijke voorspellers van renale bijwerkingen van lithiumgebruik en het effect van medicamenteuze interventies op renale bijwerkingen.
Kernpunten
Belangrijke renale bijwerkingen van chronisch lithiumgebruik zijn nefrogene diabetes insipidus en chronische nierinsufficiëntie.
Nefrogene diabetes insipidus is hinderlijk maar niet gevaarlijk mits iemand een adequate dorstprikkel heeft en de waterinname voldoende gegarandeerd is.
Chronisch lithiumgebruik leidt zelden tot terminaal nierfalen.
De belangrijkste risicofactoren voor renale bijwerkingen van lithium zijn leeftijd, duur van het lithiumgebruik en hoog-therapeutische lithiumspiegels.
Het is onduidelijk wat de voordelen zijn van het staken van lithium bij patiënten met chronische nierinsufficiëntie.
Op basis van gedeelde besluitvorming kan voortzetting van lithiumbehandeling, ondanks renale complicaties, een keuze zijn.
Bij lithium-geïnduceerde chronische nierinsufficiëntie moet aandacht besteed worden aan cardiovasculair risicomanagement volgens de multidisciplinaire richtlijn ‘Chronische nierschade’.
artikel
Casus
Een 35-jarige vrouw is op haar 16e gediagnosticeerd met een bipolaire stemmingsstoornis type I. Zij heeft meerdere ernstige manisch-psychotische episoden met gedwongen opnamen doorgemaakt. Op haar 20e is zij begonnen met een onderhoudsbehandeling met lithium, waar zij goed op reageerde; sindsdien heeft zij geen depressies of manieën meer gehad. Gedurende de afgelopen 15 jaar waarin zij lithium gebruikte is haar nierfunctie echter gestaag achteruitgegaan: de kreatinineconcentratie steeg van 70 naar 100 µmol/l en de geschatte glomerulaire filtratiesnelheid (eGFR) daalde tot 55 ml/min per 1,73 m2 (zie uitleg). Wat is het beleid omtrent het lithiumgebruik bij deze patiënte? En wat zijn hierbij belangrijke afwegingen?
Lithium is de medicamenteuze behandeling van eerste keuze voor patiënten met een bipolaire stoornis. Lithium is niet alleen de effectiefste onderhoudsbehandeling ter preventie van depressieve, manische of hypomanische episoden, maar wordt ook gebruikt bij de behandeling van een acute manie of bipolaire depressie, waarbij het vaak gecombineerd wordt met andere middelen.1 Bovendien heeft lithium een onafhankelijk effect op het voorkómen van suïcides.1 Daarnaast wordt lithiumadditie voorgeschreven aan patiënten met een unipolaire depressie die onvoldoende reageert op antidepressiva.2 Op deze manieren kan lithium de kwaliteit van leven van de patiënt en diens naasten verbeteren.3
Ondanks de bewezen superieure effectiviteit van lithium bestaat er terughoudendheid in het voorschrijven van dit medicijn vanwege de mogelijke bijwerkingen.4 Lithium is potentieel toxisch bij bloedspiegels > 1,2 mmol/l en mogelijk fataal bij spiegels ≥ 2,0 mmol/l (acute toxiciteit). Daarnaast kan langdurig gebruik van lithium schadelijke effecten hebben op meerdere orgaansystemen (chronische toxiciteit), waaronder de schildklier, bijschildklieren en nieren.5
Met name de renale bijwerkingen op de lange termijn roepen vragen op over het juiste beleid bij een onderhoudsbehandeling met lithium, zeker als er al nierschade bestaat. Sinds het verschijnen van een meta-analyse in 2012,5 en de nefrologische richtlijn in 2013,6 zijn meerdere epidemiologische studies verschenen over dit onderwerp.
In dit artikel geven wij een overzicht van de huidige kennis van renale bijwerkingen van chronisch lithiumgebruik en doen wij aanbevelingen voor de klinische praktijk en voor vervolgonderzoek.
Zoekstrategie
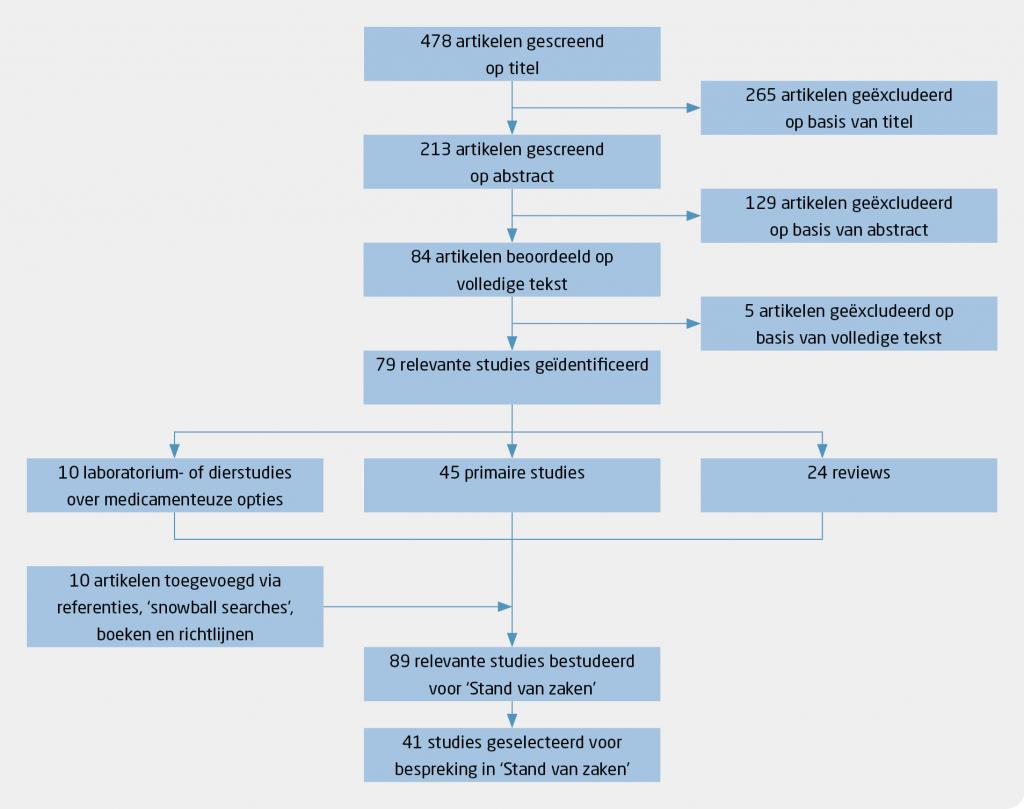
Wij verrichtten een systematisch literatuuronderzoek in PubMed naar artikelen met de kernwoorden ‘lithium’ en ‘kidney’ die gepubliceerd waren na 1 januari 2010. Dit resulteerde in 478 artikelen, waarvan 79 relevant bleken (figuur 1). Daarnaast voerden we ‘snowball searches’ uit in PubMed en Google Scholar en raadpleegden we UpToDate en twee boeken. Vanwege de beperkte ruimte bespreken wij hier een selectie van de literatuur. Op basis van alle evidentie heeft ons Consortium Nefropsychiatrie aanbevelingen opgesteld.
Lithium en de nieren
De eliminatie van lithium vindt voornamelijk plaats via de nieren. Lithium heeft een smalle therapeutische breedte (0,4-1,0 mmol/l).7 De lithiumspiegel in het bloed is afhankelijk van de dosis, de lithiumklaring en het distributievolume en wordt beïnvloed door de nierfunctie, het lichaamsgewicht en de leeftijd.6
Van nature vermindert de nierfunctie bij het ouder worden. Lithium moet daarom bij oudere patiënten (> 65 jaar) lager en bij jongere (< 25 jaar) hoger gedoseerd worden om dezelfde plasmaspiegel te bereiken.8 Bij hypertensie en hartfalen is een lagere dosis lithium noodzakelijk voor de gewenste spiegel, terwijl bij obesitas doorgaans juist een hogere dosis nodig is. Ook kan bepaalde comedicatie de spiegel beïnvloeden, zoals diuretica, NSAID’s en antihypertensiva.6
Renale bijwerkingen
Nefrogene diabetes insipidus
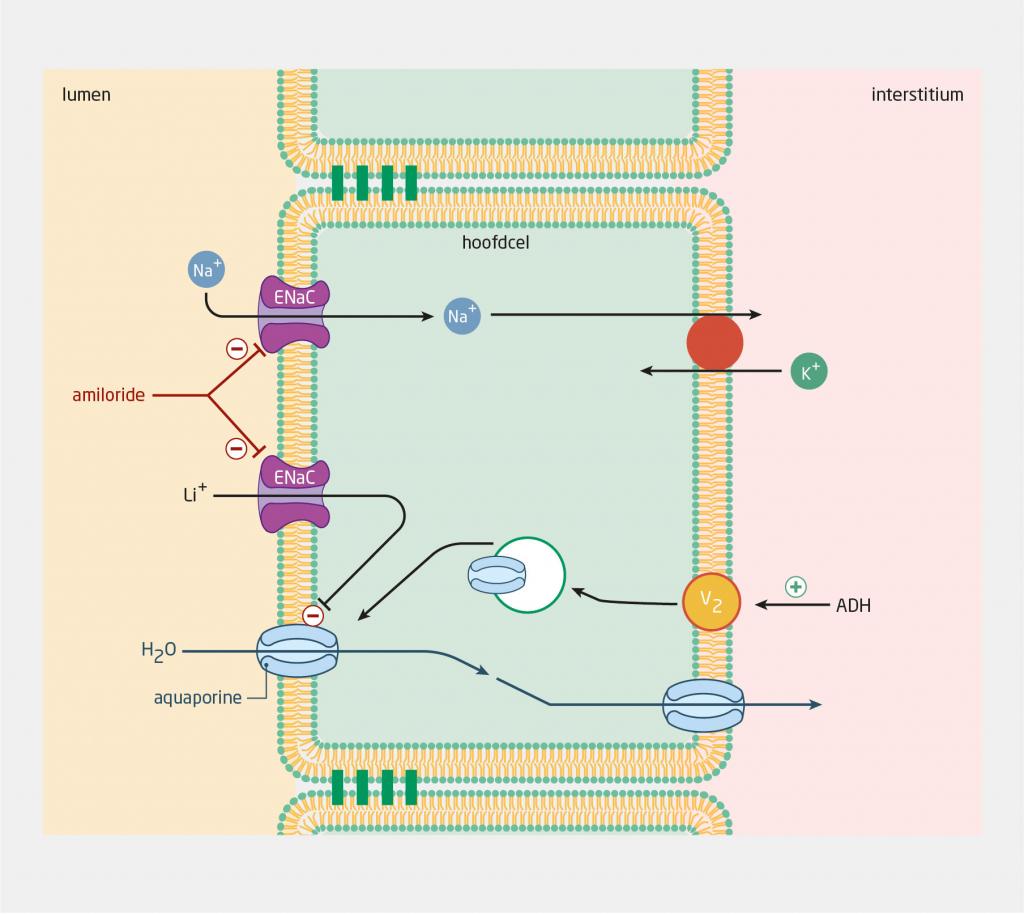
Lithium accumuleert in de hoofdcellen van de verzamelbuis van het nefron, waardoor de gevoeligheid voor antidiuretisch hormoon (ADH) afneemt en de terugresorptie van water vermindert (figuur 2).9 Hierdoor neemt het maximaal concentrerende vermogen van de nier gemiddeld met 15% af.5 Bij verdere achteruitgang van het concentrerende vermogen veroorzaakt dit polyurie, dorst en polydipsie. Polyurie kan worden aangetoond met een verzameling van 24-uursurine (> 3 l/24 h) of door de osmolaliteit van serum te vergelijken met die van ochtendurine (zie uitleg).
Uiteindelijk kan het beeld van nefrogene diabetes insipidus optreden, dat kan worden gediagnosticeerd met een dorstproef of DDAVP-test (zie uitleg). Deze onderzoeken zijn echter niet bij iedere patiënt nodig. Bovendien is een volledige dorstproef in onervaren handen niet zonder risico.6 Alternatieve oorzaken van dorst en polyurie, zoals centrale diabetes insipidus, diabetes mellitus, psychogene polydipsie en een droge mond als anticholinerge bijwerking van lithium, moeten worden uitgesloten.10
Nefrogene diabetes insipidus is de meest voorkomende bijwerking van lithiumgebruik. In een studie onder 1105 niet-geselecteerde lithiumgebruikers werd, met een dorstproef, bij 54% een verminderd concentrerend vermogen vastgesteld; bij 19% van hen was sprake van polyurie.11 Risicofactoren voor nefrogene diabetes insipidus zijn leeftijd, duur van het lithiumgebruik en hoog-therapeutische lithiumspiegels.12 De bijwerking kan vanaf enkele weken na aanvang van behandeling met lithium optreden en is geheel of gedeeltelijk reversibel als lithium gestopt wordt. Mogelijk houdt de reversibiliteit verband met de duur van het lithiumgebruik en de mate van tubulo-interstitiële fibrose op het moment van stoppen.13
Hoewel poly- en nycturie hinderlijk kunnen zijn, zijn deze klachten niet gevaarlijk zolang de patiënt een adequate dorstprikkel heeft en voldoende waterinname gegarandeerd is. Vroeger werd gedacht dat lithium-geïnduceerde diabetes insipidus een voorbode was van progressieve nierinsufficiëntie, maar het optreden van deze bijwerking blijkt slechts een zwakke voorspeller te zijn.13 Bij toegenomen vochtverlies (braken, diarree, IC-opname) daarentegen bestaat een verhoogd risico op dehydratie en hypernatriëmie en is monitoring van de plasmanatriumwaarde en de vochtbalans onontbeerlijk.6 Daarnaast moet in dergelijke omstandigheden regelmatig de lithiumspiegel worden bepaald vanwege het risico op een acute lithiumintoxicatie.
Conservatieve interventies voor nefrogene diabetes insipidus, zoals een eenmaaldaagse dosering, het streven naar een zo laag mogelijke therapeutische lithiumspiegel en een eiwit- en zoutbeperking, hebben mogelijk effect.6,14 Een enkele patiënt kan medicamenteus worden behandeld.6 Theoretisch is amiloride, een kaliumsparend diureticum, dan het middel van eerste keuze omdat dit preventief de opname van lithium in de hoofdcellen van de verzamelbuis remt (zie figuur 2).9 Dit is echter slechts in enkele studies onderzocht: in één recente studie bij ratten,15 en in één gerandomiseerde placebogecontroleerde studie bij patiënten.16
Een alternatief is een thiazidediureticum. Hierdoor vermindert het urinevolume vaak sterk, al wordt lithiumstapeling niet tegengegaan. Bij aanvang van de behandeling met een thiazidediureticum moet de lithiumdosering profylactisch met 30-50% worden verlaagd, en na 1 week moeten de calcium- en kaliumwaarde, de nierfunctie en de lithiumspiegel worden gecontroleerd.6
Chronische nierinsufficiëntie
Sinds enkele decennia wordt gedebatteerd over een mogelijk verband tussen lithiumgebruik en chronische nierinsufficiëntie.17 Twee meta-analyses, gepubliceerd in respectievelijk 2012 en 2010, toonden aan dat de nierfunctie van lithiumgebruikers slechter is dan die van controlepersonen.5,18 Beide studies konden echter geen uitspraken doen over de klinische significantie hiervan vanwege de heterogeniteit en de matige kwaliteit van de geïncludeerde studies. Bovendien waren de beschreven studies klein en gedateerd.
Sinds 2010 hebben meer dan 20 grote epidemiologische studies consequent aangetoond dat langdurig lithiumgebruik gerelateerd is aan chronische nierinsufficiëntie (voor een overzicht, zie Azab et al.,13 en Tondo et al.19 ). Zo is het risico hierop 2,7 keer zo hoog voor patiënten met een bipolaire stoornis die lithium gebruiken als voor patiënten zonder lithium.20 De prevalentie van nierinsufficiëntie (CKD-stadium ≥ 3a; zie uitleg) wordt geschat op 10-20% na 5-9 jaar lithiumgebruik, maar kan oplopen tot 50% na meer dan 25 jaar.21 Toch gaat de nierfunctie van de meeste lithiumgebruikers klinisch niet achteruit.13
Lithium kan chronische tubulo-interstitiële nefritis veroorzaken, na 10-20 jaar lithiumgebruik.6,9 Typische histologische bevindingen zijn interstitiële fibrose, tubulaire dilatatie en atrofie en in mindere mate glomerulosclerose.22 Ook kan microcystevorming optreden in de distale tubuli en verzamelbuizen, wat zowel histologisch als met radiologisch onderzoek (echo, CT, MRI) kan worden aangetoond.23 Deze pathofysiologische veranderingen leiden tot chronische nierinsufficiëntie, die meestal asymptomatisch is. Proteïnurie ontbreekt meestal of is gering van aard, en de bloeddruk en het urinesediment zijn niet-afwijkend.9 Ook is het optreden van het nefrotisch syndroom beschreven, maar dit komt zelden voor.6
Lithium-geïnduceerde nierschade is meestal langzaam progressief (‘creeping creatinine’). Bij jarenlang lithiumgebruik neemt de eGFR elk jaar met 0,92% af, vergeleken met een vermindering met 0,64% door leeftijd alleen.19 Deze afname begint 6-10 jaar na aanvang van lithiumtherapie en het duurt gemiddeld 30 jaar voordat de eGFR onder de 60 ml/min per 1,73 m2 zakt.19
Een ongewone complicatie van lithiumgebruik is terminaal nierfalen (zie uitleg). De prevalentie hiervan wordt geschat op 0,5-1,5% bij lithiumgebruik van meer dan 15 jaar.24 In een retrospectieve studie waarin 630 lithiumgebruikers werden geëvalueerd in de periode 1981-2010, had 0,9% van de mannen en 0,3% van de vrouwen een eGFR < 15 ml/min per 1,73 m2 nadat ze gedurende 10 jaar of meer lithium hadden gebruikt.25 Hierbij was het echter niet duidelijk of lithium de enige oorzaak was van het nierfalen. Een recente nationale studie onder 1,5 miljoen Denen toonde wel een verband aan tussen lithiumgebruik en nierinsufficiëntie, maar niet met eindstadiumnierfalen.26
De belangrijkste risicofactoren voor chronische nierinsufficiëntie zijn leeftijd en duur van het lithiumgebruik.13,24 Comorbiditeit, zoals hypertensie en diabetes mellitus, speelt ook een rol, evenals comedicatie.26 Negatieve invloed komt mogelijk ook van een dosering van meerdere keren per dag,14 en individuele genetische vatbaarheid.27 Daarnaast is het effect van lithium op de nierfunctie mogelijk dosisafhankelijk. Meerdere studies hebben een verband tussen de hoogte van de lithiumspiegel en nierschade aangetoond.19,28 Een grote cohortstudie liet zelfs zien dat een enkele overschrijding van de lithiumspiegel > 1,0 mmol/l gepaard gaat met een significante daling van de eGFR 3 maanden later.28 Het is nog niet duidelijk of de nierfunctie hierna kan herstellen.
Er is op dit moment geen behandeling voor lithium-geïnduceerde nierinsufficiëntie. Bij ratten die door lithiumgebruik interstitiële fibrose hadden ontwikkeld, kon additie van amiloride aan de voortgezette lithiumtoediening wel de progressie van fibrosering remmen, maar de nierfunctie verbeterde hierdoor niet.29 Voor preventieve behandeling met amiloride is op dit moment, door het ontbreken van resultaten uit klinisch onderzoek, geen plaats.
Het is onduidelijk of er voordelen zijn van het staken van lithium bij patiënten met chronische nierinsufficiëntie. Enkele studies toonden aan dat de eGFR verder blijft dalen ondanks het stoppen met lithium,21,30 terwijl een andere studie liet zien dat stoppen verdere eGFR-daling mogelijk wél voorkomt.31 Als de eGFR onder een bepaalde grens zakt (25-40 ml/min per 1,73 m2), zou de nierinsufficiëntie irreversibel zijn.32
Zweedse onderzoekers hebben een mathematisch model gecreëerd waarin ze berekenden of het zinvol was met lithium te stoppen bij patiënten die 20 jaar lithium hadden gebruikt.33 Als uitkomst bekeken ze het suïciderisico, het risico op een instabiele bipolaire stoornis en het risico op nierfalen na 30 jaar lithiumgebruik. Voor de meeste patiënten leverde het meer voordelen op lithium te continueren dan te stoppen.33 Een recente cohortstudie liet zelfs zien dat als lithium gecontinueerd wordt nadat chronische nierinsufficiëntie is vastgesteld, het risico op nierfalen niet toeneemt.34 Als patiënten overgaan op een anti-epilepticum, verandert dit het risico op nierfalen niet.
Implicaties
Klinische praktijk
Uit de beschikbare evidentie blijkt dat de prevalentie van een ernstige lithium-geïnduceerde nierfunctiestoornis zeldzaam is (tabel 1). Toch is het van belang nierschade zo veel mogelijk te voorkomen en te monitoren en de patiënt bijtijds te verwijzen naar de nefroloog.

In tabel 2 staan aanbevelingen op basis van de beschikbare literatuur. Een belangrijk advies is te streven naar een zo laag mogelijke therapeutische lithiumspiegel als onderhoudsbehandeling (0,6-0,8 mmol/l, bij ouderen 0,4-0,8 mmol/l), omdat het negatieve effect van lithium op de nieren mogelijk spiegelafhankelijk is. De ‘Lithiumeter’ is hierbij een handig hulpmiddel (figuur 3).7
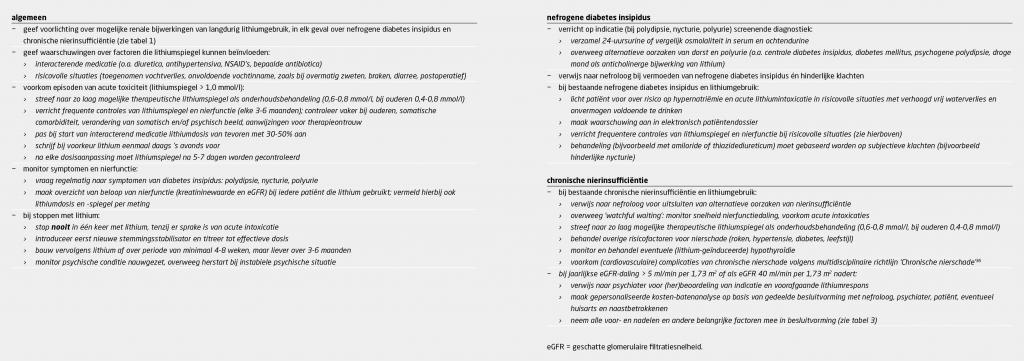
Daarnaast is het essentieel om de nierfunctie en de lithiumspiegel minstens elke 3-6 maanden te controleren, of vaker bij verandering van het somatische of psychische beeld of bij aanwijzingen voor therapieontrouw. Deze frequente controles zijn noodzakelijk om het risico op acute toxiciteit – en dus op een eGFR-daling – te verkleinen. Bovendien kan met frequente controle de snelheid van de nierfunctiedaling worden gemonitord en kan worden voorkomen dat de lithiumspiegel onder de therapeutische ondergrens van 0,4 mmol/l zakt.
Stoppen of doorgaan bij nierschade?
De huidige richtlijn ‘Bipolaire stoornissen’ beveelt aan lithium te staken als de eGFR 40 ml/min per 1,73 m2 nadert,1 of als er sprake is van een snel progressieve daling van de nierfunctie (jaarlijks verlies: > 5 ml/min per 1,73 m2).1 Uit bovenstaande bespreking van de literatuur blijkt echter dat het niet zeker is of het staken van lithium verdere progressie van de nierschade kan voorkomen. Daarentegen is het wél zeker dat het stoppen met lithium gerelateerd is aan een hoog risico op een nieuwe stemmingsepisode,37 of op suïcide.38 Bovendien hebben alternatieve stemmingsstabilisatoren, zoals valproïnezuur, quetiapine, olanzapine en lamotrigine,1 mogelijk minder nefrotoxische, maar wel andere duidelijke bijwerkingen, bijvoorbeeld het optreden van een metabool syndroom bij gebruik van antipsychotica.39 Bij renale bijwerkingen moet de beslissing om lithiumtherapie te staken daarom nooit overhaast worden genomen.
Omdat er grote individuele verschillen bestaan tussen patiënten met bipolaire stoornis in de respons op lithium en op andere stemmingsstabilisatoren, is het niet mogelijk een eenduidig antwoord te geven op de vraag of lithium gecontinueerd of gestopt moet worden bij nierschade. Wij raden daarom aan per patiënt een inschatting te maken van de voor- en nadelen van stoppen met lithium. Een dergelijk dilemma leent zich goed voor gedeelde besluitvorming (tabel 3). Hierin zouden alle betrokkenen (nefroloog, psychiater, patiënt) een stem moeten hebben.
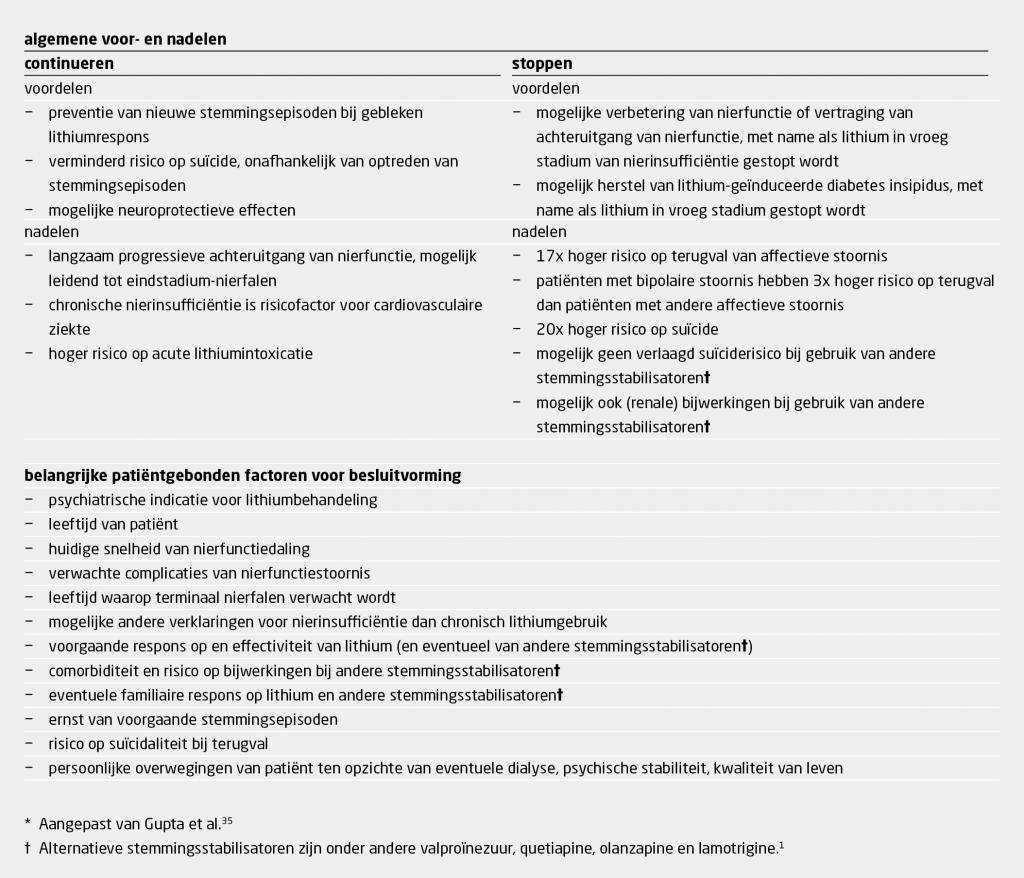
De nefroloog kan alternatieve oorzaken uitsluiten en voorlichting geven over toekomstscenario’s bij het continueren of stoppen met lithium en over mogelijke complicaties van een nierfunctiestoornis. De psychiater kan het suïcide- en het terugvalrisico bij staken van lithium bespreken, naast mogelijke alternatieven voor lithium. Daarnaast is het van belang om meerdere patiëntgebonden factoren mee te wegen bij deze beslissing, waaronder de snelheid van de nierfunctiedaling, de ernst van voorgaande stemmingsepisoden en de leeftijd van patiënt (zie tabel 3).
Ten slotte spelen de persoonlijke overwegingen van de patiënt een grote rol. Waar de ene patiënt per se een stabiele psychische toestand verkiest boven een risico op nierfalen, wil de andere wellicht koste wat kost de noodzaak tot nierfunctievervangende behandeling voorkomen. Op basis van dergelijke gedeelde besluitvorming kan bij sommige patiënten, ondanks renale complicaties, voortzetting van de lithiumbehandeling een keuze zijn.
Toekomstig onderzoek
Het is op dit moment niet goed te voorspellen welke patiënten die lithium gebruiken op de langere termijn renale bijwerkingen zullen krijgen. Bovendien is het methodologisch lastig het onafhankelijke effect van lithium te analyseren.40 Potentiële determinanten zijn het individuele bipolaire ziekteprofiel, de familiaire belasting of genetische factoren. Er is een prospectieve cohortstudie nodig die patiënten met een bipolaire stoornis en lithiumgebruik vergelijkt met lithium-naïeve patiënten met een bipolaire stoornis en met gezonde controlepersonen. Bovendien is meer onderzoek nodig naar het effect van al dan niet medicamenteuze interventies op het beloop van de nierfunctie, zoals een lagere dosis lithium,41 amiloride of thiazidediuretica.
Literatuur
Multidisciplinaire richtlijn Bipolaire stoornissen (derde revisie). Utrecht: De Tijdstroom; 2015.
Multidisciplinaire richtlijn Depressie (derde revisie). Utrecht: Trimbos-instituut; 2013.
Ostacher MJ, Nierenberg AA, Iosifescu DV, et al; STEP-BD Family Experience Collaborative Study Group. Correlates of subjective and objective burden among caregivers of patients with bipolar disorder. Acta Psychiatr Scand. 2008;118:49-56. Medlinedoi:10.1111/j.1600-0447.2008.01201.x
Zivanovic O. Lithium: A classic drug-Frequently discussed, but, sadly, seldom prescribed! Aust N Z J Psychiatry. 2017;51:886-96. Medlinedoi:10.1177/0004867417695889
McKnight RF, Adida M, Budge K, Stockton S, Goodwin GM, Geddes JR. Lithium toxicity profile: a systematic review and meta-analysis. Lancet. 2012;379:721-8. Medlinedoi:10.1016/S0140-6736(11)61516-X
Richtlijn Renale bijwerkingen van chronisch lithiumgebruik. Utrecht: Nederlandse Federatie voor Nefrologie; 2013.
Malhi GS, Gershon S, Outhred T. Lithiumeter: Version 2.0. Bipolar Disord. 2016;18:631-41. Medlinedoi:10.1111/bdi.12455
Rej S, Beaulieu S, Segal M, et al. Lithium dosing and serum concentrations across the age spectrum: from early adulthood to the tenth decade of life. Drugs Aging. 2014;31:911-6. Medlinedoi:10.1007/s40266-014-0221-1
Grünfeld JP, Rossier BC. Lithium nephrotoxicity revisited. Nat Rev Nephrol. 2009;5:270-6. Medlinedoi:10.1038/nrneph.2009.43
Dols A, Sienaert P, van Gerven H, et al. The prevalence and management of side effects of lithium and anticonvulsants as mood stabilizers in bipolar disorder from a clinical perspective: a review. Int Clin Psychopharmacol. 2013;28:287-96. Medlinedoi:10.1097/YIC.0b013e32836435e2
Boton R, Gaviria M, Batlle DC. Prevalence, pathogenesis, and treatment of renal dysfunction associated with chronic lithium therapy. Am J Kidney Dis. 1987;10:329-45. Medlinedoi:10.1016/S0272-6386(87)80098-7
Rej S, Segal M, Low NCP, et al. The McGill Geriatric Lithium-Induced Diabetes Insipidus Clinical Study (McGLIDICS). Can J Psychiatry. 2014;59:327-34. Medlinedoi:10.1177/070674371405900606
Azab AN, Shnaider A, Osher Y, Wang D, Bersudsky Y, Belmaker RH. Lithium nephrotoxicity. Int J Bipolar Disord. 2015;3:28. Medlinedoi:10.1186/s40345-015-0028-y
Carter L, Zolezzi M, Lewczyk A. An updated review of the optimal lithium dosage regimen for renal protection. Can J Psychiatry. 2013;58:595-600. Medlinedoi:10.1177/070674371305801009
Kortenoeven ML, Li Y, Shaw S, et al. Amiloride blocks lithium entry through the sodium channel thereby attenuating the resultant nephrogenic diabetes insipidus. Kidney Int. 2009;76:44-53. Medlinedoi:10.1038/ki.2009.91
Bedford JJ, Weggery S, Ellis G, et al. Lithium-induced nephrogenic diabetes insipidus: renal effects of amiloride. Clin J Am Soc Nephrol. 2008;3:1324-31. Medlinedoi:10.2215/CJN.01640408
Gupta S, Khastgir U. Drug information update. Lithium and chronic kidney disease: debates and dilemmas. BJPsych Bull. 2017;41:216-20. Medlinedoi:10.1192/pb.bp.116.054031
Paul R, Minay J, Cardwell C, Fogarty D, Kelly C. Meta-analysis of the effects of lithium usage on serum creatinine levels. J Psychopharmacol. 2010;24:1425-31. Medlinedoi:10.1177/0269881109104930
Tondo L, Abramowicz M, Alda M, et al. Long-term lithium treatment in bipolar disorder: effects on glomerular filtration rate and other metabolic parameters. Int J Bipolar Disord. 2017;5:27. Medlinedoi:10.1186/s40345-017-0096-2
Close H, Reilly J, Mason JM, et al. Renal failure in lithium-treated bipolar disorder: a retrospective cohort study. PLOS ONE. 2014;9:e90169. Medlinedoi:10.1371/journal.pone.0090169
Bocchetta A, Ardau R, Fanni T, et al. Renal function during long-term lithium treatment: a cross-sectional and longitudinal study. BMC Med. 2015;13:12. Medlinedoi:10.1186/s12916-014-0249-4
Markowitz GS, Radhakrishnan J, Kambham N, Valeri AM, Hines WH, D’Agati VD. Lithium nephrotoxicity: a progressive combined glomerular and tubulointerstitial nephropathy. J Am Soc Nephrol. 2000;11:1439-48 Medline.
Karaosmanoglu AD, Butros SR, Arellano R. Imaging findings of renal toxicity in patients on chronic lithium therapy. Diagn Interv Radiol. 2013;19:299-303 Medline.
Gitlin M. Lithium side effects and toxicity: prevalence and management strategies. Int J Bipolar Disord. 2016;4:27. Medlinedoi:10.1186/s40345-016-0068-y
Aiff H, Attman P-O, Aurell M, et al. Effects of 10 to 30 years of lithium treatment on kidney function. J Psychopharmacol. 2015;29:608-14. Medlinedoi:10.1177/0269881115573808
Kessing LV, Gerds TA, Feldt-Rasmussen B, Andersen PK, Licht RW. Use of lithium and anticonvulsants and the rate of chronic kidney disease: a nationwide population-based study. JAMA Psychiatry. 2015;72:1182-91. Medlinedoi:10.1001/jamapsychiatry.2015.1834
Tsermpini EE, Zhang Y, Niola P, et al. Pharmacogenetics of lithium effects on glomerular function in bipolar disorder patients under chronic lithium treatment: a pilot study. Neurosci Lett. 2017;638:1-4. Medlinedoi:10.1016/j.neulet.2016.12.001
Kirkham E, Skinner J, Anderson T, Bazire S, Twigg MJ, Desborough JA. One lithium level >1.0 mmol/L causes an acute decline in eGFR: findings from a retrospective analysis of a monitoring database. BMJ Open. 2014;4:e006020. Medlinedoi:10.1136/bmjopen-2014-006020
Kalita-De Croft P, Bedford JJ, Leader JP, Walker RJ. Amiloride modifies the progression of lithium-induced renal interstitial fibrosis. Nephrology (Carlton). 2018;23:20-30. Medlinedoi:10.1111/nep.12929
Bendz H, Schön S, Attman P-O, Aurell M. Renal failure occurs in chronic lithium treatment but is uncommon. Kidney Int. 2010;77:219-24. Medlinedoi:10.1038/ki.2009.433
Rej S, Abitbol R, Looper K, Segal M. Chronic renal failure in lithium-using geriatric patients: effects of lithium continuation versus discontinuationa 60-month retrospective study. Int J Geriatr Psychiatry. 2013;28:450-3. Medlinedoi:10.1002/gps.3841
Presne C, Fakhouri F, Noël LH, et al. Lithium-induced nephropathy: Rate of progression and prognostic factors. Kidney Int. 2003;64:585-92. Medlinedoi:10.1046/j.1523-1755.2003.00096.x
Werneke U, Ott M, Renberg ES, Taylor D, Stegmayr B. A decision analysis of long-term lithium treatment and the risk of renal failure. Acta Psychiatr Scand. 2012;126:186-97. Medlinedoi:10.1111/j.1600-0447.2012.01847.x
Kessing LV, Feldt-Rasmussen B, Andersen PK, Gerds TA, Licht RW. Continuation of lithium after a diagnosis of chronic kidney disease. Acta Psychiatr Scand. 2017;136:615-22. Medlinedoi:10.1111/acps.12820
Gupta S, Kripalani M, Khastgir U, Reilly J. Management of the renal adverse effects of lithium. Adv Psychiatr Treat. 2013;19:457-66.
Multidisciplinaire richtlijn Chronische nierschade. Utrecht: Nederlandse Internisten Vereniging en Nederlands Huisartsen Genootschap; 2018.
Biel MG, Peselow E, Mulcare L, Case BG, Fieve R. Continuation versus discontinuation of lithium in recurrent bipolar illness: a naturalistic study. Bipolar Disord. 2007;9:435-42. Medlinedoi:10.1111/j.1399-5618.2007.00389.x
Baldessarini RJ, Tondo L, Hennen J. Effects of lithium treatment and its discontinuation on suicidal behavior in bipolar manic-depressive disorders. J Clin Psychiatry. 1999;60(Suppl 2):77-84, discussion 111-6 Medline.
Hayes JF, Marston L, Walters K, Geddes JR, King M, Osborn DP. Adverse renal, endocrine, hepatic, and metabolic events during maintenance mood stabilizer treatment for bipolar disorder: a population-based cohort study. PLOS Med. 2016;13:e1002058. Medlinedoi:10.1371/journal.pmed.1002058
Nielsen RE, Kessing LV, Nolen WA, Licht RW. Lithium and renal impairment: a review on a still hot topic. Pharmacopsychiatry. 18 januari 2018 (epub). Medline
Gong R, Wang P, Dworkin L. What we need to know about the effect of lithium on the kidney. Am J Physiol Renal Physiol. 2016;311:F1168-71. Medlinedoi:10.1152/ajprenal.00145.2016





opmerkelijke naamskeuze: 'Consortium Nefropsychiatrie'
Als terminoloog kijk ik op van de naamskeuze 'Consortium Nefropsychiatrie'. De term 'nefropsychiatrie' is net zomin als 'psychonefrologie' online in ons taalgebied te vinden en levert in zijn Engelse vorm, 'nephropsychiatry', wereldwijd slechts 17 hits met weinig gezag op. Heeft deze term, verwarbaar met 'neuropsychiatrie', voldoende bestaansrecht?
Anoud van den Eerenbeemt, medisch terminoloog