Samenvatting
Doel
Het beloop bij ziekenhuispatiënten met bewezen covid-19 in Nederland in kaart brengen.
Opzet
Retrospectief cohortonderzoek.
Methode
Gegevens van 2579 patiënten met covid-19 die opgenomen waren in 10 Nederlandse centra in de periode februari-juli 2020 worden beschreven. De klinische gegevens zijn gebaseerd op het WHO-COVID-‘case record form’, aangevuld met patiëntkenmerken waarvan recentelijk een verband met de ernst van de ziekte is beschreven. De primaire statistische analyse bestond uit overlevingsanalyses met Kaplan-Meier-curves voor overlijden binnen 3 weken na opname, berekend voor premorbide factoren en klinische, radiologische en laboratoriumgegevens bij opname in het ziekenhuis.
Resultaten
De totale sterfte in het ziekenhuis na 3 weken bedroeg 22,2% (95%-BI: 20,7-23,9). De ziekenhuissterfte binnen 21 dagen was statistisch significant hoger voor patiënten ouder dan 70 jaar (35,0%; 95%-BI: 32,4-37,8) en voor patiënten die gedurende de 21 dagen ook op de IC opgenomen waren geweest (36,5%; 95%-BI: 32,1-41,3). Los daarvan zien we in deze Nederlandse populatie ook een toegenomen risico op overlijden bij patiënten met comorbiditeit – bijvoorbeeld een chronische neurologische, nefrologische of cardiale aandoening of hypertensie – en bij patiënten met meer thuismedicatie en of met een verhoogde ureum- en creatininewaarde.
Conclusie
Sterfte binnen 21 na ziekenhuisopname ten gevolge van covid-19 in Nederland lijkt verband te houden met demografische variabelen (bijvoorbeeld leeftijd) en comorbiditeit (bijvoorbeeld hart- en vaatziekten), maar ook ziektekenmerken bij opname.
artikel
Inleiding
Nederland telt sinds het begin van de covid-19-uitbraak op 27 februari 2020 meer dan 13.852 ziekenhuisopnames, waarvan circa 3830 opnames op de Intensive Care (IC, peildatum 18 oktober 2020). Inzicht in het beloop van patiënten met covid-19 is van belang om de kwaliteit en organisatie van zorg voor nieuwe patiënten met covid-19 te verbeteren. Buitenlandse cohorten en internationale studies zijn hiervoor onvoldoende informatief,1-6 omdat Nederland een specifieke samenstelling van de bevolking, zorgorganisatie en zorgcultuur kent.
De beschrijving van de eerste 100 patiënten in het Elisabeth-Tweesteden Ziekenhuis geeft een inzicht in de Nederlandse situatie.7 Om een zo goed mogelijk beeld te krijgen over het beloop bij patiënten in de eerste covid-19-golf in Nederland is het echter essentieel om een groter aantal patiënten systematisch in kaart te brengen. Daarbij is het vooral belangrijk onderscheid te maken tussen een relatief mild beloop en een ernstig beloop, omdat dit kan helpen bij het nemen van beslissingen over de behandeling van individuele patiënten. Daarnaast kan deze informatie beleidsmakers ondersteunen.
In dit artikel presenteren wij gegevens van de eerste 2607 Nederlandse covid-19-patiënten die geïncludeerd zijn in de COVID-PREDICT-studie. In de analyse onderzoeken wij welke patiëntkenmerken bij ziekenhuisopname verband houden met overlijden.
Methode
Na goedkeuring van de medisch-ethische commissies werden retrospectief patiëntgegevens verzameld in meerdere Nederlandse perifere en academische ziekenhuizen (actueel overzicht op www.covidpredict.nl). De inclusiecriteria zijn (a) een leeftijd van 18 jaar of ouder en (b) een positieve SARS-CoV-2-PCR-test en/of een CO-RADS-score ≥ 4 op een CT-scan van de thorax. Van deze patiënten werden gegevens verzameld op basis van het WHO-COVID-‘case record form’ (CRF, versie februari 2020), aangevuld met patiëntkenmerken waarvan recentelijk een verband met de ernst van de ziekte is beschreven.3,4,6 Voor dit artikel hebben wij de mortaliteitscijfers tot 21 dagen na opname in het ziekenhuis gebruikt. Voor de analyses gebruikten wij de gegevens die tot en met 31 juli 2020 waren verzameld.
Als primaire statistische analyse voerden wij overlevingsanalyses uit met Kaplan-Meier-curves voor overlijden binnen een periode van 21 dagen na opname, berekend voor kenmerken van de patiënt voordat deze ziek werd (‘premorbide factoren’) en voor klinische, radiologische en laboratoriumgegevens bij opname in het ziekenhuis. Hierbij werden patiënten die nog opgenomen waren in het ziekenhuis maar het gekozen eindpunt (dag 21) nog niet bereikt hadden, gecensureerd vanaf de dag van de laatste follow-up (n = 205). Verder namen we aan dat patiënten die binnen 3 weken na opname ontslagen en niet heropgenomen waren, 21 dagen na de opnamedatum nog in leven waren.8 Daarom werd de tijd tot overlijden voor ontslagen patiënten in de Kaplan-Meier-analyse gesteld op 22 dagen. Patiënten van wie de uitkomst onbekend was, werden gecensureerd op de laatste dag (n = 177). Patiënten van wie geen follow-upgegevens of opnamedatum beschikbaar waren (n = 28), werden niet meegenomen in de Kaplan-Meier-analyses.
Voor de Kaplan-Meier-analyses werden binaire en categorische variabelen opgesplitst in 2 of meer categorieën; numerieke variabelen werden opgesplitst in tertielen of – op basis van referentiewaarden – in afwijkend en niet-afwijkend. De overlevingskansen werden vergeleken met de log-rank-toets en voor de verschillen in overlevingskansen werden Bonferroni-gecorrigeerde p-waarden berekend. Tevens werd voor elke variabele bepaald of de Kaplan-Meier-curve van patiënten met ontbrekende waarden – na Bonferroni-correctie – statistisch significant verschilde van de Kaplan-Meier-curve van patiënten zonder ontbrekende waarden. In het supplement bij dit artikel staan de klinisch relevante premorbide factoren, klinische parameters en laboratoriumwaarden bij opname (data-extractie op 1 augustus 2020).
Resultaten en beschouwing
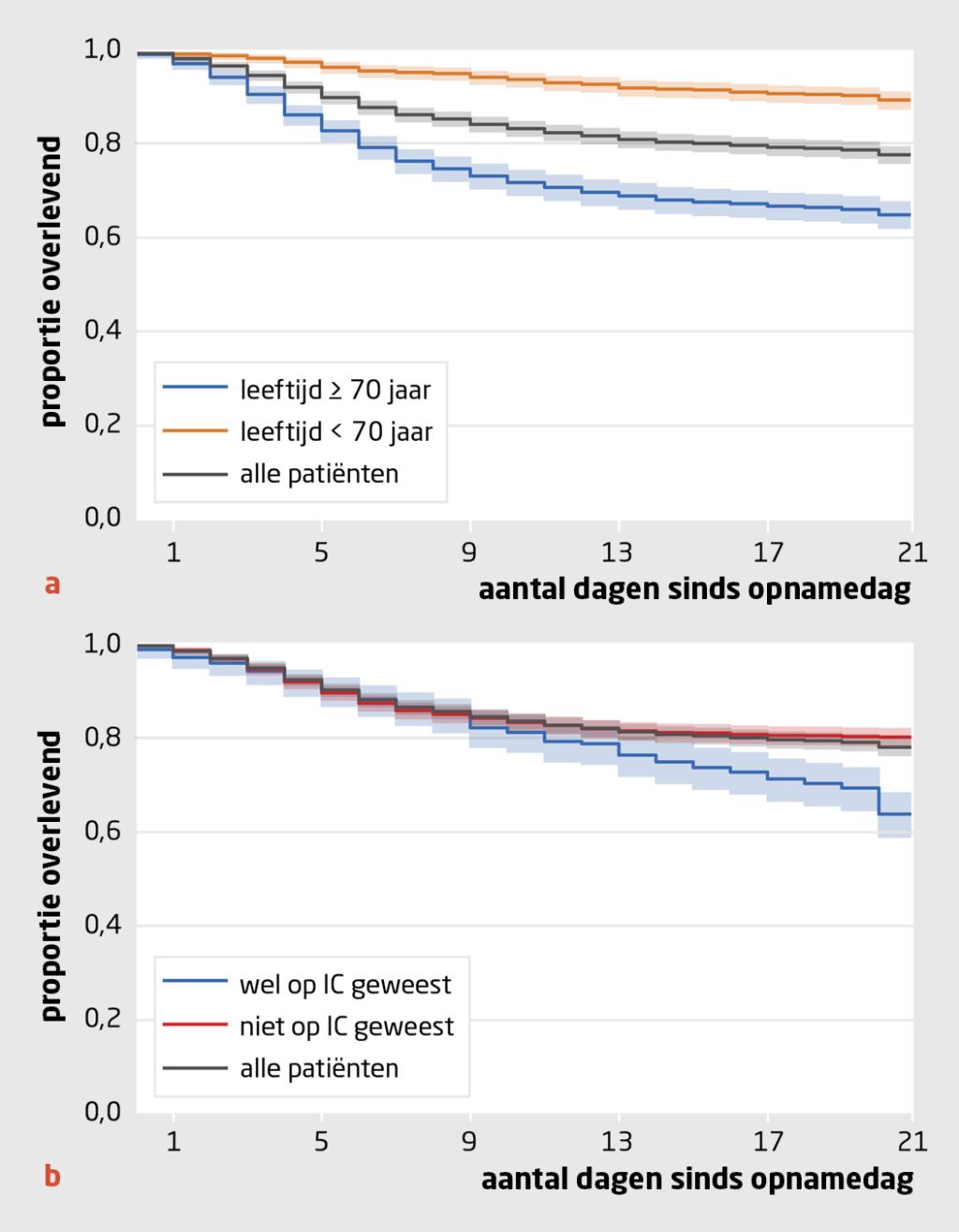
Van in totaal 2579 patiënten met covid-19 die in de periode februari-juli 2020 waren opgenomen in 10 Nederlandse centra konden wij de klinische gegevens gebruiken voor de analyse (zie het supplement bij dit artikel). De sterfte onder covid-19-patiënten binnen 21 dagen na opname in het ziekenhuis bedroeg 22,2% (95%-BI: 20,7-23,9). De ziekenhuissterfte binnen 21 dagen was statistisch significant hoger voor patiënten ouder dan 70 jaar (35,0%; 95%-BI: 32,4-37,8) en voor patiënten die gedurende die 21 dagen ook op de IC opgenomen waren geweest (36,5%; 95%-BI: 32,1- 41,3).
Los daarvan zagen we in deze Nederlandse populatie ook een toegenomen risico op overlijden binnen 21 dagen bij patiënten met comorbiditeit – zoals een chronische neurologische, nefrologische of cardiale aandoening of hypertensie –, patiënten met meer thuismedicatie en patiënten met bepaalde afwijkende bloedwaarden, zoals een verhoogde ureum- of creatinineconcentratie. Dit resultaat is minder betrouwbaar voor de ureum- en creatinineconcentratie, omdat patiënten van wie deze waarden niet bekend waren, een statistisch significant hoger risico op overlijden hadden. Een totaaloverzicht van de Kaplan-Meier curves is te vinden in Dropbox via de volgende link: www.dropbox.com/sh/x34jj4ncwi1i0tf/AAA8Do-NHCzpVS0Cx0GJAiLka?dl=1.
Ter illustratie laten we de Kaplan-Meier-curves zien van patiënten ouder en jonger dan 70 (figuur a) en patiënten die al dan niet op de IC waren opgenomen (figuur b).
Kanttekeningen bij dit onderzoek
Een kanttekening bij onze Kaplan-Meier-modellen is dat het aantal overledenen klein is ten opzichte van het aantal patiënten dat in leven is gebleven. Een tweede kanttekening is dat 142 patiënten werden overgeplaatst naar een ander ziekenhuis, waaronder mogelijk centra die ook aan het COVID-PREDICT-cohort bijdroegen; sommige patiënten kunnen daardoor twee maal zijn geïncludeerd. Door pseudonimisatie van patiëntengegevens konden wij hier niet voor corrigeren.
De beschrijving van een patiëntencohort met klinische uitkomsten op een korte termijn (in ons geval een periode van 21 dagen) kent belangrijke klinische beperkingen. Ontslag binnen 21 dagen uit het ziekenhuis wil niet zeggen dat de patiënt adequaat hersteld is; sommige patiënten zullen na de ziekenhuisopname alsnog overleden zijn, mogelijk binnen 21 dagen na de opnamedatum. Tevens zijn niet van elke patiënt alle variabelen bekend of ingevoerd in de database. Voorbeeld hiervan zijn de klinische kwetsbaarheid (‘clinical frailty score’) en bepaalde stollings- en inflammatiewaarden. Een langere follow-upduur zal nodig zijn om de factoren te identificeren die verband houden met een gunstig herstel.
Voor het Kaplan-Meier-model voor de op de IC opgenomen patiënten geldt de zogenoemde ‘immortal time bias’. Dit wil zeggen dat patiënten in de IC-groep per definitie nog in leven zijn wanneer zij op de IC worden opgenomen, waardoor de niet-IC-groep zowel patiënten met een slechtere overleving als een betere overleving omvat. Desalniettemin laat deze analyse met kortetermijnuitkomsten al een hoge ziekenhuismortaliteit zien (22%). Voor deze aanhoudende pandemie zijn predictiemodellen in ontwikkeling voor individuele prognostiek, capaciteitsberekeningen en ziekenhuis- dan wel IC-triage. Deze modellen moeten waarschijnlijk een combinatie bevatten van demografische variabelen (bijvoorbeeld leeftijd), comorbiditeit (bijvoorbeeld hart- en vaatziekten) en variabelen waarmee bij opname de ziekte-ernst geschat kan worden, zoals aanwijzingen voor multi-orgaanbetrokkenheid.9
Oproep
De gegevens die wij hier presenteren zijn het resultaat van een samenwerking tussen Nederlandse ziekenhuizen waarbij belangrijke informatie over de presentatie en het beloop van covid-19 in Nederlandse ziekenhuizen is verzameld. Omdat er momenteel nog geen landelijke covid-19-database met klinische gegevens bestaat, nodigen wij ziekenhuizen die nog niet bij de COVID-PREDICT-werkgroep aangesloten zijn, uit om alsnog deel te nemen.
Literatuur
Guan WJ, Ni ZY, H Y, et al. Clinical characteristics of coronavirus disease 2019 in China. N Engl J Med. 2020;382:1708-20. Medline
Wang T, Du Z, Zhu F, et al. Comorbidities and multi-organ injuries in the treatment of COVID-19. Lancet. 2020;395:e52. doi:10.1016/S0140-6736(20)30558-4. Medline
Ruan Q, Yang K, Wang W, Jiang L, Song J. Clinical predictors of mortality due to COVID-19 based on an analysis of data of 150 patients from Wuhan, China. Intensive Care Med. 2020;46:846-8. doi:10.1007/s00134-020-05991-x. Medline
Zhou F, Yu T, Du R, et al. Clinical course and risk factors for mortality of adult inpatients with COVID-19 in Wuhan, China: a retrospective cohort study. Lancet. 2020;395:1054-62. doi:10.1016/S0140-6736(20)30566-3. Medline
Richardson S, Hirsch JS, Narasimhan M, et al; the Northwell COVID-19 Research Consortium. Presenting Characteristics, Comorbidities, and Outcomes Among 5700 Patients Hospitalized With COVID-19 in the New York City Area. JAMA. 2020;323:2052-9. doi:10.1001/jama.2020.6775. Medline
Ji D, Zhang D, Xu J, et al. Prediction for Progression Risk in Patients With COVID-19 Pneumonia: The CALL Score. Clin Infect Dis. 2020;71:1393-9. doi:10.1093/cid/ciaa414. Medline
Murk JL, van de Biggelaar R, Stohr J, et al. De eerste honderd opgenomen COVID-19-patiënten in het Elisabeth-Tweesteden Ziekenhuis. Ned Tijdschr Geneeskd. 2020;164:D5002 Medline.
Houwelingen van JJ. De statistiek van overlevingscurven. Ned Tijdschr Geneeskd. 1991;135:1735-44.
Knight SR, Ho A, Pius R, et al; ISARIC4C investigators. Risk stratification of patients admitted to hospital with covid-19 using the ISARIC WHO Clinical Characterisation Protocol: development and validation of the 4C Mortality Score. BMJ. 2020;370:m3339. doi:10.1136/bmj.m3339. Medline






Reacties