Dit leerartikel is herzien. De herziene versie (D6922) is gecontroleerd op actualiteit en juistheid. Bij de herziene versie is een nieuwe nascholingstoets beschikbaar.
Op de hoogte blijven van nieuwe leerartikelen, compleet met geaccrediteerde toetsvragen en luisterversie?
⚡Schrijf je gratis in op een e-mail alert door het dossier Leerartikelen te volgen.⚡
Dyspneu is een belangrijke en veelvoorkomende klacht van patiënten met een long- of hartziekte. Het is een vitaal signaal dat we allemaal kunnen voelen tijdens zware lichamelijke inspanning; het kan ook een uiting zijn van diverse aandoeningen. In dit leerartikel beantwoorden we 10 vragen over dyspneu die gesteld zijn door huisartsen, chirurgen en internisten. We gaan in op oorzaken van dyspneu, stellen een systematische strategie voor ten behoeve van de analyse in de kliniek en gaan in op de onderdelen van de anamnese, het lichamelijk onderzoek en het aanvullende onderzoek die het relevantste zijn voor de differentiaaldiagnose en waarmee je zo effectief mogelijk tot de juiste diagnose kunt komen.
Toets voor nascholing (verlopen)
Aan dit leerartikel was een toets gekoppeld waarmee je nascholingspunten kon verdienen.
Leerdoelen
- Inzicht krijgen in de verschillende soorten dyspneu, omdat het behulpzaam is in de zoektocht naar de oorzaak en adequate therapie als je hierin onderscheid kunt maken.
- Aanleren van een strategie in klinisch redeneren rond dyspneu, met aandacht voor onderscheidende aanwijzingen in anamnese, lichamelijk en aanvullend onderzoek.
- Overzicht krijgen van de verschillende behandelopties bij dyspneu, met als speciale notie de multidisciplinaire aanpak bij chronische problematiek.
artikel
Bij veel patiënten met een hart- of longziekte is dyspneu een van de belangrijkste klachten. Daarnaast kan dyspneu een uiting zijn van uiteenlopende ziekten en omstandigheden, zoals bloedarmoede, shock, obesitas, neuromusculaire ziekte of angst. Het is een nuttig vitaal signaal dat ook bij gezonde mensen voorkomt, bijvoorbeeld tijdens zware inspanning of bij zwemmen onder water.
Ook bij patiënten is dyspneu doorgaans een nuttig signaal, onder meer omdat het aanleiding geeft om medische hulp te zoeken wanneer de zuurstofvoorziening van het lichaam in gevaar komt. Bij een onbehandelbare oorzaak van dyspneu kunnen we ons richten op een symptomatische behandeling. Omdat dyspneu vele oorzaken kan hebben, streven we in dit artikel niet naar volledigheid, maar naar een systematische aanpak die in verschillende situaties toepasbaar is.
Wat is dyspneu?
Vraag 1: Hoe kun je dyspneu kwantificeren?
Het antwoord op de vraag ‘Wat is dyspneu’ kan verschillende invalshoeken hebben: hoe beschrijven mensen de sensatie, is het ‘zichtbaar’ of te objectiveren, en wat zijn de pathofysiologische mechanismen?
Een vaak gebruikte beschrijving van dyspneu is ‘een onaangename gewaarwording van de ademhaling’.1 Volgens deze definitie is dyspneu een gevoel dat alleen de patiënt zelf kan omschrijven. Op basis van de anamnese kan de hevigheid van het gevoel worden uitgedrukt in de Borg-score (tabel 1).

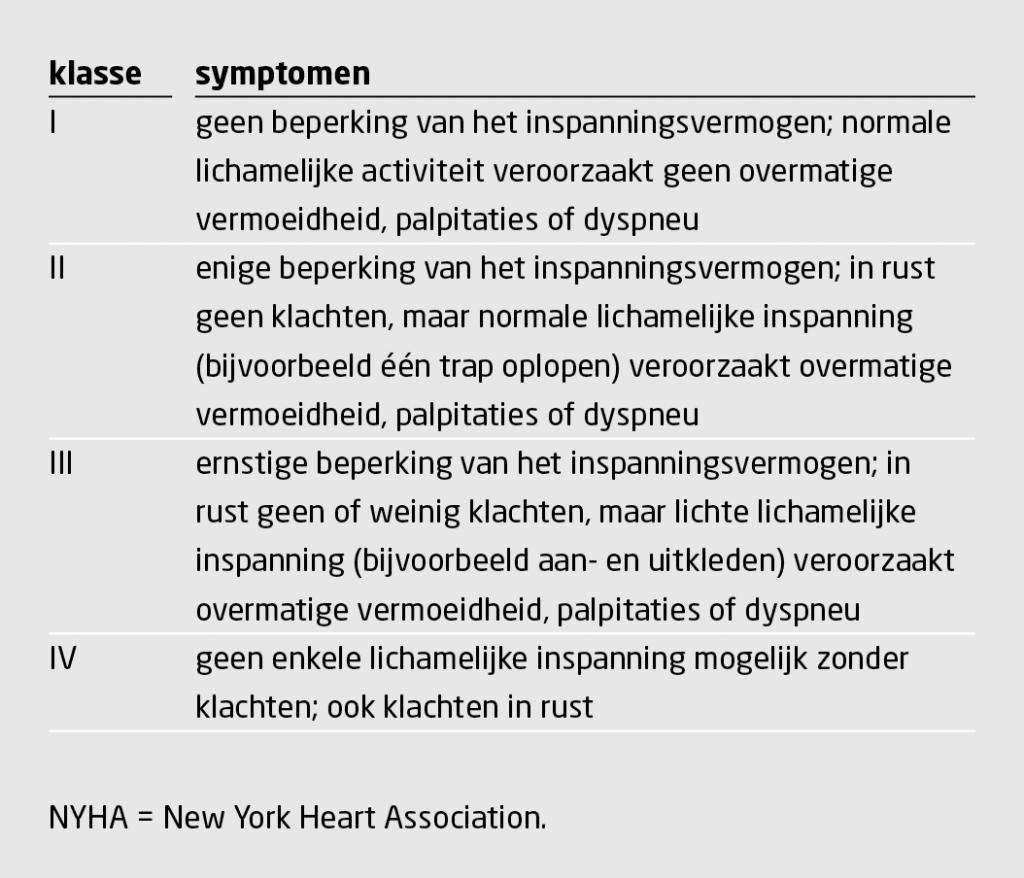
Men kan de ernst van dyspneu ook afmeten aan het effect op het inspanningsvermogen met bijvoorbeeld de classificatie voor hartfalen volgens de New York Heart Association (NYHA-klasse) of de ‘modified medical research council scale’ (mMRC-schaal)(tabel 2 en 3).

Vaak is dyspneu iemand aan te zien, door tachypneu, hoorbare ademhaling, gebruik van hulpademhalingsspieren, onvermogen om lange zinnen uit te spreken, of een angstige gelaatsuitdrukking.2 Dat geldt zowel bij ziekte als in gezondheid. Tijdens inspanning komt het moment van verzuring overeen met het moment waarop getrainde proefpersonen niet meer comfortabel kunnen spreken (de ‘talk test’).3 Het is belangrijk te beseffen dat uitwendig zichtbare tekenen niet altijd gepaard gaan met het gevoel van dyspneu. Iemand die hardloopt hoeft geen dyspneu te ervaren, ook al ademt hij of zij dieper en sneller dan in rust.
Dyspneu kan uiteenlopende oorzaken hebben, zoals een hart- of longziekte, bovensteluchtwegproblemen – bijvoorbeeld Reinke-oedeem van de stembanden –, aspiratie, bloedarmoede, sepsis, metabole ontregeling – bijvoorbeeld keto-acidose met Kussmaul-ademhaling –, een neuromusculaire ziekte, obesitas of achteruitgang in de lichamelijke conditie (‘deconditionering’).2 Dyspneu kan ook een uiting zijn van angst, meestal in combinatie met hyperventilatie,4 en komt zelfs bij gezonde mensen voor, met name tijdens inspanning. Wat alle oorzaken van dyspneu gemeen hebben, is dat ze leiden tot een verhoogde ademprikkel. Waarschijnlijk ontstaat dyspneu wanneer deze ademprikkel als onaangenaam wordt ervaren. Hierbij spelen de amygdala en de insula van de hersenschors een belangrijke rol.5
Het mechanisme van dyspneu hangt sterk af van de manier waarop de ademhaling wordt gestimuleerd. Op grond hiervan kunnen minstens 4 soorten dyspneu worden onderscheiden: luchthonger (dit ontstaat door stimulatie van chemoreceptoren), gevoel van verhoogde ademarbeid, benauwd gevoel door bronchospasme, en dyspneu door stimulatie van J-receptoren (‘juxtacapillaire receptoren’) die gelegen zijn in het interstitium van de long en die reageren op vasculaire stuwing of op bijvoorbeeld adenosine.1
Deze opsomming van oorzaken is niet volledig. Er zijn meer signalen die dyspneu kunnen opwekken. Cardiale ischemie bijvoorbeeld kan zich uiten als dyspneu, waarschijnlijk opgewekt door afferente sympathische vezels vanuit het hart (‘dyspneu-equivalent van angina pectoris’, of ‘blockpnea’).6
Van sommige ziekten is niet helemaal duidelijk hoe zij precies dyspneu veroorzaken. Een pneumothorax kan bijvoorbeeld leiden tot verhoogde ademarbeid doordat meer contractie van de ademspieren nodig is om dezelfde onderdruk in de pleuraholte te creëren tijdens inademing. Daarnaast speelt de ‘longdeflatiereflex’, die uitgaat van rekreceptoren in de luchtwegen, mogelijk een rol tijdens collaps van de long.7 Afhankelijk van de mate van hypoxemie worden ook de perifere chemoreceptoren gestimuleerd. Een ander voorbeeld is anemie. Het is al heel lang bekend dat anemie kan leiden tot een hyperdynamische circulatie en toegenomen ademhaling,8 maar het is niet precies bekend op welk mechanisme dit berust. Mogelijk spelen chemoreflexen een rol, hoewel anemie doorgaans niet gepaard gaat met hypoxemie.9
Een onderverdeling van dyspneu op basis van afferente stimuli, zoals we hier gedaan hebben, geeft inzicht in het onderliggende pathofysiologische probleem. Dit kan helpen bij het opstellen van een differentiaaldiagnose en uiteindelijk het stellen van de diagnose, vooral bij patiënten met een atypische presentatie.
Vraag 2: Welke oorzaken komen het vaakst voor?
Tabel 4 geeft een overzicht van oorzaken van dyspneu, onderverdeeld naar orgaansysteem en diagnose. De frequentie van voorkomen is afhankelijk van de setting: huisartsenpraktijk versus spoedeisende hulp versus de tweede lijn.
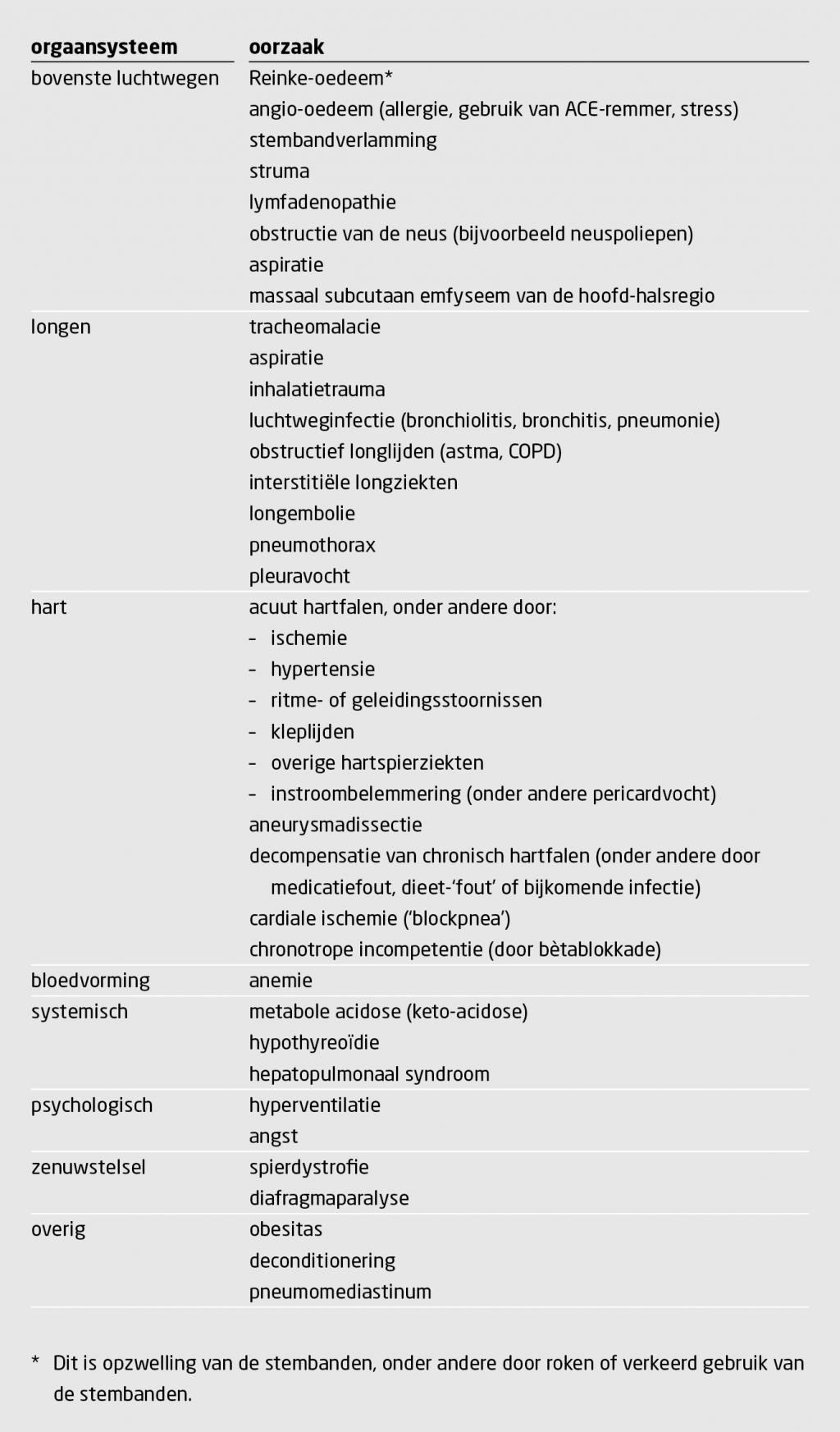
Uit Duits onderzoek bleek dyspneu bij patiënten op de Eerste Hulp vaak te berusten op pneumonie, COPD of acuut hartfalen.10 In de huisartsenpraktijk werd acute dyspneu vaak veroorzaakt door luchtweginfecties en pneumonieën. De meest voorkomende oorzaken van chronische dyspneu zijn astma, COPD, interstitiële longziekten, hartfalen door welke oorzaak dan ook (bijvoorbeeld door ischemie, hypertensie, klepgebreken, ritmestoornissen en hooggradig atrioventriculair blok), obesitas en deconditonering.11
Dyspneu komt in alle leeftijdscategorieën voor. In de leeftijdscategorie 0-4 jaar is tachypneu – een uitingsvorm van dyspneu – de meest voorkomende reden voor een bezoek aan de huisarts.12 Het beslaat een aanzienlijk deel van de kosten in de gezondheidszorg; in 2015 werd 8% van Nederlandse ambulanceritten ingezet vanwege ademhalingsproblemen. In 2016 werden vergelijkbare percentages (6-10%) gezien voor SEH-bezoeken.13
Diagnostiek
Vraag 3: Wat is een effectieve manier om dyspneu te analyseren?
Zoals bij veel klinische problemen verloopt de analyse meestal volgens een vast patroon. Het begint met de informatie die je op voorhand al krijgt over het probleem (verwijsbrief, telefonische informatie). In combinatie met bekende informatie (leeftijd, geslacht, voorgeschiedenis) is soms al een inschatting te maken van de ernst en de differentiaaldiagnose. Soms leidt dat al direct tot een interventie (‘ik wil hem vanmiddag op het spreekuur zien’, of ‘hij moet direct per ambulance naar het ziekenhuis’). Bij elke stap maken we een inschatting van de ernst, de differentiaaldiagnose en eventueel het mechanisme van de dyspneu. Bij elke stap kan dit leiden tot een interventie en een besluit over wat zinnig onderzoek is in de volgende stap.
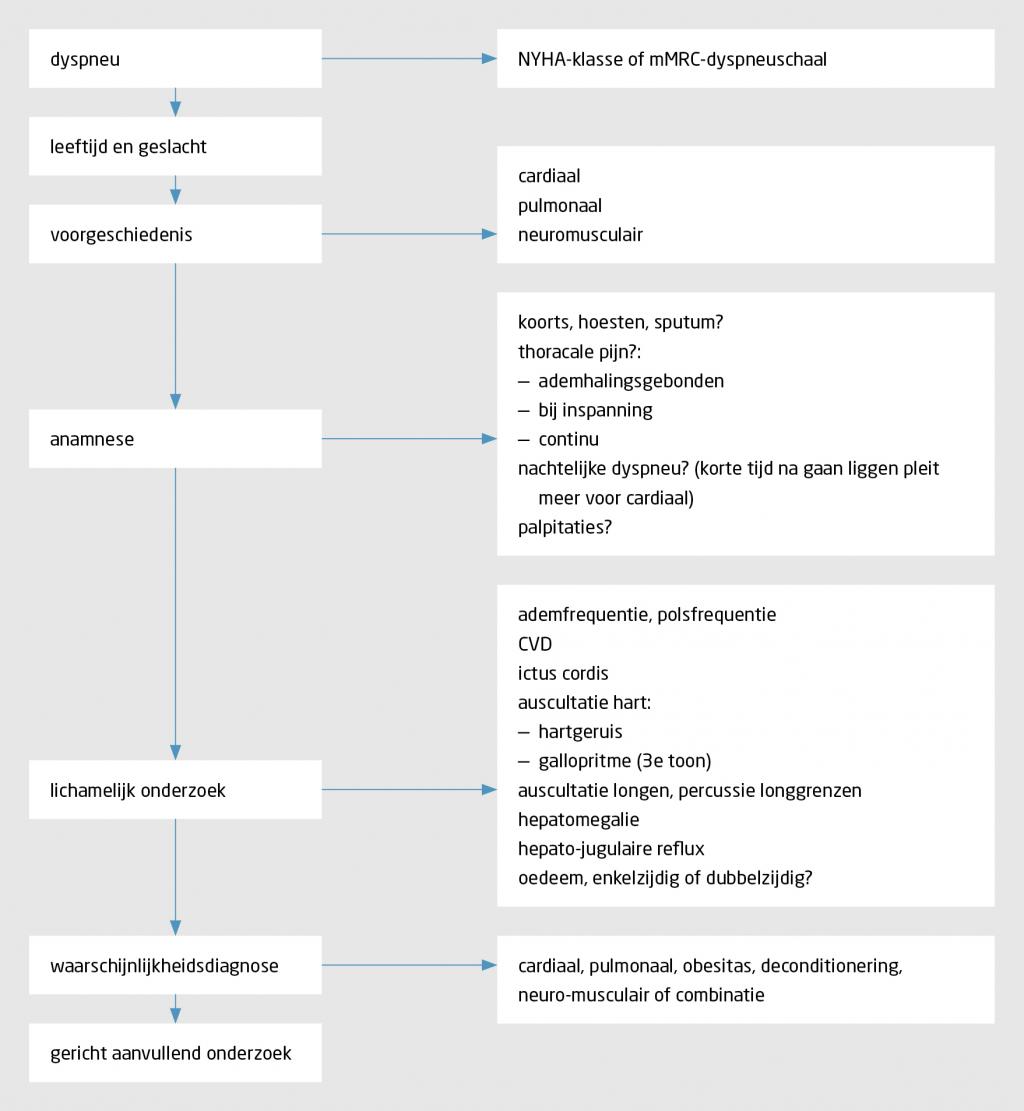
In het supplement bij dit artikel staat het voorbeeld van een 32-jarige man met acute dyspneu en pijn op de borst. Het is niet aangetoond dat deze benadering de meest effectieve is, maar dit is wel zoals het in de praktijk meestal werkt. Het stroomdiagram schetst de systematiek voor de analyse van dyspneu (figuur). Het overzicht van mogelijke oorzaken voor dyspneu in tabel 4 komt hierbij goed van pas, net als de aanwijzingen uit de anamnese en de fysische diagnostiek (zie vraag 4).
Vraag 4: Welke aanwijzingen uit anamnese en fysische diagnostiek zijn belangrijk?
Omdat dyspneu bij iedereen kan voorkomen en uiteenlopende oorzaken kan hebben, hangt het sterk van de situatie af – onder andere van de leeftijd, het geslacht en de voorgeschiedenis – welke anamnestische en fysisch-diagnostische gegevens belangrijk zijn. In het algemeen is het van belang om een beeld te krijgen van de cardiopulmonale toestand en de kans op een onderliggende ziekte. Tabel 5 laat zien hoe aanwijzingen uit de anamnese hiervoor te gebruiken zijn; tabel 6 geeft de belangrijkste aanwijzingen uit het fysisch-diagnostische onderzoek.


Zolang we de oorzaak niet weten, is het zinvol in ieder geval de gegevens te verzamelen die in tabel 5 en 6 vermeld staan. Interessant is op te merken dat veel aanwijzingen, zoals orthopneu, crepitaties en een verlengd exspirium, niet direct onderscheidend zijn voor een specifieke oorzaak van dyspneu.
Vraag 5: Welk laboratoriumonderzoek is belangrijk?
In het algemeen is het zinvol om de Hb-, kreatinine en TSH-waarde te laten bepalen, om een onderliggende anemie, nierinsufficiëntie en hyper- of hypothyreoïdie uit te sluiten. Nierinsufficiëntie kan dyspneu veroorzaken door een renale anemie, asthma renale of metabole acidose. De kans op anemie als enige oorzaak voor dyspneu is echter kleiner dan 0,1%.17 Bij een patiënt met acute dyspneu hoort ook een glucosemeting gedaan te worden, gezien de mogelijkheid van een keto-acidose.
Een perifere saturatiemeting geeft een eerste indruk van de oxygenatie en kan in combinatie met de ademhalingsfrequentie iets zeggen over de ernst van de respiratoire insufficiëntie. Foutief verlaagde waarden kunnen we zien bij patiënten met hypothermie, hypotensie of een slechte perifere doorbloeding. Bij een zuurstofsaturatie onder de 70% is pulsoximetrie ook niet meer betrouwbaar.18
Zolang de oorzaak van dyspneu niet bekend is, bestaat er een indicatie voor een bepaling van arteriële bloedgaswaarden. Deze zeggen iets over de ernst van een eventuele hypoxemie. De ernst van een intrapulmonale gaswisselingsstoornis kan worden afgemeten aan het alveolo-arteriële zuurstofgradiënt (PA-ao2, zie uitleg). Hierin is de PAo2 de ‘ideale’ alveolaire Po2, dat wil zeggen: de alveolaire Po2 die je zou verwachten bij de gemeten arteriële Pco2 als de gaswisseling in de long perfect is. De PA-ao2 is het verschil tussen deze ideale alveolaire Po2 en de werkelijk gemeten arteriële Po2. Een verhoogd PA-ao2 duidt op een gaswisselingsstoornis in de long. Bij gezonde mensen in rust is PA-ao2 < 30 mmHg (< 4 kPa). Hypoxemie bij een niet-afwijkend PA-ao2 past bij hypoventilatie.
Bepaling van arteriële bloedgaswaarden heeft ook toegevoegde waarde bij de verdenking op een koolmonoxidevergiftiging, aangezien een perifere saturatiemeting met pulsoximetrie geen onderscheid maakt tussen hemoglobinemoleculen waaraan zuurstof is gebonden en hemoglobinemoleculen waaraan koolmonoxide (CO) gebonden is. Hierdoor kan er bij CO-vergiftiging een foutief-verhoogde perifere saturatie gemeten worden. Dit geldt ook voor methemoglobinemie, waarbij het hemoglobine door oxidatie van het haemmolecuul (Fe3+ in plaats van Fe2+) niet in staat is om zuurstof te binden en te vervoeren. Een pulsoximeter maakt namelijk geen onderscheid tussen geoxigeneerd hemoglobine en methemoglobine.
Een arteriële bloedgaswaarde levert ook informatie op over eventuele hypercapnie of metabole acidose. In sommige gevallen kan worden volstaan met een capillaire of veneuze bloedgaswaarde.19,20
Natriuretische peptiden zoals brein-natriuretisch peptide (BNP) en NT-proBNP kunnen zowel gebruikt worden om de diagnose ‘hartfalen’ te stellen als om de behandeling te monitoren. Deze peptiden hebben vooral diagnostische betekenis als een echocardiogram niet beschikbaar is. Bij acuut hartfalen liggen de afkapwaarden hoger dan bij chronisch hartfalen. Ook zijn de afkapwaarden leeftijdsafhankelijk. De afkapwaarden zijn 400 pg/ml (NT-proBNP) en 100 pg/ml (BNP) voor acuut hartfalen en 125 pg/ml (NT-proBNP) en 35 pg/ml (BNP) voor geleidelijk ontstaan hartfalen.21 Bij deze afkapwaarden heeft de bepaling een hoge negatief voorspellende waarde, zowel voor acuut als chronisch hartfalen (94-98%). De positief voorspellende waarde is echter beduidend lager (66% en 44-57% bij respectievelijk acuut en chronisch hartfalen). Natriuretische peptiden zijn dus vooral geschikt om hartfalen uit te sluiten, niet zozeer om het aan te tonen.
De concentraties van natriuretische peptiden kunnen ook verhoogd zijn door atriumfibrilleren of nierinsufficiëntie zonder evident hartfalen.21 De NHG-richtlijn ‘Hartfalen’ adviseert om bij een vermoeden van hartfalen een ecg te maken en het (NT-pro)BNP te bepalen. Bij een abnormaal ecg of een verhoogde BNP- of NT-proBNP-waarde is nader onderzoek aangewezen, in de vorm van laboratoriumonderzoek, echocardiografie en eventueel een thoraxfoto.
De D-dimeerbepaling heeft een plaats in de diagnostiek naar acute longembolie. De D-dimeerwaarde is verhoogd bij acute trombose door de gelijktijdige activatie van coagulatie en fibrinolyse. Deze bepaling heeft een hoge negatief voorspellende waarde voor longembolie als de klinische verdenking laag is; de klinische verdenking is met de Wells-score in te schatten.22 Een verhoogde D-dimeerwaarde kan ook veroorzaakt worden door onder andere longontsteking of aortadissectie.
Vraag 6: Welk beeldvormend onderzoek?
Een thoraxfoto is zinvol bij de meeste patiënten die zich presenteren met dyspneu. Uitzonderingen zijn bijvoorbeeld jonge astmapatiënten, die duidelijke obstructieve longgeluiden laten horen en die ooit al beeldvormend onderzoek hebben gehad. De thoraxfoto kan helpen om pneumonie, pneumothorax, pleuravocht, diafragmaparalyse, decompensatio cordis, interstitiële afwijkingen, skeletafwijkingen, lymfadenopathie en ruimte-innemende processen vast te stellen. Al deze afwijkingen kunnen een rol spelen bij dyspneu. Met name bij interstitiële afwijkingen, lymfadenopathie en ruimte-innemende processen is een CT-scan van de thorax aangewezen, eventueel met CT-angiografie van de A. pulmonalis bij de verdenking op longembolie. Bij een sterke verdenking op pulmonale arteriële hypertensie of een primair cardiale afwijking bestaat er een indicatie voor een echocardiogram.
Vraag 7: Wat is de waarde van functioneel onderzoek?
Functioneel onderzoek heeft een plaats bij klachten van subacute en chronische dyspneu, vooral als het algemene laboratoriumonderzoek (genoemd bij vraag 5), de röntgenfoto (genoemd bij vraag 6) en het ecg geen directe verklaring voor de dyspneu bieden. De meeste pulmonale oorzaken van dyspneu geven afwijkingen bij longfunctieonderzoek (spirometrie, CO-diffusiebepaling of plethysmografie (‘bodybox’-meting)). Vaak gaat het om bronchusobstructie of restrictie, al dan niet in combinatie met verkleining van het oppervlak van de alveolo-capillaire membraan (verlaagde diffusiecapaciteit).23
Een laag expiratoir reservevolume bij spirometrie past bij belemmerde ademhaling door abdominale adipositas.24 Een uitzondering is astma, waarbij de uitslagen van spirometrie niet-afwijkend kunnen zijn. Om deze diagnose te kunnen stellen is soms aanvullend een metacholine- of histamine-provocatietest nodig. Deze test is vooral sensitief, maar minder specifiek voor de diagnose ‘astma’. Ook bij longembolie – zowel acute als chronische – worden met longfunctieonderzoek vaak weinig afwijkingen gevonden; meestal is de CO-diffusie slechts licht verlaagd.25 Chronisch hartfalen daarentegen kan gepaard gaan met zowel obstructieve als restrictieve longfunctiestoornissen.26
Als de origine van dyspneu onduidelijk is, en vooral wanneer er getwijfeld wordt tussen een pulmonale of cardiale oorzaak, kan ergometrie vaak duidelijkheid geven.27
Behandeling
Vraag 8: Helpt zuurstof tegen het dyspneugevoel, en wanneer moet je zuurstof geven?
Zuurstofsuppletie is noodzakelijk bij een saturatie < 90%, ongeacht de onderliggende afwijking (dit is een veilige grens).28 Volgens een Cochrane-review uit 2005 verbetert continue zuurstoftherapie de overleving van patiënten met ernstige COPD (Pao2 < 8 kPa of < 55 mmHg).29 Zuurstof heeft echter beperkt effect op het dyspneugevoel bij stabiele COPD-patiënten en bij veel patiënten heeft het zelfs helemaal geen effect.30 Dit is vermoedelijk te verklaren door andere oorzaken van dyspneu bij COPD, zoals de toegenomen ademarbeid.
In een trial bleek slechts een klein deel van COPD-patiënten met lichte hypoxemie minder dyspneu te ervaren met zuurstof dan met placebo (lucht toegediend via een neusbril).31 Een studie onder patiënten met gevorderde kanker liet geen verschil zien tussen inhalatie van zuurstof en kamerlucht voor wat betreft de klachten van dyspneu.32 Voor andere ziekten, zoals chronisch hartfalen, zijn geen vergelijkbare studies verricht, maar de genoemde bevindingen gelden daar hoogstwaarschijnlijk ook voor.
Vraag 9: Welke behandelopties zijn er voor dyspneu?
Een behandeling is het effectiefst als deze gericht is op het ontstaansmechanisme van de dyspneu. Zo zal bij een diepe hypoxemie de toediening van zuurstof vaak effectief zijn. Luchtwegverwijdende medicamenten verbeteren de longinflatie en kunnen vooral helpen bij bronchospasme en luchthonger. Hetzelfde geldt voor invasieve en non-invasieve beademing, die bovendien zorgen dat de patiënt minder ademarbeid hoeft te leveren. Bij patiënten met chronische dyspneu als gevolg van COPD kunnen technieken als ‘pursed lip breathing’ en ‘actieve expiratie’ het gevoel van ademarbeid verminderen. Ook het trainen van de conditie kan de dyspneu doen afnemen, net als gewichtsreductie bij patiënten met obesitas.
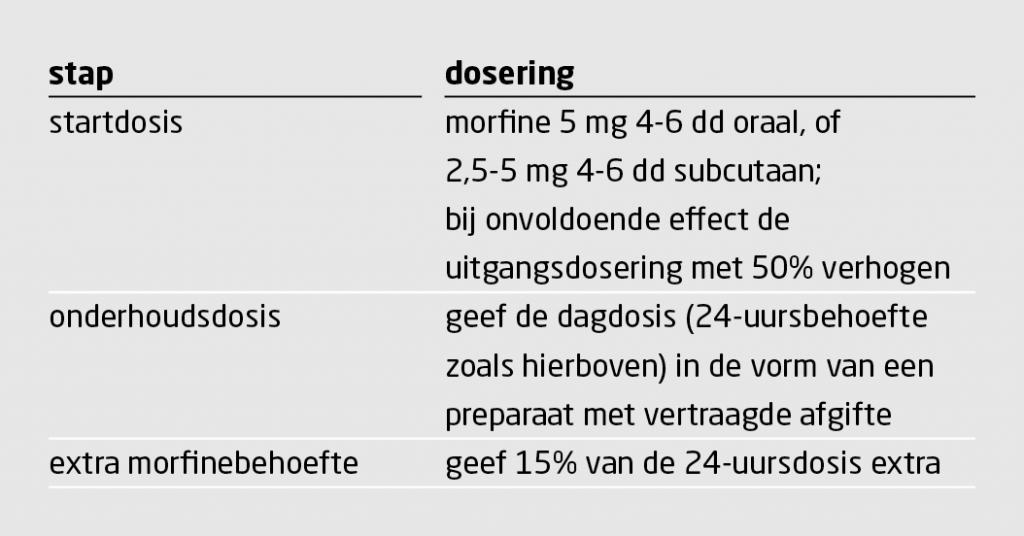
Bij refractaire dyspneu door luchthonger kunnen chemoreflexen worden gedempt met morfinomimetica, ongeacht het onderliggende lijden.33 Voor patiënten met COPD in het eindstadium die nog niet eerder met opioïden behandeld zijn, kan het morfine-stappenplan in tabel 7 als leidraad dienen, in het geval van refractaire dyspneu.34
Bij patiënten met chronisch hartfalen kan de symptomatische behandeling gericht worden op de oorzaak van de dyspneu. Zo kan overvulling medicamenteus behandeld worden met diuretica, en systolisch hartfalen met ACE-remmers en bètablokkers. Daarnaast dient de onderliggende oorzaak behandeld te worden, bijvoorbeeld door revascularisatie of door behandeling van hypertensie, kleplijden of een ritmestoornis.
Vraag 10: Wat is de plaats van een multidisciplinaire aanpak?
Omdat dyspneu vaak ontstaat door afwijkingen in meerdere orgaansystemen, vraagt de aanpak een brede kijk op het lichaam. Dat betekent niet dat iedere patiënt met dyspneu door verschillende specialisten hoeft te worden gezien. Bij een aantal patiënten is er één duidelijke – voornaamste – oorzaak aan te wijzen, bijvoorbeeld bronchusobstructie door COPD of linksdecompensatie door een myocardinfarct. Bij deze patiënten is een multidisciplinaire aanpak niet direct noodzakelijk.
Een voorwaarde is wel dat de dokter die in de tweede lijn bij de patiënt betrokken is, situaties herkent waarin de klachten niet goed door de vastgestelde afwijking worden verklaard en waarbij dus een combinatie van ziektebeelden als oorzaak aan te wijzen is. Daarbij is het voor de huisarts soms lastig om in te schatten of dyspneu primair door een pulmonaal of cardiaal probleem wordt veroorzaakt. Het lijkt dan ook zinvol dat in elk ziekenhuis een overlegstructuur bestaat tussen op zijn minst een cardioloog en een longarts, eventueel geïntegreerd in een ‘eerste hart-longhulp’ of ‘dyspneupoli’ (voor respectievelijk acute en chronische geneeskunde). In academische ziekenhuizen is er een plaats voor multidisciplinair overleg tussen cardioloog en longarts om patiënten te bespreken die zijn verwezen met dyspneu waarvan de oorzaak niet direct duidelijk is.
Tot besluit
In dit leerartikel hebben we een beperkt antwoord gegeven op 10 vragen over dyspneu. Een uitgebreider antwoord is mogelijk, maar vraagt ook om meer onderzoek naar het mechanisme van dyspneu en de effectiviteit van verschillende diagnostische strategieën. Wel hebben we een strategie voorgesteld om dyspneu in de klinische praktijk te analyseren. De belangrijkste pijlers onder deze strategie zijn de inschatting van de ernst van het probleem, het opstellen van een differentiaaldiagnose, nadenken over het mechanisme van dyspneu en tijdige interventies. We denken dat de analyse en behandeling van dyspneu zich bij uitstek lenen voor een multidisciplinaire aanpak.
Literatuur
-
Van den Aardweg JG. 4 soorten dyspneu. Ned Tijdschr Geneeskd. 2013;157:A5415 Medline.
-
Parshall MB, Schwartzstein RM, Adams L, et al; American Thoracic Society Committee on Dyspnea. An official American Thoracic Society statement: update on the mechanisms, assessment, and management of dyspnea. Am J Respir Crit Care Med. 2012;185:435-52. doi:10.1164/rccm.201111-2042ST. Medline
-
Recalde PT, Foster C, Skemp-Arlt KM, et al. The ‘Talk Test’ as a simple marker of ventilatory threshold. S Afr J Sports Med. 2002;9:5-8.
-
Van den Aardweg JG, Berretty EW. Inzicht in hyperventilatie. Houten: Lannoo; 2018.
-
Herigstad M, Hayen A, Wiech K, Pattinson KT. Dyspnoea and the brain. Respir Med. 2011;105:809-17. doi:10.1016/j.rmed.2010.12.022. Medline
-
Chevalier H. Blockpnea on effort in emphysematous patients—a diagnostic challenge. Am Heart J. 1967;73:579-81. doi:10.1016/0002-8703(67)90166-4. Medline
-
Guz A, Noble MI, Eisele JH, Trenchard D. The effect of lung deflation on breathing in man. Clin Sci. 1971;40:451-61. doi:10.1042/cs0400451. Medline
-
Blumgart HL, Altschule MD. Clinical significance of cardiac and respiratory adjustments in chronic anemia. Blood. 1948;3:329-48. doi:10.1182/blood.V3.4.329.329. Medline
-
Hatcher JD, Chiu LK, Jennings DB. Anemia as a stimulus to aortic and carotid chemoreceptors in the cat. J Appl Physiol. 1978;44:696-702. doi:10.1152/jappl.1978.44.5.696. Medline
-
Berliner D, Schneider N, Welte T, Bauersachs J. The differential diagnosis of dyspnea. Dtsch Arztebl Int. 2016;113:834-45 Medline.
-
Pratter MR, Curley FJ, Dubois J, Irwin RS. Cause and evaluation of chronic dyspnea in a pulmonary disease clinic. Arch Intern Med. 1989;149:2277-82. doi:10.1001/archinte.1989.00390100089021. Medline
-
Frese T, Sobeck C, Herrmann K, Sandholzer H. Dyspnea as the reason for encounter in general practice. J Clin Med Res. 2011;3:239-46. doi:10.4021/jocmr642w. Medline
-
Bron: www.volksgezondheidenzorg.info/onderwerp/acute-zorg, kijk onder ‘Cijfers & Context. Geraadpleegd op 13 januari 2020.
-
Storey RF, Becker RC, Harrington RA, et al. Characterization of dyspnoea in PLATO study patients treated with ticagrelor or clopidogrel and its association with clinical outcomes. Eur Heart J. 2011;32:2945-53. doi:10.1093/eurheartj/ehr231. Medline
-
Medical Multimedia Laboratories. Heart sounds and cardiac arrhytmias. www.blaufuss.org/ Doorklikken naar ‘Heart Sounds Tutorial’ en de ‘Heart Sounds Quiz’.
-
Hamer JPM, Pieper PG, van den Brink RBA. Het beoordelen van de centraalveneuze druk. Ned Tijdschr Geneeskd. 2016;160:A9600 Medline.
-
Thoonen BPA, Van Weel C. Kortademigheid. Huisarts Wet. 2002;45:414-9.
-
Jensen LA, Onyskiw JE, Prasad NG. Meta-analysis of arterial oxygen saturation monitoring by pulse oximetry in adults. Heart Lung. 1998;27:387-408. doi:10.1016/S0147-9563(98)90086-3. Medline
-
Zavorsky GS, Cao J, Mayo NE, Gabbay R, Murias JM. Arterial versus capillary blood gases: a meta-analysis. Respir Physiol Neurobiol. 2007;155:268-79. doi:10.1016/j.resp.2006.07.002. Medline
-
Van Exsel JA, Simons SO, Kramers C, Heijdra YF. Wanneer volstaat een veneuze bloedgas op de SEH? Ned Tijdschr Geneeskd. 2017;161:D785 Medline.
-
Ponikowski P, Voors AA, Anker SD, et al; ESC Scientific Document Group. 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J. 2016;37:2129-200. doi:10.1093/eurheartj/ehw128. Medline
-
Carrier M, Righini M, Djurabi RK, et al. VIDAS D-dimer in combination with clinical pre-test probability to rule out pulmonary embolism. Thromb Haemost. 2009;101:886-92. doi:10.1160/TH-08-10-0689. Medline
-
Heijdra YF, van Helvoort HAC. Praktische handleiding longfunctietesten. Houten: Bohn Stafleu van Loghem, 2006.
-
Jones RL, Nzekwu MM. The effects of body mass index on lung volumes. Chest. 2006;130:827-33. doi:10.1378/chest.130.3.827. Medline
-
Piirilä P, Laiho M, Mustonen P, et al. Reduction in membrane component of diffusing capacity is associated with the extent of acute pulmonary embolism. Clin Physiol Funct Imaging. 2011;31:196-202. doi:10.1111/j.1475-097X.2010.01000.x. Medline
-
Minasian AG, van den Elshout FJ, Dekhuijzen PN, et al. Pulmonary function impairment in patients with chronic heart failure: lower limit of normal versus conventional cutoff values. Heart Lung. 2014;43:311-6. doi:10.1016/j.hrtlng.2014.03.011. Medline
-
Palange P, Ward SA, Carlsen KH, et al; ERS Task Force. Recommendations on the use of exercise testing in clinical practice. Eur Respir J. 2007;29:185-209. doi:10.1183/09031936.00046906. Medline
-
Smulders YM, van den Aardweg JG. Kan dat neusbrilletje met zuurstof niet af? Ned Tijdschr Geneeskd. 2018;162:D2497 Medline.
-
Cranston JM, Crockett A, Moss J, Alpers JH. Domiciliary oxygen for chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2005;(4):CD001744. Medline
-
Lacasse Y, Lecours R, Pelletier C, Bégin R, Maltais F. Randomised trial of ambulatory oxygen in oxygen-dependent COPD. Eur Respir J. 2005;25:1032-8. doi:10.1183/09031936.05.00113504. Medline
-
Nonoyama ML, Brooks D, Guyatt GH, Goldstein RS. Effect of oxygen on health quality of life in patients with chronic obstructive pulmonary disease with transient exertional hypoxemia. Am J Respir Crit Care Med. 2007;176:343-9. doi:10.1164/rccm.200702-308OC. Medline
-
Booth S, Kelly MJ, Cox NP, Adams L, Guz A. Does oxygen help dyspnea in patients with cancer? Am J Respir Crit Care Med. 1996;153:1515-8. doi:10.1164/ajrccm.153.5.8630595. Medline
-
Jennings AL, Davies AN, Higgins JP, Gibbs JS, Broadley KE. A systematic review of the use of opioids in the management of dyspnoea. Thorax. 2002;57:939-44. doi:10.1136/thorax.57.11.939. Medline
-
Long Alliantie Nederland. Richtlijn palliatieve zorg voor mensen met COPD. Amersfoort: LAN; 2011.





Aanvullingen op tabel 6
Ik mis in tabel 6 een aantal items: percussie van het hart en met name de longen (pleuravocht, hoogstand diafragma), onderzoek van het abdomen gericht op hepatomegalie en eventuele ascites (hartfalen, processen die leiden tot hoogstand van het diafragma), oedeem aan de benen en gewicht.
E.M. Stuiveling, huisarts
Het oog ziet meer dan het oort hoort
Wij pleiten voor meer gebruik van point-of-care echografie (point-of-care ultrasonography - POCUS) tijdens het lichamelijk onderzoek. Helaas sloegen de auteurs het gebruik van POCUS over bij de analyse van dyspnoe, terwijl echografie hier juist veel in kan betekenen. Het gebruik van POCUS van de thorax heeft een hogere sensitiviteit dan auscultatie en percussie voor diverse pulmonale afwijkingen zoals longoedeem, pneumothorax en pleuravocht. Ook de specificiteit van echografische bevindingen is vaak hoger dan die van het klassieke lichamelijke onderzoek.1,2 Daarnaast is echografie van de thorax in veel opzichten superieur aan de X-thorax.3,4
Met het verweven van POCUS in het lichamelijk onderzoek kan de patiënt(e) bovendien gewoon doorpraten. Hierdoor kan de speciële anamnese doorgaan tijdens het lichamelijk onderzoek en kan op real-time nieuwe informatie het consult bijgestuurd worden. Hiermee wordt de kwaliteit van het patiëntconsult per tijdseenheid fors verhoogd terwijl dit netto nauwelijks extra tijd kost. Door de gerichtere aanvullende vervolgonderzoeken kan de patiënt(e) bovendien onnodige potentieel schadelijke aanvullende handelingen bespaard worden en kan er efficiënter gebruik gemaakt worden van ondersteunende disciplines.
Tegenwoordig past, net zoals de stethoscoop, ook een kwalitatief goed echografieapparaat in de doktersjas.
referenties:
1. Kimura BJ, Point-of-care cardiac ultrasound techniques in the physical examination: better at bedside. Heart 2017;103:987-994
2. Al Deeb M, et al. Point-of-care ultrasonography for the diagnosis of acute cardiogenic pulmonary edema in patients presenting with acute dyspnea: a systematic review and meta-analysis. Acad Emerg Med 2014;21:843
3. Ye X, et al. Accuracy of Lung Ultrasonography versus Chest Radiography for the Diagnosis of Adult Community-Acquired Pneumonia: Review of the Literature and Meta-Analysis. PLoS One 2015;10:e0130066
4. Alrajab S, et al. Pleural ultrasonography versus chest radiography for the diagnosis of pneumothorax: review of the literature and meta-analysis. Crit Care 2013;17(5):R208.
drs. Dirk Tjwa, UMC Utrecht, afdeling interne geneeskunde, Utrecht, internist-acute geneeskunde
dr. Martijn Bauer, LUMC, afdeling interne geneeskunde, Leiden, internist-acute geneeskunde
prof. dr. Frank Bosch, RadboudUMC, afdeling interne geneeskunde, Nijmegen, internist-acute geneeskunde