artikel
De laatste jaren groeit de bezorgdheid over mogelijk schadelijke effecten van anesthesie op jonge leeftijd.1 Het aantal proefdieronderzoeken waarin neurotoxiciteit van anesthetica is aangetoond, neemt sinds 2003 nog steeds toe. Bij de mens is echter nog niet met zekerheid vastgesteld dat blootstelling aan anesthetica leidt tot een gestoorde neurologische ontwikkeling. Wel blijkt uit een aantal retrospectieve cohortonderzoeken dat kinderen die op jonge leeftijd meerdere operaties onder algehele anesthesie hebben ondergaan, op latere leeftijd meer last hebben van leerstoornissen en gedragsproblemen.2-4
Op dit moment is er discussie of de waarnemingen bij proefdieren nu al zouden moeten leiden tot een terughoudend beleid met betrekking tot operaties en diagnostische procedures onder algehele anesthesie bij zeer jonge kinderen. Veel anesthesiologen zijn er niet van overtuigd dat de bevindingen van dierexperimenteel onderzoek ook van toepassing zijn op mensen. Daarentegen menen sommige neurowetenschappers die zich bezighouden met onderzoek bij dieren dat er voldoende aanleiding is om terughoudender te zijn met blootstelling van jonge kinderen aan anesthetica. Zij vinden dat anesthesie bij jonge kinderen gereserveerd zou moeten worden voor ingrepen bij levensbedreigende situaties en ingrepen waarmee ernstige functionele beperkingen voorkomen kunnen worden.5 Vanwege deze discussie vinden wij het belangrijk om een overzicht te geven van de wetenschappelijke stand van zaken op het gebied van kinderanesthesiologie en hersenontwikkeling.
Dierexperimenteel onderzoek
Tijdens de zogenoemde groeispurt van de hersenen is het brein gevoelig voor beschadiging door anesthetica zoals propofol, isofluraan en sevofluraan, gamma-aminoboterzuur(GABA)-agonisten en ketamine (een N-methyl-D-asparaginezuur(NMDA)-antagonist) (tabel). Uit dierexperimenteel onderzoek blijkt dat enkele uren blootstelling aan anesthetica van jonge dieren tot 30 dagen postnataal leidt tot een sterke toename van neuroapoptose en tot veranderingen in dendritische morfologie.6 De mechanismen achter deze fenomenen zijn tot op heden niet bekend, maar verondersteld wordt dat anesthetica een vermindering van neurotrofe factoren, zoals ‘brain-derived neurotrophic factor’, veroorzaken. Tevens zou de upregulatie van NMDA-receptoren door anesthetica kunnen leiden tot excitotoxiciteit (overstimulatie door toxische concentraties van neurotransmitter glutamaat).7
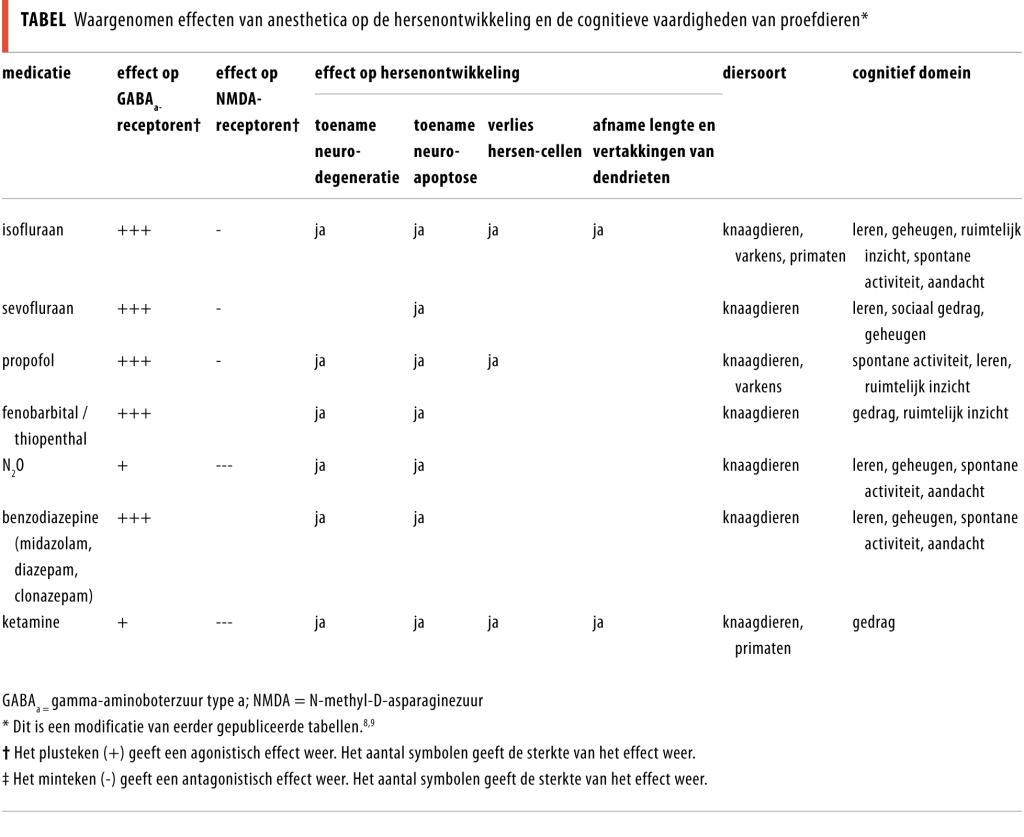
Er is sprake van een soortspecifieke kwetsbare periode (‘window of vulnerability’) waarin het brein het gevoeligst is voor de schadelijke effecten van anesthesie. Deze effecten zijn duidelijk dosisgerelateerd: hoe vaker, hoe langer en hoe meer anesthesie, des te meer schade.10 Opmerkelijk is dat dit fenomeen in tientallen dierexperimentele onderzoeken wordt beschreven bij vrijwel alle anesthetica die in de dagelijkse praktijk voor kinderen worden gebruikt voor sedatie en anesthesie. Voorbeelden hiervan zijn midazolam, ketamine, propofol en inhalatieanesthetica zoals sevofluraan en isofluraan.9 Neurotoxiciteit door anesthetica werd aanvankelijk alleen beschreven bij knaagdieren, maar sinds 2007 ook bij primaten zoals de resusaap (Macaca mulatta).9 Tevens is er bewijs dat dieren die op jonge leeftijd blootgesteld zijn aan anesthetica op latere leeftijd leer- en gedragsstoornissen vertonen.10
Een belangrijk punt van kritiek op dierexperimenteel onderzoek is dat het niet mogelijk is om laboratoriumbevindingen 1 op 1 te vertalen naar de klinische situatie bij de mens. Het is dus mogelijk dat de schadelijke effecten van anesthetica irrelevant zijn voor mensen doordat menselijke hersenen een langere rijping en meer herstelcapaciteit hebben. Bovendien is het lastig om resultaten van onderzoek naar de effecten van intraveneuze anesthetica bij proefdieren te vertalen naar de mens omdat er grote verschillen zijn in de dosis-responsrelatie tussen dieren en mensen. Dit geldt in mindere mate voor inhalatieanesthetica; na toediening hiervan aan resusapen van 6 dagen oud werd toegenomen neuroapoptose waargenomen. De apen kregen gedurende een periode van 5 h isofluraaninhalatie in een dosering van 0,7-1,5%; deze dosering is vergelijkbaar met die bij neonaten en zuigelingen.11
Retrospectieve studies bij de mens
Het klinisch onderzoek naar de effecten van anesthesie op het menselijke brein in ontwikkeling is schaars; we hebben vooralsnog alleen de resultaten van enkele retrospectieve cohortonderzoeken. Het blijkt niet eenvoudig om een cohort te vinden met adequate gegevens over chirurgie en vooral anesthesie, en de follow-up hiervan. Hieronder vatten wij het tot nu toe gepubliceerde werk samen.
Een groep uit de Verenigde Staten beschreef diverse retrospectieve analyses van een geboortecohort van 5357 kinderen uit Olmsted County (Minnesota, Verenigde Staten), van wie er 593 algehele anesthesie voor het 4e levensjaar hadden gehad.2 Uit deze analyses bleek dat kinderen die 2 of meer operaties hadden gehad een verhoogde kans hadden op leerproblemen en ADHD op de langere termijn. Tevens was er een verband te zien tussen de cumulatieve anesthesieduur en het optreden van leerproblemen en ADHD.2,4
Een ander cohort werd gevormd door kinderen die geboren waren in de periode 1999-2001 in de staat New York en van wie de ouders gratis verzekerd waren in het kader van Medicaid (een gezondheidsverzekering voor de allerarmsten). In dit retrospectieve onderzoek hadden 383 kinderen voor hun 3e levensjaar een liesbreukoperatie ondergaan; zij werden vergeleken met een steekproef van 5050 en 10450 kinderen zonder liesbreukoperatie.2,3 Er werd gecorrigeerd voor bekende confounders als geslacht, leeftijd en geboortegerelateerde complicaties zoals laag geboortegewicht. Uit beide onderzoeken bleek dat er een relatie bestond tussen operaties onder algehele anesthesie vóór het 3e levensjaar en ontwikkelings- en gedragsstoornissen zoals vertraagde ontwikkeling, mentale retardatie, autisme en taal- en spraakproblemen. Het risico nam toe van 1,1 voor 1 operatie (95%-BI: 0,8-1,4) tot 4,0 voor ≥ 3 operaties (95%-BI: 3,5-4,5).
Van kinderen die in de neonatale fase aan een congenitale cardiovasculaire afwijking geopereerd worden, is al langer bekend dat zij een verhoogd risico hebben op het ontwikkelen van neurologische afwijkingen. Uit een recent onderzoek bleek dat neonaten die geopereerd waren aan andere, niet-cardiale congenitale afwijkingen – zoals gastroschisis, anusatresie, pylorushypertrofie – even slecht scoorden op cognitieve testen en taalvaardigheidstesten als neonaten die geopereerd waren aan een cardiale congenitale afwijking. 73% van de geopereerde kinderen scoorde onder het gemiddelde niveau.12
Bij retrospectief epidemiologisch onderzoek is confounding door comorbiditeit een groot probleem. Zo bleken in een epidemiologisch onderzoek de leerprestaties op 15-jarige leeftijd binnen een geboortecohort significant lager te zijn bij kinderen die voor hun 1e jaar een liesbreukoperatie hadden gehad (n = 2689) dan bij een controlegroep van kinderen die niet geopereerd waren aan een liesbreuk (n = 14575).13 Na correctie voor bekende confounders (geslacht, geboortegewicht, opleidingsniveau en leeftijd van de ouders) kon dit verband echter niet meer worden aangetoond. Een mogelijkheid om voor de invloed van confounders te corrigeren, is door een cohortonderzoek uit voeren met monozygote tweelingen.
Een cohortonderzoek met tweelingparen is gedaan in de VU. Daaruit bleek dat wanneer beide kinderen waren blootgesteld aan anesthesie voor het 3e levensjaar, ze allebei lager scoorden op de Cito-toets en meer cognitieve problemen hadden dan de tweelingparen die voor hun 3e jaar niet blootgesteld waren aan anesthesie. Wanneer echter slechts 1 kind van een tweelingpaar was blootgesteld aan anesthesie voor het 3e levensjaar, was er geen verschil tussen beide kinderen.14 In dit onderzoek was geen informatie beschikbaar over de aard van de operatie en het type anesthesie. Het zou goed mogelijk kunnen zijn dat de blootstelling aan anesthesie in de discordante tweelingparen te kort was om een effect te hebben op later cognitief functioneren.
Prospectief onderzoek
Het is bijzonder lastig om een klinisch onderzoek op te zetten waarin de mogelijke causaliteit van anesthesie als oorzaak voor hersenschade kan worden vastgesteld. Om de relatieve bijdrage van de primaire aandoening, de anesthesie en de chirurgie inclusief ziekenhuisopname te onderzoeken zou men idealiter kinderen randomiseren tussen wel en geen anesthesie zonder chirurgie, of tussen chirurgie met en zonder anesthesie. Een dergelijke opzet is op ethische gronden uiteraard onmogelijk. Gerandomiseerd onderzoek waarin algehele anesthesie met regionale (spinale) anesthesie wordt vergeleken lijkt tot nu toe de enige mogelijkheid om op termijn inzicht te krijgen in de rol van blootstelling aan algehele anesthesie.
Op dit moment loopt er in onder meer Australië, de Verenigde Staten, het Verenigd Koninkrijk, Italië en Nederland een RCT waarbij 720 kinderen van < 5 maanden oud die een liesbreukoperatie moeten ondergaan, worden gerandomiseerd tussen algehele anesthesie óf locoregionale (spinale) anesthesie (GAS-studie; meer informatie is te vinden op http://clinicaltrials.gov/ct2/show/NCT00756600). De inclusie van patiënten loopt in 2013 ten einde. Omdat het niet mogelijk is om bij kinderen voor het 5e levensjaar betrouwbaar neurocognitief onderzoek te doen, zullen we minstens tot 2018 moeten wachten voordat er betrouwbare conclusies uit dit onderzoek getrokken kunnen worden. Omdat een liesbreukoperatie minder dan een uur duurt, zal dit onderzoek slechts inzicht geven in de effecten van relatief korte blootstelling aan anesthetica.
Beleid
Hoe nu verder? De schadelijkheid van blootstelling aan anesthetica voor de hersenontwikkeling is veelvuldig aangetoond in dierexperimenteel onderzoek, maar op basis van de beschikbare retrospectieve cohortonderzoeken kunnen we niet met zekerheid concluderen dat anesthesie schadelijk is voor jonge kinderen. Ouders van jonge kinderen die moeten worden geopereerd, chirurgen en anesthesiologen hebben op korte termijn behoefte aan duidelijke antwoorden, maar het duurt nog enkele jaren voordat de resultaten van de GAS-studie bekend zullen worden. Andere RCT’s zijn nog niet gestart.
Op basis van het beschikbare onderzoek zijn 2 strategieën mogelijk. De ene optie is wachten met een verandering van beleid totdat er klinisch bewijs is voor neurotoxiciteit bij jonge kinderen; kleine interventies en diagnostische procedures kunnen nog steeds onder algehele anesthesie plaatsvinden. De andere optie is om op voorhand rekening te houden met toekomstig bewijs voor neurotoxische gevolgen van anesthesie. Het mogelijke risico van anesthesie wordt dan bij de indicatiestelling voor iedere operatie en ook voor de timing van de procedure meegewogen.
In de praktijk zal de laatste strategie er op neerkomen dat bij zeer jonge kinderen alleen ingrepen onder algehele anesthesie worden verricht voor levensbedreigende problemen of voor afwijkingen die zonder tijdige correctie tot ernstige functionele beperkingen zullen leiden. Voorbeelden van ingrepen die niet uitgesteld kunnen worden zijn correctie van ernstige, al dan niet congenitale, afwijkingen zoals hernia diaphragmatica, anorectale malformaties, buikwanddefecten, pylorushypertrofie en liesbreuken. De meerwaarde van adenoïdectomie vanwege recidiverende bovensteluchtweginfecties bij kinderen onder de 3 jaar is niet aangetoond.15 Hier lijkt het dan ook verstandig op zijn minst terughoudend te zijn met vroeg opereren.
Het argument dat ouders niet ‘nodeloos’ ongerust mogen worden gemaakt, past niet in een moderne arts-patiëntrelatie. Ouders moeten eerlijke informatie krijgen over de te verwachten gezondheidswinst en de risico’s van een procedure. Als er twijfel bestaat over de noodzaak van een operatie of diagnostische procedure onder algehele anesthesie op zeer jonge leeftijd, zouden operateur en anesthesioloog dit dilemma niet alleen met elkaar moeten bespreken, maar ook aan de ouders moeten voorleggen.
Literatuur
Rappaport B, Mellon RD, Simone A, Woodcock J. Defining safe use of anesthesia in children. N Engl J Med. 2011;364:1387-90 Medline. doi:10.1056/NEJMp1102155
Wilder RT, Flick RP, Sprung J, et al. Early exposure to anesthesia and learning disabilities in a population-based birth cohort. Anesthesiology. 2009;110:796-804 Medline. doi:10.1097/01.anes.0000344728.34332.5d
DiMaggio C, Sun LS, Li G. Early childhood exposure to anesthesia and risk of developmental and behavioral disorders in a sibling birth cohort. Anesth Analg. 2011;113:1143-51 Medline. doi:10.1213/ANE.0b013e3182147f42
Flick RP, Katusic SK, Colligan RC, et al. Cognitive and behavioral outcomes after early exposure to anesthesia and surgery. Pediatrics. 2011;128:e1053-e61 Medline. doi:10.1542/peds.2011-0351
Jevtovic-Todorovic V. General anesthetics and the developing brain: friends or foes? J Neurosurg Anesthesiol. 2005;17:204-6 Medline. doi:10.1097/01.ana.0000178111.26972.16
Patel P, Sun L. Update on neonatal anesthetic neurotoxicity: insight into molecular mechanisms and relevance to humans. Anesthesiology. 2009;110:703-8 Medline. doi:10.1097/ALN.0b013e31819c42a4
Head BP, Patel HH, Niesman IR, Drummond JC, Roth DM, Patel PM. Inhibition of p75 neurotrophin receptor attenuates isoflurane-mediated neuronal apoptosis in the neonatal central nervous system. Anesthesiology. 2009;110:813-25 Medline. doi:10.1097/ALN.0b013e31819b602b
Sun L. Early childhood general anaesthesia exposure and neurocognitive development. Br J Anaesth. 2010;105 Suppl 1:i61-8.Medline
Loepke AW, Soriano SG. An assessment of the effects of general anesthetics on developing brain structure and neurocognitive function. Anesth Analg. 2008;106:1681-707 Medline. doi:10.1213/ane.0b013e318167ad77
Davidson AJ. Anesthesia and neurotoxicity to the developing brain: the clinical relevance. Paediatr Anaesth. 2011;21:716-21 Medline. doi:10.1111/j.1460-9592.2010.03506.x
Brambrink AM, Evers AS, Avidan MS, et al. Isoflurane-induced neuroapoptosis in the neonatal rhesus macaque brain. Anesthesiology. 2010;112:834-41 Medline. doi:10.1097/ALN.0b013e3181d049cd
Laing S, Spence K, McMahon C, Ungerer J, Badawi N. Challenges in conducting prospective research of developmentally directed care in surgical neonates: a case study. Early Hum Dev. 2012;88:171-8 Medline.
Hansen TG, Pedersen JK, Henneberg SW, et al. Academic performance in adolescence after inguinal hernia repair in infancy: a nationwide cohort study. Anesthesiology. 2011;114:1076-85 Medline. doi:10.1097/ALN.0b013e31820e77a0
Bartels M, Althoff RR, Boomsma DI. Anesthesia and cognitive performance in children: no evidence for a causal relationship. Twin Res Hum Genet. 2009;12:246-53 Medline. doi:10.1375/twin.12.3.246
Van den Aardweg MT, Boonacker CW, Rovers MM, Hoes AW, Schilder AG. Effectiveness of adenoidectomy in children with recurrent upper respiratory tract infections: open randomised controlled trial. BMJ. 2011;343:d5154 Medline. doi:10.1136/bmj.d5154





Wat betekent dit?! Anesthesie bij kinderen schadelijk
Artikelinhoud werd al langer (zonder echte consequenties) bediscussieerd, nu het in het NTvG is verschenen welhaast nog actueler! Hoe gaan we hiermee om? De eerste narcose bij een kind lijkt (...) nog geen onoverkomelijke consequenties te veroorzaken, daarna wordt het moeilijker. De kleine KNO-chirurgie als MOD's en AT-en lijkt hiermee minder 'aantrekkelijk' en we zullen met het onzekere gevoel dat we als anesthesisten mogelijk ook schadelijk bezig zijn bij andere (meer acute) ingrepen moeten leren leven.
Interessant blijft de vraag waar de leeftijdsgrens wordt gelegd waaronder problemen zouden kunnen worden verwacht, dwz wat is safe?!
George Moor, anesthesioloog, Tergooiziekenhuizen