Samenvatting
-
‘Acute nierschade’ is de moderne term voor een plotseling verslechterde nierfunctie en deze wordt gedefinieerd aan de hand van de RIFLE-classificatie (RIFLE staat voor ‘risk’, ‘injury’, ‘failure’, ‘loss’ en ‘end-stage kidney disease’).
-
Acute nierschade ontstaat door een combinatie van verminderde doorbloeding van de nier, systemische ontsteking en toediening van nefrotoxische geneesmiddelen.
-
Patiënten met chronische nierschade, hoge leeftijd, diabetes mellitus of hartfalen hebben een verhoogd risico op acute nierschade.
-
Op korte termijn leidt acute nierschade tot een sterk verhoogd risico op overlijden; op lange termijn veroorzaakt acute nierschade permanent verlies van de renale microcirculatie, waardoor chronische nierziekte kan ontstaan.
-
Biomarkers in de urine bieden nieuwe mogelijkheden om acute nierschade in een vroeg stadium te detecteren.
-
De huidige behandeling van patiënten met acute nierschade is ondersteunend van aard; Hemodynamische optimalisatie van patiënten leidt tot vermindering van acute nierschade rondom grote chirurgische ingrepen.
-
Een veelbelovende behandeling ter preventie van acute nierschade is ‘remote ischaemic preconditioning’.
artikel
Er zijn 2 belangrijke ontwikkelingen geweest in het afgelopen decennium die verandering hebben gebracht in de benadering van patiënten met een acuut verminderde nierfunctie. Ten eerste is door internationale experts consensus bereikt over de introductie en de definiëring van de term ‘acute nierschade’.1 Ten tweede blijkt dat een beperkte toename van de serumcreatinineconcentratie bij patiënten het mortaliteitsrisico vergroot.2
Deze nieuwe ontwikkelingen worden in dit overzichtsartikel toegelicht. Daarnaast wordt recent onderzoek naar vroegdiagnostiek en behandeling van acute nierschade besproken. We hopen hiermee het fenomeen onder de aandacht te brengen bij een breed medisch publiek.
Definitie van ‘acute nierschade’
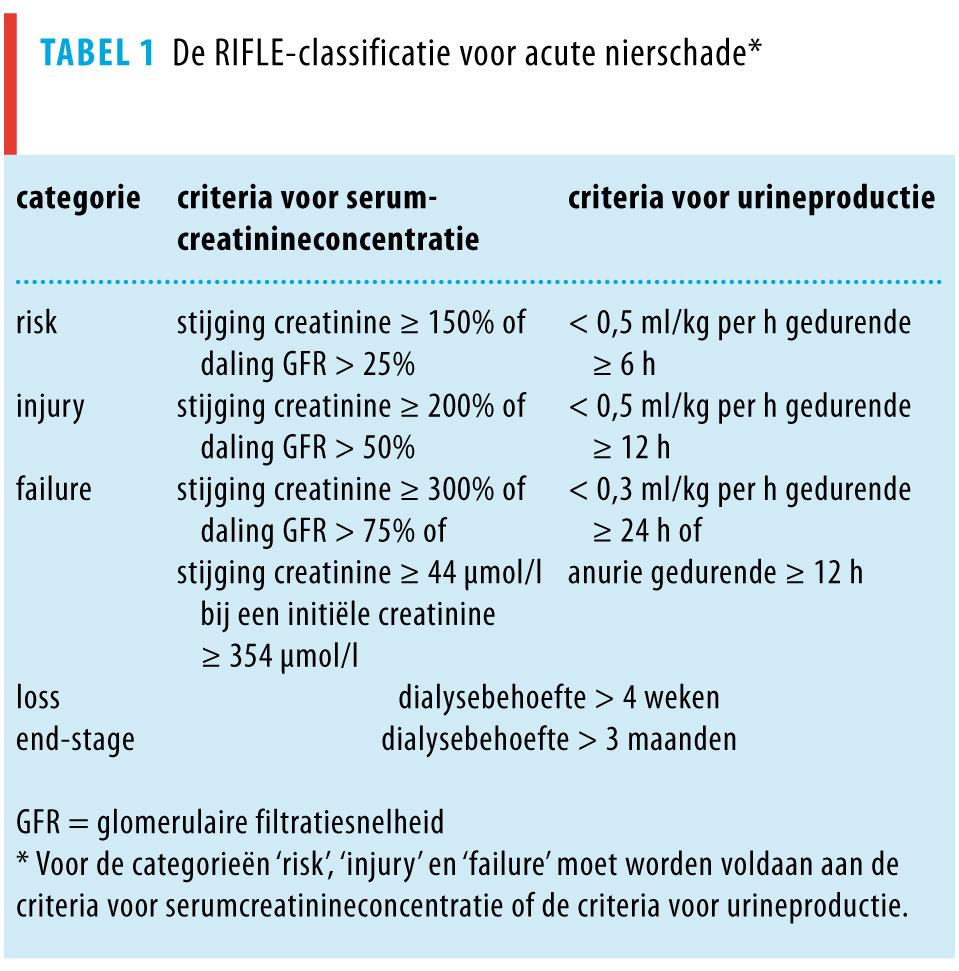
‘Acute nierschade’ is de moderne term voor een plotseling verslechterde nierfunctie. Tot voor kort liep de definitie van acute nierschade sterk uiteen; in de literatuur waren wel 35 verschillende definities in omloop. Hierdoor ontstonden grote variaties in schattingen van de incidentie en mortaliteit van deze aandoening. Deze impasse werd doorbroken met de introductie van de RIFLE-classificatie vanuit het Acute Dialysis Quality Initiative, waarbij RIFLE staat voor ‘risk’, ‘injury’, ‘failure’, ‘loss’ en ‘end-stage kidney disease’ (tabel 1).1 Deze classificatie definieert de aanwezigheid en de ernst van acute nierschade op basis van de toename van de serumcreatinineconcentratie en de afname van de urineproductie. De RIFLE-classificatie werd gevalideerd bij duizenden patiënten en is in korte tijd uitgegroeid tot een gevestigd classificatiesysteem. We zullen in dit overzichtsartikel dan ook alleen publicaties bespreken waarin acute nierschade volgens de RIFLE-classificatie wordt gedefinieerd.
Incidentie en risicofactoren
Op basis van de RIFLE-classificatie wordt de incidentie van acute nierschade in de algemene populatie geschat op 2 per 1000 inwoners per jaar.3 De incidentie bij patiënten die worden opgenomen in het ziekenhuis is 18% per opname.4 Op de IC wordt de hoogste prevalentie gezien: 22-36% van de patiënten voldoet tijdens het verblijf op de IC aan de criteria van acute nierschade en bij 4-12% van deze patiënten is dialyse noodzakelijk.5,6 Patiënten met chronische nierschade, hoge leeftijd, diabetes mellitus of hartfalen hebben een verhoogd risico op het ontwikkelen van acute nierschade.6
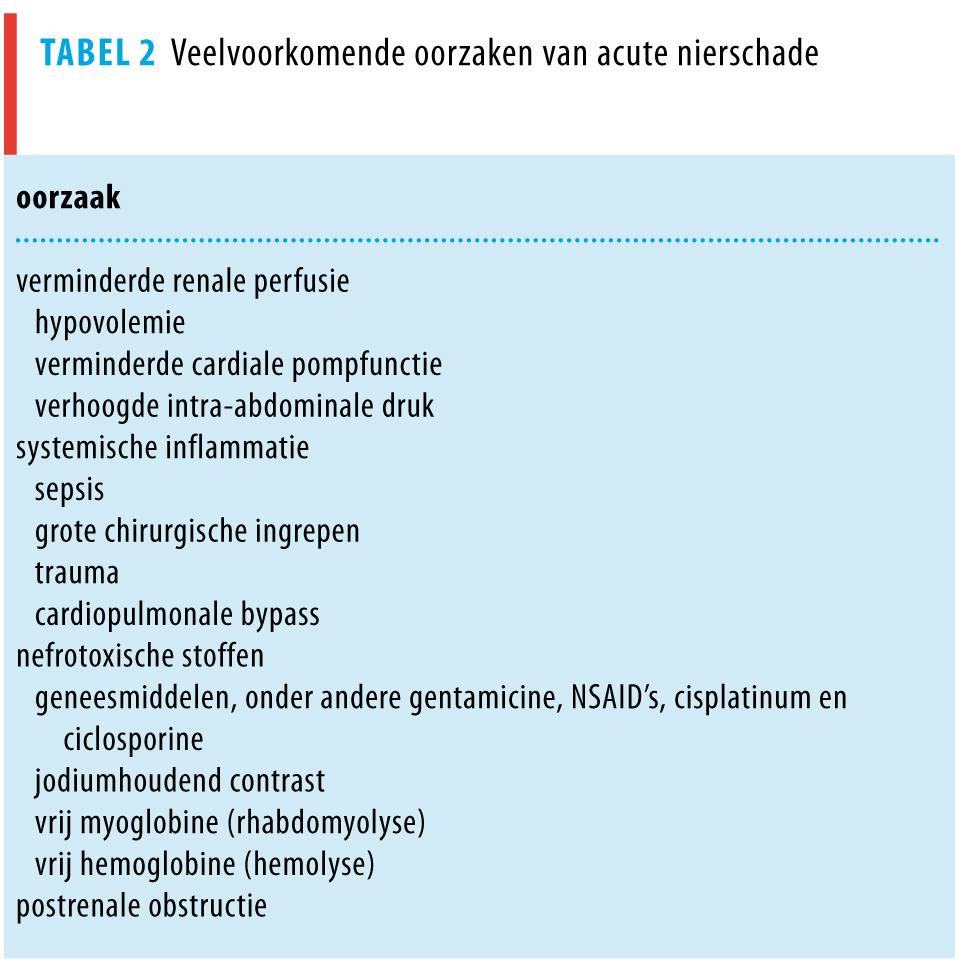
De oorzaak van acute nierschade bij patiënten op de IC is gewoonlijk multifactorieel. Bij deze ernstig zieke patiënten ontwikkelt acute nierschade zich uit een combinatie van verminderde renale perfusie, systemische inflammatie en toediening van nefrotoxische stoffen. Veelvoorkomende oorzaken van acute nierschade zijn samengevat in tabel 2. Bespreking van de pathofysiologie en een uiteenzetting van specifieke oorzaken van acute nierschade, zoals acute glomerulonefritis en acute interstitiële nefritis, vallen buiten het bestek van dit artikel en kunnen worden gevonden in een ander overzichtsartikel.7
Op basis van deze predisponerende factoren zou men verwachten dat acute nierschade frequent voorkomt bij patiënten die een grote chirurgische ingreep ondergaan. Inderdaad blijkt dat 15% van de patiënten na een hartoperatie acute nierschade ontwikkelt en dat een derde van deze patiënten wordt gedialyseerd.8 Deze dialysebehoefte kan preoperatief worden voorspeld met behulp van een eenvoudige risicoscore.9 Er is veel minder bekend over de incidentie na algemeen chirurgische ingrepen. Op basis van de resultaten van het enige beschikbare onderzoek – dat weliswaar beperkt is door onduidelijke inclusie van patiënten en door exclusie van patiënten met chronische nierschade – wordt geschat dat 8% van de patiënten na een grote operatie acute nierschade ontwikkelt.10
Gevolgen van acute nierschade
Het is al lang bekend dat acuut nierfalen met dialysebehoefte gepaard gaat met een hoge mortaliteit. In de afgelopen jaren is echter ontdekt dat ook een geringe verslechtering van de nierfunctie samengaat met een slechte prognose op korte en lange termijn.
Op korte termijn hebben patiënten met acute nierschade een sterk verhoogd risico op overlijden tijdens de ziekenhuisopname. Dit risico neemt toe met de ernst van de schade volgens de RIFLE-classificatie: patiënten in de categorie ‘risk’ hebben 2,4 maal zoveel kans om te overlijden als patiënten zonder acute nierschade, terwijl deze kans voor patiënten in de categorie ‘injury’ 4,2 en voor patiënten in de categorie ‘failure’ 6,4 maal zo groot is.11 Dit is de reden waarom de term ‘acute nierschade’ de voorkeur heeft boven de traditionele benaming ‘acuut nierfalen’, die ten onrechte impliceert dat alleen volledig verlies van de nierfunctie met dialysebehoefte van belang is voor patiënten.
Na herstel van acute nierschade keert de nierfunctie meestal terug naar de uitgangssituatie. Hierdoor bestond lange tijd de indruk dat acute nierschade een tijdelijk probleem is zonder consequenties op de lange termijn. Onderzoek bij proefdieren toont echter aan dat de aandoening permanent verlies van de renale microcirculatie veroorzaakt, waardoor op lange termijn atrofie en fibrose van het nierweefsel kan ontstaan.12 In overeenstemming met deze resultaten laat epidemiologisch onderzoek zien dat patiënten ook na volledig herstel van acute nierschade een verhoogd risico op chronische nierschade en mortaliteit hebben ten opzichte van vergelijkbare patiënten zonder acute nierschade.13 Acute nierschade veroorzaakt dus blijvende veranderingen in de nier, waarvan patiënten ook op lange termijn nadeel ondervinden.
Vroegdiagnostiek
Bij acute vermindering van de nierfunctie duurt het enige tijd voordat de serumcreatinineconcentratie zodanig is gestegen dat de patiënt voldoet aan de criteria van acute nierschade volgens de RIFLE-classificatie. Dit betekent dat vaak pas enkele dagen na het uitlokkende moment kan worden vastgesteld dat acute nierschade heeft plaatsgevonden. Hierdoor is vroegtijdige interventie niet mogelijk. Om deze reden werd in het afgelopen decennium veel onderzoek verricht naar biomarkers waarmee acute nierschade in een vroeger stadium ontdekt kan worden.
Traditioneel wordt in de urine de fractionele excretie van natrium bepaald en kan een microscopische analyse van het urinesediment worden verricht.14 Het meten van de urine-excretie van natrium of ureum kan bijdragen aan de differentiatie tussen verschillende oorzaken van acute nierschade. Recent werd aangetoond dat de hoeveelheid korrelcylinders en tubulaire epitheelcellen in de urine de ernst en de progressie van acute nierschade voorspelt.15 De diagnostische waarde van deze bepalingen bij de vroegtijdige detectie is echter onbekend. Toch blijft analyse van het urinesediment onontbeerlijk voor het aantonen van specifieke oorzaken, zoals acute glomerulonefritis.
De nieuwe biomarkers voor acute nierschade kunnen worden ingedeeld in 3 groepen: (a) eiwitten die gewoonlijk aanwezig zijn in het nierweefsel en bij celdood in de urine terechtkomen; (b) eiwitten die nieuw geproduceerd en uitgescheiden worden door het nierweefsel als reactie op acute nierschade; (c) plasma-eiwitten die na glomerulaire filtratie normaliter door het nierweefsel worden geresorbeerd, maar bij verminderde nierfunctie in de urine worden uitgescheiden. Veelbelovende biomarkers die in de urine bepaald kunnen worden, zijn ‘neutrophil gelatinase associated lipocalin’ (NGAL), interleukine 18 (IL-18), ‘kidney injury molecule 1’ (KIM-1) en in mindere mate ‘liver fatty acid binding protein’ (L-FABP), ‘retinol binding protein’ (RBP) en albumine.16
De diagnostische waarde van de diverse biomarkers voor acute nierschade is moeilijk onderling te vergelijken, omdat de markers in verschillende klinische situaties zijn gemeten. Bovendien zijn de meeste biomarkers niet gevalideerd in een groot patiëntencohort en is slechts voor enkele markers een sneltest beschikbaar. Ten slotte is het onduidelijk of een positieve testuitslag consequenties heeft voor de behandeling van patiënten. Om deze redenen hebben dergelijke biomarkers voor vroegdiagnostiek naar acute nierschade nog geen plaats verworven in de dagelijkse praktijk.
Behandelmogelijkheden
De huidige behandeling van patiënten met acute nierschade is ondersteunend van aard, waarbij progressie van het nierfunctieverlies moet worden voorkomen.17,18 Het is belangrijk om de vullingstoestand van deze patiënten te optimaliseren door adequate resuscitatie zonder dat daarbij de patiënt overvuld raakt. Wanneer patiënten onvoldoende reageren op de intraveneuze vochttoediening kan het nodig zijn om hen te behandelen met vasopressoren of inotropica, waarbij meestal een gemiddelde bloeddruk (‘mean arterial pressure’) van minimaal 65 mmHg wordt nagestreefd. Daarnaast dient obstructie van de urinewegen als oorzaak te worden uitgesloten met echografisch onderzoek. Ten slotte moet toediening van medicatie die bijdraagt aan acute nierschade worden vermeden en dient eventuele sepsis adequaat te worden behandeld met antibiotica en drainage van mogelijk aanwezige puscollecties. Een dilemma ontstaat wanneer de toediening van nefrotoxische antibiotica zoals gentamicine voor de behandeling van een infectie leidt tot progressie van de nierschade. Indien geen alternatieve antibiotica voor handen zijn, moeten de voor- en nadelen van de behandeling per patiënt worden afgewogen.
Vaak wordt de indicatie voor dialyse gesteld wanneer de nierfunctie ondanks deze maatregelen zodanig verslechtert dat hyperkaliëmie, metabole acidose of overvulling een gevaar vormen voor de patiënt. Een bespreking van de optimale vorm van dialyse, de dosis en het moment waarop dialyse gestart moet worden in het kader van acute nierschade valt buiten het bestek van dit artikel, maar kan worden gevonden in een recente meta-analyse.19
Een verscheidenheid aan RCT’s heeft het effect bestudeerd van medicamenteuze interventies op de nierfunctie rondom grote chirurgische ingrepen. Een meta-analyse van deze onderzoeken laat zien dat geen enkele behandeling – inclusief dopamine, diuretica, calciumblokkers en ACE-remmers – bewezen effectief is voor de preventie van acute nierschade.20
Preventiemogelijkheden
In tegenstelling tot het teleurstellende preventieve effect van farmacologische interventies leidt hemodynamische optimalisatie rondom grote chirurgische ingrepen wel tot significante vermindering van acute nierschade.21 Bij hemodynamische optimalisatie worden de vullingstoestand en cardiac output van patiënten gemeten, meestal met behulp van Swan-Ganz-katheters of oesofageaal Doppler-onderzoek. Deze parameters worden vervolgens met infusievloeistof en inotropica bijgestuurd totdat niet-afwijkende waarden zijn verkregen. Het meten van de variatie in polsdruk bij beademde patiënten maakt het mogelijk om te voorspellen of extra vochttoediening zal leiden tot een verhoging van de cardiac output.22 Hierdoor kan het risico op overvulling worden beperkt.
Een veelbelovende behandeling ter preventie van acute nierschade is ‘remote ischaemic preconditioning’.23 Deze behandeling bestaat uit het induceren van kortdurende ischemie en reperfusie in een ledemaat, waardoor afgelegen organen zoals hart, nieren en hersenen worden beschermd tegen langdurige ischemie. Het precieze werkingsmechanisme van remote ischaemic preconditioning is nog niet opgehelderd. Uit onderzoek met proefdieren blijkt dat zowel circulerende stoffen die vanuit het ischemische weefsel vrijkomen als stimulatie van zenuwen door ischemie en reperfusie een belangrijke rol spelen.23 De behandeling lijkt geen belangrijke risico’s te kennen en is vrijwel kosteloos; het nadeel is dat het tijdstip van het uitlokkende moment bekend moet zijn om preconditioning op voorhand te kunnen toedienen.
Uit verschillende RCT’s blijkt dat remote ischaemic preconditioning het risico op acute nierschade na een hartoperatie significant vermindert.24 Momenteel worden grote RCT’s uitgevoerd om de resultaten van deze relatief kleine onderzoeken te bevestigen en om te bestuderen of preventie van acute nierschade zich vertaalt in een lagere mortaliteit.
Conclusie
Er hebben zich in het afgelopen decennium belangrijke ontwikkelingen voorgedaan in de benadering van patiënten met acute verslechtering van de nierfunctie. Er is consensus bereikt over de term ‘acute nierschade’ en de definitie hiervan. Verder is bekend geworden dat een beperkte toename van de serumcreatinineconcentratie al leidt tot een sterk verhoogd mortaliteitsrisico tijdens een ziekenhuisopname. Op het gebied van vroegdiagnostiek, behandeling en preventie moet nog veel onderzoek worden gedaan voordat nieuwe methoden kunnen worden geïmplementeerd in de dagelijkse praktijk. Zo moet de diagnostische waarde van diverse biomarkers voor acute nierschade die in de urine kunnen worden bepaald, worden vastgesteld in een groot patiëntencohort. Bovendien moet in grote RCT’s worden bepaald of veelbelovende behandelingen zoals ‘remote ischaemic preconditioning’ leiden tot preventie van acute nierschade en tot vermindering van de mortaliteit na grote chirurgische ingrepen. In de tussentijd is de therapie beperkt en slechts ondersteunend van aard.
Leerpunten
-
‘Acute nierschade’ is een plotseling verslechterde nierfunctie; sinds enkele jaren is hier een heldere en algemeen geaccepteerde definitie voor op basis van classificatiecriteria.
-
Op de IC wordt de hoogste prevalentie van acute nierschade gezien; er is echter minder bekend over de incidentie van acute nierschade na algemeen chirurgische ingrepen.
-
Zowel acuut nierfalen met dialysebehoefte als een geringe verslechtering van de nierfunctie gaan gepaard met een slechte prognose op korte en lange termijn.
-
De waarde van biomarkers in de urine voor de vroegdiagnostiek van acute nierschade moet nog worden vastgesteld.
-
Farmacologische behandeling ter preventie van acute nierschade leidt tot teleurstellende resultaten.
-
Hemodynamische optimalisatie en ‘remote ischaemic preconditioning’ zijn veelbelovende interventies ter preventie van acute nierschade na een hartoperatie.
Literatuur
Bellomo R, Ronco C, Kellum JA, Mehta RL, Palevsky P. Acute renal failure – definition, outcome measures, animal models, fluid therapy and information technology needs: the Second International Consensus Conference of the Acute Dialysis Quality Initiative (ADQI) Group. Crit Care. 2004;8:R204-12 Medline. doi:10.1186/cc2872
Chertow GM, Burdick E, Honour M, Bonventre JV, Bates DW. Acute kidney injury, mortality, length of stay, and costs in hospitalized patients. J Am Soc Nephrol. 2005;16:3365-70 Medline. doi:10.1681/ASN.2004090740
Ali T, Khan I, Simpson W, Prescott G, Townend J, Smith W, et al. Incidence and outcomes in acute kidney injury: a comprehensive population-based study. J Am Soc Nephrol. 2007;18:1292-8 Medline. doi:10.1681/ASN.2006070756
Uchino S, Bellomo R, Goldsmith D, Bates S, Ronco C. An assessment of the RIFLE criteria for acute renal failure in hospitalized patients. Crit Care Med. 2006;34:1913-7 Medline. doi:10.1097/01.CCM.0000224227.70642.4F
Ostermann M, Chang RW. Acute kidney injury in the intensive care unit according to RIFLE. Crit Care Med. 2007;35:1837-43.
Thakar CV, Christianson A, Freyberg R, Almenoff P, Render ML. Incidence and outcomes of acute kidney injury in intensive care units: a Veterans Administration study. Crit Care Med. 2009;37:2552-8 Medline. doi:10.1097/CCM.0b013e3181a5906f
Bellomo R, Kellum JA, Ronco C. Acute kidney injury. Lancet. 2012;380:756-66 Medline. doi:10.1016/S0140-6736(11)61454-2
Heringlake M, Knappe M, Vargas Hein O, Lufft H, Kindgen-Milles D, Böttiger BW, et al. Renal dysfunction according to the ADQI-RIFLE system and clinical practice patterns after cardiac surgery in Germany. Minerva Anestesiol. 2006;72:645-54 Medline.
Wijeysundera DN, Karkouti K, Dupuis JY, Rao V, Chan CT, Granton JT, et al. Derivation and validation of a simplified predictive index for renal replacement therapy after cardiac surgery. JAMA. 2007;297:1801-9 Medline. doi:10.1001/jama.297.16.1801
Abelha FJ, Botelho M, Fernandes V, Barros H. Determinants of postoperative acute kidney injury. Crit Care. 2009;13:R79 Medline. doi:10.1186/cc7894
Ricci Z, Cruz D, Ronco C. The RIFLE criteria and mortality in acute kidney injury: A systematic review. Kidney Int. 2008;73:538-46 Medline. doi:10.1038/sj.ki.5002743
Basile DP, Donohoe D, Roethe K, Osborn JL. Renal ischemic injury results in permanent damage to peritubular capillaries and influences long-term function. Am J Physiol Renal Physiol. 2001;281:F887-99 Medline.
Bucaloiu ID, Kirchner HL, Norfolk ER, Hartle JE II, Perkins RM. Increased risk of death and de novo chronic kidney disease following reversible acute kidney injury. Kidney Int. 2012;81:477-85 Medline. doi:10.1038/ki.2011.405
Perazella MA, Coca SG. Traditional urinary biomarkers in the assessment of hospital-acquired AKI. Clin J Am Soc Nephrol. 2012;7:167-74 Medline. doi:10.2215/CJN.09490911
Perazella MA, Coca SG, Hall IE, Iyanam U, Koraishy M, Parikh CR. Urine microscopy is associated with severity and worsening of acute kidney injury in hospitalized patients. Clin J Am Soc Nephrol. 2010;5:402-8 Medline. doi:10.2215/CJN.06960909
Siew ED, Ware LB, Ikizler TA. Biological markers of acute kidney injury. J Am Soc Nephrol. 2011;22:810-20 Medline. doi:10.1681/ASN.2010080796
Borthwick E, Ferguson A. Perioperative acute kidney injury: risk factors, recognition, management, and outcomes. BMJ. 2010;341:c3365 Medline. doi:10.1136/bmj.c3365
Brochard L, Abroug F, Brenner M, Broccard AF, Danner RL, Ferrer M, et al. An Official ATS/ERS/ESICM/SCCM/SRLF Statement: Prevention and Management of Acute Renal Failure in the ICU Patient: an international consensus conference in intensive care medicine. Am J Respir Crit Care Med. 2010;181:1128-55 Medline. doi:10.1164/rccm.200711-1664ST
Pannu N, Klarenbach S, Wiebe N, Manns B, Tonelli M. Renal replacement therapy in patients with acute renal failure: a systematic review. JAMA. 2008;299:793-805 Medline. doi:10.1001/jama.299.7.793
Zacharias M, Conlon NP, Herbison GP, Sivalingam P, Walker RJ, Hovhannisyan K. Interventions for protecting renal function in the perioperative period. Cochrane Database Syst Rev. 2008;(4):CD003590 Medline.
Brienza N, Giglio MT, Marucci M, Fiore T. Does perioperative hemodynamic optimization protect renal function in surgical patients? A meta-analytic study. Crit Care Med. 2009;37:2079-90 Medline. doi:10.1097/CCM.0b013e3181a00a43
Marik PE, Cavallazzi R, Vasu T, Hirani A. Dynamic changes in arterial waveform derived variables and fluid responsiveness in mechanically ventilated patients: a systematic review of the literature. Crit Care Med. 2009;37:2642-7 Medline. doi:10.1097/CCM.0b013e3181a590da
Kharbanda RK, Nielsen TT, Redington AN. Translation of remote ischaemic preconditioning into clinical practice. Lancet. 2009;374:1557-65 Medline. doi:10.1016/S0140-6736(09)61421-5
Zimmerman RF, Ezeanuna PU, Kane JC, Cleland CD, Kempananjappa TJ, Lucas FL, et al. Ischemic preconditioning at a remote site prevents acute kidney injury in patients following cardiac surgery. Kidney Int. 2011;80:861-7 Medline. doi:10.1038/ki.2011.156




Reacties