Dit artikel is een actualisatie van een eerder verschenen leerartikel Lymfadenopathie in de eerste lijn (D4901). In de rubriek ‘Leerartikel’ beantwoorden experts veelvoorkomende vragen over een bepaald onderwerp. Test je kennis met de onlinetoets.
Op de hoogte blijven van nieuwe leerartikelen, compleet met geaccrediteerde toetsvragen en luisterversie?
⚡Schrijf je gratis in op een e-mail alert door het dossier Leerartikelen te volgen.⚡
In de rubriek ‘Leerartikel’ beantwoorden experts veelvoorkomende vragen over een bepaald onderwerp. Test je kennis met de onlinetoets.
Toets voor nascholing (verlopen)
Aan dit artikel was een toets gekoppeld waarmee je nascholingspunten kon verdienen.
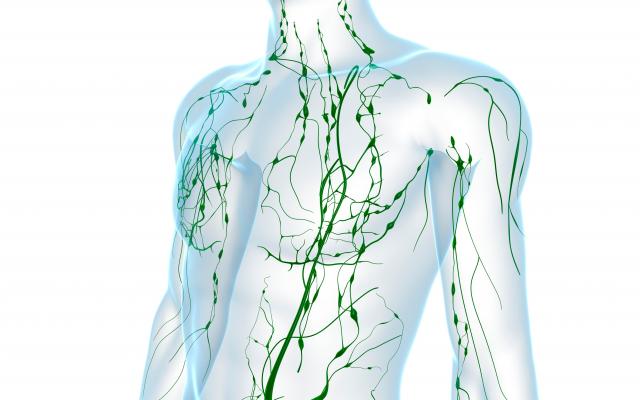
Lymfadenopathie komt vrij frequent voor in Nederland; een huisarts ziet gemiddeld eens per maand een patiënt met deze klacht.1,2 Er is sprake van lymfadenopathie bij pijn of toegenomen grootte van één of meer lymfeklieren; we spreken van vergrote lymfeklieren bij een diameter van > 2 cm voor klieren in de lies en van > 1 cm voor lymflieren op andere locaties.3,4
Lymfadenopathie is een aspecifieke bevinding met een brede differentiaaldiagnose, die afhankelijk is van patiëntgerelateerde factoren als leeftijd, voorgeschiedenis, comorbiditeit en leefstijl. Ook het klinisch beeld en eventuele begeleidende symptomen hebben een sterke invloed op de volgorde van de differentiaaldiagnose.5 Bij het opstellen van de differentiaaldiagnose helpt het om onderscheid te maken in de lokalisatie (lokaal vs. gegeneraliseerd; welk lymfeklierstation?) en in het beloop of de dynamiek (acuut vs. chronisch).
Classificatie van lymfadenopathie
Lokale lymfadenopathie Hierbij is één lymfeklier of een groep lymfeklieren (klierstation) afwijkend. In de…
Luisterversie
Het audiobestand van dit artikel is alleen toegankelijk voor abonnees. Log in om het artikel te beluisteren.
Inloggen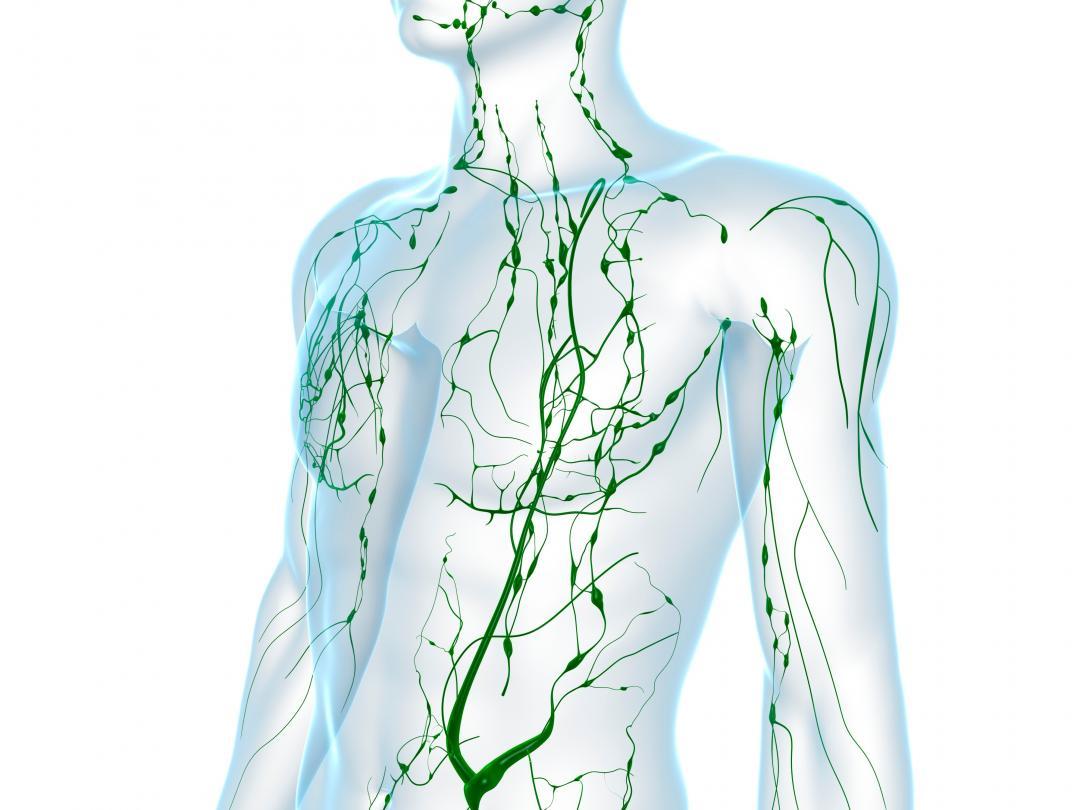


Reacties