Samenvatting
Achtergrond
Thyreotoxische hypokaliëmische periodieke paralyse (THPP) is een zeldzaam en in potentie levensgevaarlijk ziektebeeld. Dit treft voornamelijk mannen van Oost-Aziatische afkomst en is zelden beschreven bij blanke personen.
Casus
Een 34-jarige, Nederlandse man, bekend met de ziekte van Graves, presenteerde zich met krachtverlies in de onderste extremiteiten. Het laboratoriumonderzoek toonde ernstige hypokaliëmie (1,8 mmol/l) en een verhoogde creatinekinasewaarde. Het elektrocardiogram liet atriumfibrilleren zien met een verlengd QTc-interval. Patiënt werd opgenomen met ritmebewaking en kreeg kaliumsuppletie. Laboratoriumonderzoek van de schildklierfunctie toonde thyreotoxicose. Patiënt kreeg propranolol en thiamazol. Bij follow-up waren de schildklierfunctie, de kaliumconcentratie en de spierkracht genormaliseerd.
Conclusie
Bij onbegrepen paralyse moet gedacht worden aan hypokaliëmie als manifestatie van thyreotoxicose. De behandeling van THPP bestaat uit behandeling van hyperthyreoïdie met daaraan toegevoegd propranolol. Aangezien de hypokaliëmie zelflimiterend is, is kaliumsuppletie slechts noodzakelijk bij ritme- of geleidingsstoornissen. Ondanks adequate behandeling bestaat er een risico op recidief. Regelmatige controle is geïndiceerd totdat euthyreoïdie bereikt is.
Leerdoelen
- Thyreotoxische hypokaliëmische periodieke paralyse (THPP) is een zeldzame aandoening, die potentieel dodelijk is vanwege hartritmestoornissen.
- THPP komt met name voor bij mannen van Aziatische afkomst, maar is ook beschreven bij blanke mannen.
- Onbegrepen, bilaterale parese of paralyse in vooral de onderste extremiteiten kan een uiting zijn van hypokaliëmie op basis van thyreotoxicose.
- De hypokaliëmie bij THPP is zelflimiterend, daarom is suppletie van kalium alleen geïndiceerd bij hartritme- of geleidingsstoornissen; dan is frequente serum-kalium-controle aangewezen.
- De behandeling van THPP bestaat uit de behandeling van hyperthyreoïdie met daaraan toegevoegd propranolol.
- Ondanks adequate behandeling is er een grote kans op recidief van THPP in de eerste 3 maanden.
artikel
Inleiding
Thyreotoxische hypokaliëmische periodieke paralyse (THPP) is een zeldzaam ziektebeeld en in potentie levensgevaarlijk, omdat het risico geeft op 'sudden unexplained nocturnal death'. THPP is slechts zelden beschreven bij blanke personen. Een snelle behandeling van de thyreotoxicose in combinatie met een bètablokker is geïndiceerd. In dit artikel beschrijven wij een Nederlandse man met THPP als uiting van de ziekte van Graves.
Ziektegeschiedenis
Patiënt A, een 34-jarige, Nederlandse man, bezocht op de SEH de neuroloog. Hij had krachtverlies, voornamelijk in de bovenbenen, waarbij opstaan en lopen onmogelijk waren. Dit was in enkele uren tijd ontstaan. Een soortgelijke aanval van spierzwakte had patiënt enkele weken eerder ondervonden, toen was hij spontaan hersteld na een paar uur rust. Patiënt had geen bewustzijnsverlies, sensibiliteitsverlies of aanwijzingen voor een epileptisch insult. Bij neurologisch onderzoek vond de neuroloog milde algehele spierzwakte van de benen (parese MRC-graad 4), beiderzijds niet-afwijkende reflexen en een forse tremor. Omdat deze bevindingen meer in de richting wezen van een internistische oorzaak werd patiënt overgedragen aan de internist.
Wij zagen een heldere, adequate man met een subjectief matige exoftalmus beiderzijds. Patiënt maakte een gejaagde indruk. Zijn bloeddruk was 190/87 mmHg en hij had irregulaire tachycardie (135 slagen/min) zonder koorts, maar met een klamme huid. De schildklier was bij palpatie rechts enigszins vergroot zonder noduli. Bij auscultatie van hart en longen werden irregulaire harttonen zonder souffles en vesiculair ademgeruis gehoord.
De medische voorgeschiedenis van patiënt vermeldde de ziekte van Graves. Hiervoor was hij 3 jaar eerder gedurende enkele maanden behandeld met propranolol en thiamazol. Op eigen initiatief was hij echter met deze behandeling gestopt en de schildklierfunctie was sindsdien ongecontroleerd gebleven. Patiënt vertelde ook dat hij al 6 maanden steeds meer gewichtsverlies had, ondanks toename van zijn eetlust. Daarnaast had hij klachten van warmte-intolerantie. Hij gebruikte nu geen medicatie.
Het laboratoriumonderzoek toonde ernstige hypokaliëmie (referentiewaarden tussen haakjes): 1,8 mmol/l (3,5-5,0) en een hoge creatinekinasewaarde: 1099 U/l (< 171). De ontstekingsparameters, nierfunctie, elektrolyten en de serumglucoseconcentratie waren niet-afwijkend. Bloedgasanalyse toonde een metabole acidose. Op de thoraxfoto werden geen afwijkingen gezien. Bij toxicologisch onderzoek werden geen afwijkingen gevonden. Naar aanleiding van de eerdere ziekte van Graves zetten wij aanvullend onderzoek in naar de schildklierfunctie. Het elektrocardiogram toonde atriumfibrilleren met een sterk verlengd QTc-interval (556 msec).
Patiënt werd opgenomen met hartritmebewaking onder de werkdiagnose 'atriumfibrilleren en hartritmegeleidingsstoornis bij hypokaliëmie'. Wij gaven patiënt intraveneuze kaliumsuppletie met 1 g kalium gedurende 2 x 15 min via een perfusorpomp, gevolgd door 2 g kalium in 500 cm3 infusievloeistof dat in 2 uur tijd werd toegediend. Vervolgens gaven wij orale kaliumsuppletie in de vorm van kaliumchloride 600 mg. Hiermee was het kaliumgehalte na 3 uur gestegen naar 5,0 mmol/l, een 'rebound-hyperkaliëmie'.
De volgende dag toonde het laboratoriumonderzoek van de schildklierfunctie een lage TSH-concentratie (0,01 mE/l; referentiewaarde: 0,40-4,0) en een verhoogde concentratie vrij T4 (58,2 pmol/l; referentiewaarde: 10,3-25,8). Dit duidde op thyreotoxicose. Op basis van deze bevindingen werd de diagnose 'thyreotoxische hypokaliëmische periodieke paralyse (THPP) bij onderbehandelde ziekte van Graves' gesteld. Patiënt kreeg propranolol 40 mg 3 dd en thiamazol 10 mg 3 dd. Gedurende de opname normaliseerde de kaliumconcentratie in het bloed, net als het elektrocardiogram. Tevens herstelde de spierkracht. Bij poliklinische follow-up was patiënt klachtenvrij en vertoonde de schildklierfunctie geen afwijkingen meer.
Beschouwing
THPP komt sporadisch voor bij patiënten met hyperthyreoïdie en treft voornamelijk mannen van Oost-Aziatische afkomst. De man-vrouwratio van deze aandoening is 20:1, ondanks de hogere incidentie van hyperthyreoïdie onder vrouwen. De incidentie van THPP bij hyperthyreoïdiepatiënten in China en Japan bedraagt 1,8-1,9%, terwijl de incidentie bij patiënten in andere landen slechts 0,1-0,2% is.1 Vaak ontbreken de typerende hyperthyreoïdie-verschijnselen omdat deze gelijktijdig met of kort na de manifestatie van de parese optreden.2
THPP wordt gekenmerkt door terugkerende aanvallen van bilaterale paralyse, voornamelijk van de onderste extremiteiten, en levensbedreigende aritmieën veroorzaakt door hypokaliëmie in combinatie met thyreotoxicose. Een dergelijk aanval ontstaat hoofdzakelijk 's nachts en geeft risico op 'sudden unexplained nocturnal death'. Een aanval kan worden uitgelokt door koolhydraatrijke voeding, rust na overmatige inspanning, stress en hyperinsulinemie.3,4
Pathofysiologie
De pathofysiologie van THPP is slechts gedeeltelijk bekend. Onder normale omstandigheden treedt contractie van de skeletspiercellen op door een actiepotentiaal over het celmembraan, die ontstaat via in- en efflux van natrium-, kalium- en calciumionen. Bij THPP worden de hypokaliëmie en de bijbehorende spierzwakte veroorzaakt door een verstoorde, snellere werking van de Na+/K+-ATPase-pomp op het celmembraan. Door overmatige stimulatie van de Na+/K+-ATPase-pomp ontstaat een toename van kaliuminflux, waardoor er een meer gehyperpolariseerde spiercelmembraan ontstaat. Dit geeft een verlaagd extracellulair K+-niveau. Op deze manier leidt de verstoorde werking van de Na+/K+-ATPase-pomp – en het gebrek aan compensatiemechanismen hiervoor – tot paradoxale depolarisatie (zie uitlegkader) en daardoor een verminderde actiepotentiaal. Dit veroorzaakt inactiviteit van de Na+-kanalen en uiteindelijk paralyse en aritmieën.1,2 De overmatige stimulatie van de Na+/K+-ATPase-pomp heeft diverse oorzaken, zoals te zien is in figuur 1.1
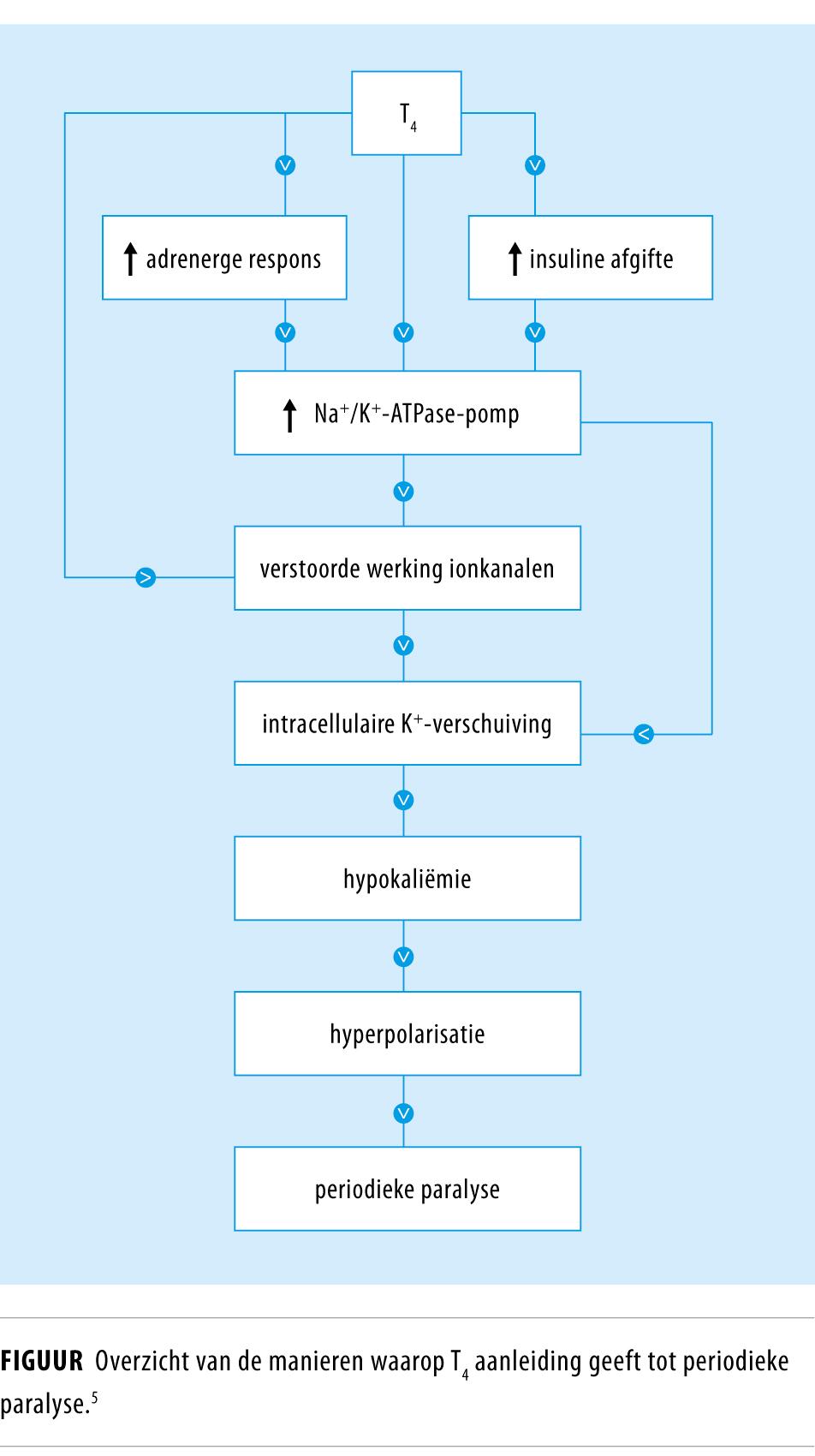
Allereerst stimuleert thyroxine zelf direct de Na+/K+-ATPase-pomp.2,3 Tevens is de Na+/K+-ATPase-pomp van patiënten met THPP gevoeliger voor thyroxine door genetische predispositie; dit is een mogelijke verklaring voor de hogere incidentie bij patiënten van Oost-Aziatische afkomst.2,6 Daarnaast wordt de activiteit van de Na+/K+-ATPase-pomp gestimuleerd door verhoogde stimulatie van de bèta-2-adrenerge receptoren. Gestegen sympathicusactiviteit lokt daarom THPP uit, zoals bij overmatige inspanning en stress.2 Ook reguleert insuline, onder invloed van thyroxine, de kaliuminflux. Dit verklaart postprandiale aanvallen van paralyse.4 Omdat 's nachts de kaliuminstroom in de skeletspieren hoger is, treden aanvallen van THPP vaker 's nachts op. De hogere prevalentie van THPP onder mannen wordt verklaard door het stimulerende effect van androgenen op de Na+/K+-ATPase-pomp en het inhiberende effect van oestrogenen en progesteron.1,3
Behandeling
Bij alle patiënten met hyperthyreoïdie, met of zonder periodieke paralyse, herstelt de Na+/K+-ATPase-pompactiviteit zodra een euthyreotische status is bereikt.1,3,7 De langetermijnbehandeling van THPP is daarom gericht op het verlagen van de thyroxineconcentratie door middel van thyreostatica – zoals thiamazol of propyl-thio-uracil –, radioactief jodium of eventueel een thyreoïdectomie.1 Voordat deze euthyreotische status bereikt is, heeft 62,2% van de THPP-patiënten een recidief van de paralytische aanval, het merendeel in de eerste 3 maanden.7
De hypokaliëmie is zelflimiterend en normaliseert bij herstel van de Na+/K+-ATPase-pomp als de patiënt euthyreotisch blijft. In de acute situatie kan hyperadrenerge activiteit behandeld worden met propranolol.8 Kaliumsuppletie is niet noodzakelijk, tenzij er sprake is van ernstige hypokaliëmie met een hartritme- of geleidingsstoornis. Hierbij dient gewaakt te worden voor een 'rebound hyperkaliëmie' door frequente controle van de kaliumconcentratie in serum. De kaliumsuppletie moet tijdig worden gestaakt.2,3,7
Conclusie
THPP is een zeldzame aandoening met een mogelijk dodelijke afloop die met name bij Aziatische mannen voorkomt. Bij onbegrepen parese of paralyse moet gedacht worden aan hypokaliëmie als uiting van thyreotoxicose. De behandeling van THPP bestaat uit behandeling van de hyperthyreoïdie en het geven van propranolol. Aangezien de hypokaliëmie zelflimiterend is, is kortdurende kaliumsuppletie slechts noodzakelijk bij ritme- of geleidingsstoornissen. Ondanks adequate behandeling bestaat er een hoog risico op een recidief. Regelmatige controle is geïndiceerd totdat een euthyreotische status bereikt is.
Literatuur
Kung, AWC. Clinical review: Thyrotoxic periodic paralysis: a diagnostic challenge. J Clin End Metab. 2006;91:2490-5. Medline
Lehmann-Horn F, Rüdel R, Jurkat-Rott K. Nondystropic myotonias and periodic paralysis. In: Engel AG, Franzini-Armstrong C, red. Myology. 3e dr. New York: Mc Graw-Hill; 2004. p. 1257-1300.
Lin SH, Mechanism of thyrotoxic periodic paralysis. J Am Soc Nephrol. 2012;23:985-988. Medline
Chan A, Shinde R, Chow CC, Cockram CS, Swaminathan R. Hyperinsulinaemia and Na+, K(+)-ATPase activity in thyrotoxic periodic paralysis.Clin Endocrinol. 1994;41:213-6. Medline
Kung AWC. Clinical review: thyrotoxic periodic paralysis: a diagnostic challenge. J Clin Endocrinol Metab. 2006;91:2490-5. Medline
Li Y, Yao Y, Yang M, Shi L, Li X, Yang Y, Zhang Y, Xiao C. Association between HLA-B*46 allele and Graves disease in Asian populations: a meta-analysis. In J Med Sci. 2013;10:164-70. Medline
Hsieh MJ, Lyu RK, Chang WN, Chang KH, Chen CM, Chang HS, Wu YR, Chen ST, Ro LS: Hypokalemic thyrotoxic periodic paralysis: clinical characteristics and predictors of recurrent paralytic attacks. Eur J Neurol. 2008;15:559-64. Medline
Shayne P, Hart A. Thyrotoxic periodic paralysis terminated with intravenous propranolol. Ann Emerg Med 1994;24:736-40. Medline





Reacties