artikel
Dieetvoeding voor medisch gebruik, kortweg medische voeding, dient om ondervoede patiënten te voorzien van voedingsstoffen. Patiënten kunnen ondervoed raken als ze niet goed kunnen eten of geen eetlust hebben. Een lekker smakend drankje met een hoge concentratie aan vitamines, eiwitten en andere nutriënten helpt dan misschien.1
Er is weinig controle op medische voeding. De producent moet het etiket en de samenstelling van het middel naar de Nederlandse Voedsel en Warenautoriteit (NVWA) opsturen, maar die kijkt alleen of het geen kwaad kan en of het bevat wat de mens aan voedingsstoffen nodig heeft. Voor sommige middelen suggereren de producenten echter dat ze meer doen dan het leveren van voedingsstoffen. Zo zou Cubitan helpen tegen decubitus, en Souvenaid tegen geheugenverlies bij patiënten met beginnende alzheimerdementie. Beide producten worden gefabriceerd door Nutricia.
De patiënt kan een dergelijk product zelf aanschaffen, maar dat kost 1300 euro per jaar; vult de dokter een ZN-artsenverklaring in dan betaalt de verzekering. De arts die daar het verzoek toe krijgt, zal zich afvragen of het middel werkt. Nutricia zegt dat ‘nutriënten grote invloed kunnen hebben op de pathofysiologie en progressie van de ziekte van Alzheimer’ (bron: www.souvenaid.nl), en verwijst naar een publicatie waarin gesteld wordt: ‘data from this study suggest that Souvenaid has a beneficial effect on cognitive function in mild A[lzheimer’s] D[isease]’.2 Maar Souvenaid is niet geregistreerd als geneesmiddel. De suggestie dat het de achteruitgang van het geheugen tegengaat is niet gecontroleerd door de European Food Safety Authority (EFSA), de instelling die gezondheidsclaims voor voedingsmiddelen beoordeelt. Bij gebrek aan overheidscontrole moet de arts dus zelf uitmaken of het middel werkt.
Naar mijn mening schiet het toezicht op deze quasi-geneesmiddelen tekort. Deze kwestie illustreert tevens de problematische kanten van samenwerking tussen bedrijven en onderzoekers op het gebied van voeding en gezondheid.
Wat is Souvenaid?
Souvenaid dient voor ‘dieetbehandeling in het beginstadium van de ziekte van Alzheimer’. De naam lijkt een combinatie te zijn van ‘souvenir’ (geheugen) en ‘aid’ (hulp), ‘geheugenhulp’ dus. Souvenaid is een melkdrankje. Behalve de gebruikelijke voedingsstoffen bevat het visolievetzuren, fosfolipiden, choline, uridine, selenium en 5 vitamines. Veel van deze bestanddelen zijn eerder onderzocht en bleken niet werkzaam tegen geheugenverlies. De onderzoekers beweren dat ze wél werkzaam zijn als ze tegelijk gegeven worden in de juiste verhoudingen.
Opmerkelijk is dat dit specifieke mengsel van voedingsstoffen te patenteren was. Er waren al eerder mengsels van voedingsstoffen tegen geheugenverlies gepubliceerd of gepatenteerd, maar kennelijk was er nog ruimte voor een patent voor Souvenaid. Het onderzoek dat tot deze verhouding van nutriënten heeft geleid, is niet openbaar gemaakt. Werd de samenstelling uitsluitend ingegeven door onderzoek, of speelde ook een rol wat er nog te patenteren was?
Dat weten we allemaal niet. Wel kunnen we nagaan hoe sterk de bewijzen zijn dat Souvenaid iets doet in de behandeling van patiënten met het beginstadium van de ziekte van Alzheimer. Hieronder bespreek ik de resultaten van 3 studies die de werkzaamheid van Souvenaid onderzochten (tabel).
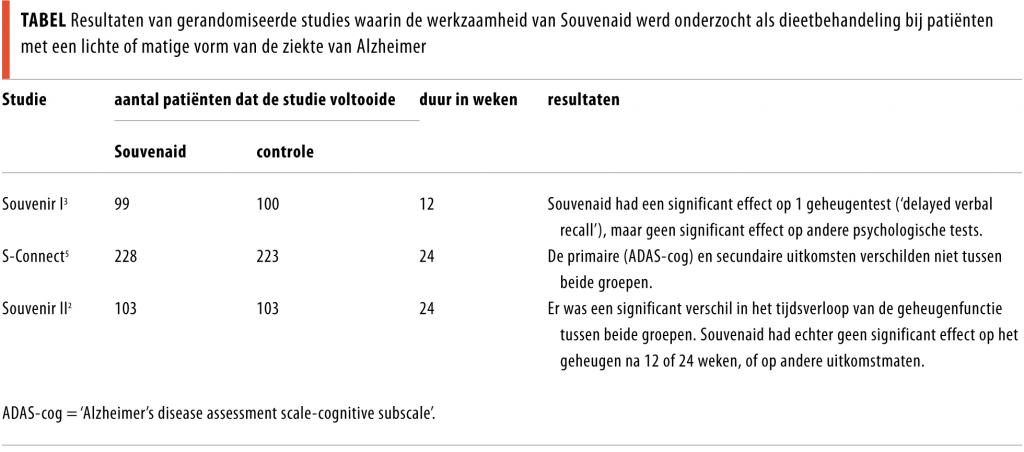
Klinische trials met Souvenaid
Souvenir I-studieDe Souvenir I-studie is de oudste van de 3 studies. Deze werd zoals dat hoort vooraf geregistreerd in een trialregister, namelijk het Nederlands Trial Register (NTR702). Daarin werd ‘cognitive performance at 12 weeks’ aangemerkt als primaire uitkomstmaat. Maar dat is weinig concreet; er werd niet aangegeven welke van de geplande psychologische tests beslissend was.
De resultaten werden gepubliceerd in 2010.3 Het abstract vermeldt: ‘... significant improvement in the delayed verbal recall task was noted in the active group compared with control (P = .021)’. Dit betreft echter niet de geplande statistische toetsing. De auteurs vermelden zonder nadere toelichting dat 40% van de patiënten na 12 weken een ‘0’ scoorden op deze geheugentest, met als gevolg dat de geplande statistische analyse werd vervangen door een andere. Souvenaid had geen effect op de uitkomst van de overige psychologische tests, waaronder ‘immediate recall’, of op het dagelijks functioneren.4
S-Connect-studieDe S-Connect-studie is de grootste van de 3 studies. Bij aanvang van de studie waren er 527 deelnemers; in de Souvenir I- en II studie waren dit er respectievelijk 225 en 259.2,3 In het trialregister (NTR1683) was tevoren een duidelijke primaire uitkomstmaat aangegeven, de ‘Alzheimer’s disease assessment scale-cognitive subscale’ (ADAS-cog). De resultaten zijn tot nu toe uitsluitend in een congresabstract beschreven.5 Daarin staan de volgende conclusies: ‘Both study groups showed a modest increase of ADAS-cog scores over time; however, no 24-week differences between the groups on the primary endpoint ADAS-cog were noted.’, en: ‘No difference between the groups was observed on the secondary parameters, ADCS-ADL and CDR-SOB’. Souvenaid had dus geen effect. Het effect van Souvenaid op ‘delayed verbal recall’, dat gunstig was in de voorafgaande Souvenir I-studie, werd in de S-Connect-studie niet onderzocht.
Souvenir II-studieBij de Souvenir II-studie vermeldt Danone, de eigenaar van Nutricia, als primaire uitkomstmaat in het trialregister (NTR1975): ‘Memory performance (NTB) during 24 weeks of intervention’. NTB staat voor ‘Neuropsychological test battery’, een set van 9 tests die elk weer uit subtests kunnen bestaan. Welke daarvan door de onderzoekers als beslissend werd beschouwd, werd niet aangegeven.
De publicatie verscheen in 2012.2 De auteurs presenteerden als primaire uitkomstmaat een combinatie van 5 geheugentests die ze tezamen ‘NTB memory domain’ noemden; 2 van die tests betroffen ‘immediate recall’ en 2 betroffen ‘delayed recall’. In het abstract staat: ‘The NTB memory domain Z-score was significantly increased in the active versus the control group over the 24-week intervention period (p = 0.023…’. In werkelijkheid was er geen significant effect van de behandeling, niet na 12 en niet na 24 weken. De significante p-waarde sloeg op een verschil in tijdsverloop van de geheugenfunctie; na 12 weken deed de Souvenaid-groep het iets slechter dan de controlegroep en na 24 weken iets beter, zij het niet-significant. Het is twijfelachtig hoe relevant dit verschil in verloop van de geheugenfunctie met de tijd is, gegeven dat het eindresultaat na 24 weken niet duidelijk verschilde. De auteurs vermeldden niet of het effect op de ‘delayed verbal recall’ uit de Souvenir I-studie kon worden gereproduceerd.
Conclusies
Kwaliteit van bewijsvoering De primaire uitkomstmaat was in de 2 ‘succesvolle’ studies tevoren niet concreet gespecificeerd. De significante uitkomst in de Souvenir I-studie werd in de Souvenir II-studie niet bevestigd; de statistische significantie betrof een effect dat wellicht interessant is voor statistici maar dat irrelevant is voor patiënten en behandelaars. Het blijft denkbaar dat voedingsstoffen of mengsels daarvan het geheugen verbeteren.6 De uitkomsten van het onderzoek naar Souvenaid volstaan echter niet om dit middel tegen alzheimerdementie op de markt te zetten, laat staan om vergoeding door de ziektekostenverzekering te rechtvaardigen. Dat genereert nodeloze kosten én voorbarige hoop op genezing.
Invloed van de fabrikant In het Souvenaid-onderzoek kwamen een aantal zaken samen die mis kunnen gaan in de samenwerking tussen wetenschappers en het bedrijfsleven. De studies werden betaald door Nutricia, en veel van de auteurs waren daar in dienst of traden op als adviseur of consultant. De gegevensverwerking van de Souvenir I-studie gebeurde onder toezicht van Nutricia en het bedrijf huurde een ghostwriter in om het artikel te schrijven. De titels van de publicaties bevatten de merknaam van het product.2,5 Elke studie omvatte een groot aantal klinische centra die een klein aantal patiënten leverden, en dat terwijl beginnende alzheimerdementie veel voorkomt en het consumeren van een melkdrankje weinig belastend is. De studies hadden simpeler en goedkoper kunnen worden uitgevoerd met minder centra die meer patiënten leverden. Een dergelijke ‘versnipperende’ strategie lijkt op ‘seeding’, waarbij een farmaceutisch bedrijf probeert zoveel mogelijk artsen vertrouwd te maken met een nieuw middel.7 De S-Connect-studie leverde geen gunstige uitkomst op, maar de Souvenir II-studie wel; de S-Connect-studie werd in 2010 voltooid maar is nog niet gepubliceerd, terwijl de Souvenir II-studie in 2011 werd voltooid en in 2012 is gepubliceerd.2 Er lijkt dus sprake te zijn van publicatiebias.8
Wat moet er gebeuren?
De huidige regelgeving is toegesneden op medische voeding voor patiënten die niet op normale wijze kunnen of willen eten. Daar is niets op tegen. Maar als een fabrikant suggereert dat een medische voeding alzheimerdementie, decubitus of een ander ziektebeeld voorkomt of geneest zouden de NVWA en de zorgverzekeraars het moeten aanmerken als geneesmiddel. Zonder registratie als geneesmiddel geen vergoeding. Daarmee is het dilemma van de voorschrijvende arts opgelost. Als het College ter Beoordeling van Geneesmiddelen (CBG) concludeert dat het middel werkt, kunnen veel patiënten daarvan profiteren. Als het niet werkt, kunnen de zorgverzekeraars hun en ons geld beter in de zak houden.
Literatuur
Ondervoeding bij ouderen. Publicatienr 2011/32. Den Haag: Gezondheidsraad; 2011.
Scheltens P, Twisk JW, Blesa R, et al. Efficacy of Souvenaid in mild Alzheimer’s disease: results from a randomized, controlled trial. J Alzheimers Dis. 2012;31:225-36 Medline. doi:10.3233/JAD-2012-121189
Scheltens P, Kamphuis PJ, Verhey FR, et al. Efficacy of a medical food in mild Alzheimer’s disease: a randomized, controlled trial. Alzheimers Dement. 2010;6:1-10.e1 Medline. http://dx.doi.org/10.1016/j.jalz.2009.10.003
Kamphuis PJ, Verhey FR, Olde Rikkert MG, Twisk JW, Swinkels SH, Scheltens P. Effect of a medical food on body mass index and activities of daily living in patients with Alzheimer’s disease: secondary analyses from a randomized, controlled trial. J Nutr Health Aging. 2011;15:672-6 Medline. doi:10.1007/s12603-011-0339-3
Shah R, Kamphuis PJ, Leurgans S, et al. Souvenaid as an add-on intervention in patients with mild to moderate Alzheimer’s disease using Alzheimer’s disease medication: results from a randomized, controlled, double-blind study (S-Connect). J Nutr Health Aging. 2011;15(Suppl 1):S30.
Durga J, van Boxtel MP, Schouten EG, et al. Effect of 3-year folic acid supplementation on cognitive function in older adults in the FACIT trial: a randomised, double blind, controlled trial. Lancet. 2007;369:208-16 Medline. doi:10.1016/S0140-6736(07)60109-3
Sox HC, Rennie D. Seeding trials: just say “no”. Ann Intern Med. 2008;149:279-80 Medline. doi:10.7326/0003-4819-149-4-200808190-00012
Montori VM, Smieja M, Guyatt GH. Publication bias: a brief review for clinicians. Mayo Clin Proc. 2000;75:1284-8 Medline. doi:10.4065/75.12.1284





Medische voeding
Overtuigend verhaal!
Nu maar hopen dat de conclusies en aanbevelingen van de auteur worden overgenomen!
Ronald Houwing, dermatoloog, Deventer Ziekenhuis