Een 71-jarige patiënte komt op het spreekuur wegens een kortdurende woordvindstoornis met versprekingen. Dat lijkt in eerste instantie op een TIA, maar ondanks gebruik van een plaatjesaggregatieremmer kwamen de klachten terug. Korte tijd later kreeg zij ook acute draaiduizeligheid met misselijkheid en braken. Wat is er met deze patiënte aan de hand?
Samenvatting
Het syndroom van Susac is een auto-immuunangiopathie wat klassiek leidt tot de trias encefalopathie, retinopathie en gehoorverlies. Diagnostiek verloopt multidisciplinair en bestaat uit een MRI-hersenen, fluorescentieangiografie (FAG) en audiografie. Vroegtijdige behandeling is van belang voor een betere prognose met mogelijk reversibiliteit.
In dit artikel presenteren wij een 71-jarige vrouw met meerdere episodes van afzonderlijke klachten zoals een afasie, gedragsverandering, geheugenverlies en draaiduizeligheid met tinnitus. MRI van de hersenen liet kenmerkende signaalveranderingen van het corpus callosum zien, waardoor werd gedacht aan het syndroom van Susac. Met een afwijkend FAG en audiografie was de trias compleet. Hierop kreeg de patiënte een behandeling met immunosuppressiva, waarna cognitieve verbetering optrad.
Kernpunten
- Het syndroom van Susac begint vaak met neurologische of psychiatrische symptomen; daarnaast kunnen gehoorklachten en draaiduizeligheid optreden, al dan niet met visusdaling.
- De diagnose ‘syndroom van Susac’ wordt gesteld in samenspraak met de neuroloog, oogarts en kno-arts, omdat zich in korte tijd verschillende klachten voordoen bij dit ziektebeeld.
- Hoekstenen van de diagnostiek zijn een MRI van de hersenen, fluorescentieangiografie van de retina en een audiogram.
- Omdat het syndroom van Susac zeldzaam is en verschillende klinische uitingsvormen kent, moeten andere oorzaken worden uitgesloten om de diagnose met zekerheid te kunnen stellen.
- De behandeling voor het syndroom van Susac is gericht op de auto-immuniteit van de ziekte met immunosuppressiva.
artikel
Het syndroom van Susac is een zeldzame auto-immuunaandoening van de precapillaire arteriolen in de hersenen, het netvlies en het binnenoor.1 Doordat meerdere organen bij deze aandoening zijn betrokken, is multidisciplinaire diagnostiek vereist. Het klassieke klinische beeld bestaat uit een trias van encefalopathie, retinopathie en gehoorklachten.2 De diagnose wordt voornamelijk gesteld bij vrouwen met een gemiddelde leeftijd tussen de 20 en 40 jaar.1,2 In dit artikel presenteren wij de casus van een patiënte bij wie het syndroom van Susac op 71-jarige leeftijd werd vastgesteld.
Ziektegeschiedenis
Patiënte, een 71-jarige vrouw die bekend was met een lage-rughernia en sinds enkele jaren slechthorendheid, zocht in korte tijd meerdere keren medische hulp vanwege diverse klachten. De eerste klacht betrof een kortdurende woordvindstoornis met versprekingen, waarbij gedacht werd aan een TIA. Zij begon met clopidogrel, een plaatjesaggregatieremmer; achttien dagen later kwam zij echter opnieuw bij de neuroloog met een woordvindstoornis en daarnaast vertoonde zij ook duidelijke cognitieve vertraging. Op een MRI van de hersenen werden geen afwijkingen vastgesteld, ook niet in het corpus callosum of op de diffusiegewogen opnames; uitgebreide cardiale analyse bracht geen cardiale emboliebron aan het licht.
Elf dagen later kwam de patiënte opnieuw bij de neuroloog, deze keer vanwege acute draaiduizeligheid met misselijkheid en braken. Ook bleek dat het gehoor sinds een halfjaar achteruit was gegaan en had zij last van tinnitus. Bij deze klachten dacht de neuroloog direct aan een perifeer vestibulair syndroom, waarna in overleg met de kno-arts opnieuw een audiogram werd verricht. Dit liet beiderzijds symmetrisch perceptief gehoorverlies zien, met name in de lage tonen; de toestand was verslechterd ten opzichte van de registratie van zes jaar daarvoor.
Een maand later bij poliklinische neurologische controle bleek dat het thuis niet goed ging door stemmingswisselingen (wisselende euforie), balansproblemen, meer moeite met handelingen (met name kledingapraxie), motorische onrust en vermoeidheid met de neiging tot het omdraaien van het dag-nachtritme. Omdat de neurologische klachten progressief waren en er mogelijk een delier dan wel een encefalopathisch beeld was opgetreden, werd de differentiaaldiagnose verbreed. De neuroloog liet opnieuw een MRI van de hersenen maken, waarop een groot aantal nieuwe, kleine wittestofafwijkingen zichtbaar waren; ook het corpus callosum was duidelijk aangedaan (figuur 1).
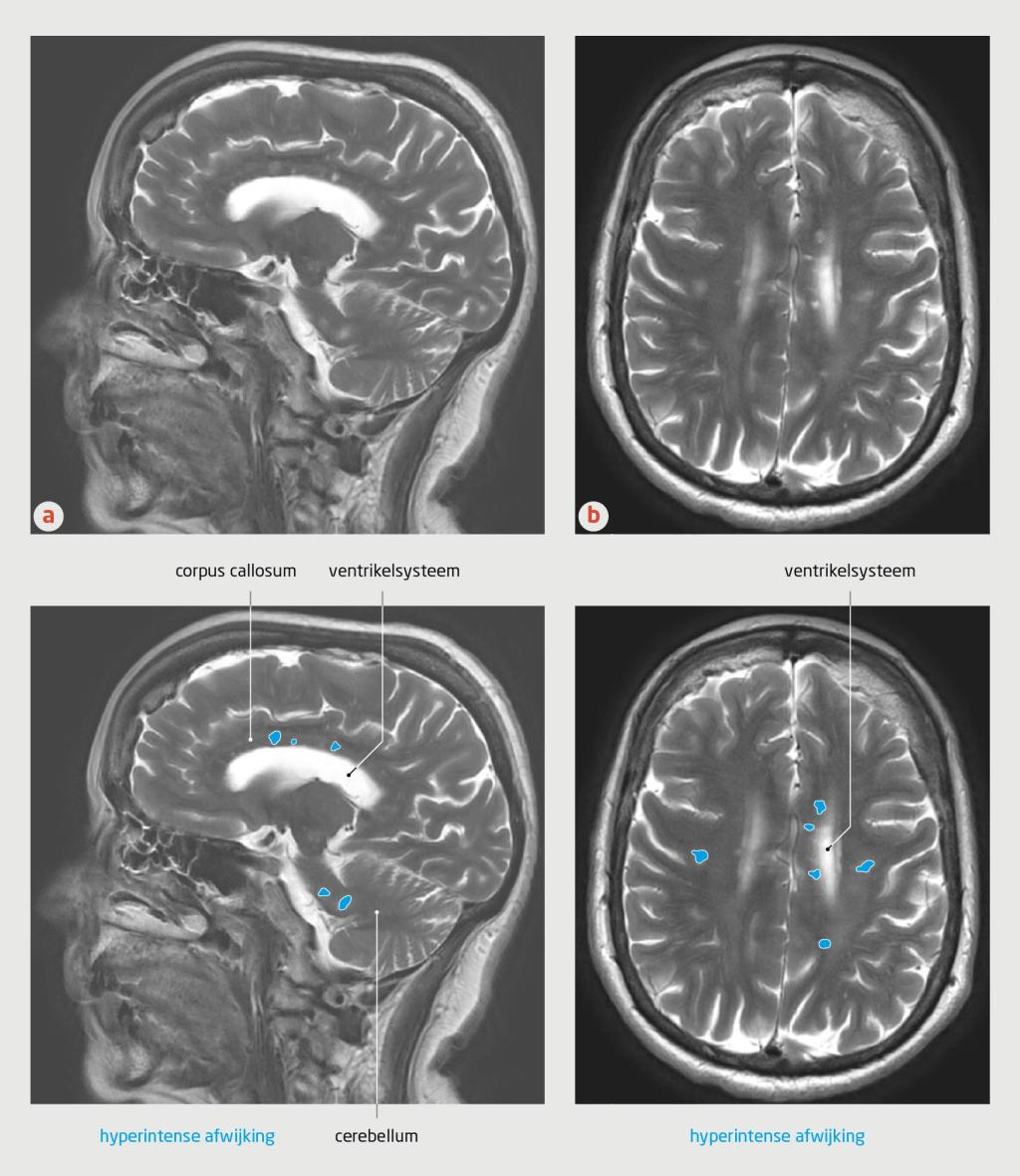
Door de lokalisatie in voornamelijk het centrale deel van het corpus callosum en gezien de eerder vastgestelde audiogramafwijkingen, werd gedacht aan het syndroom van Susac. Vanwege de zeldzaamheid van dit ziektebeeld en de atypische leeftijd waarop het ziektebeeld zich voordeed, overlegde de neuroloog met een academisch ziekenhuis. De afwijkingen waren weliswaar kenmerkend voor het syndroom van Susac, maar dat sluit andere verklaringen niet uit, zoals infecties, paraneoplastische verschijnselen en auto-immuunziektes. Daarom werd aanvullend onderzoek ingezet.
Met CT-angiografie van de thorax, liquordiagnostiek en een PET-CT-scan werden andere afwijkingen uitgesloten, wat het vertrouwen gaf om inderdaad de diagnose ‘syndroom van Susac’ te stellen. Hoewel de patiënte geen visusklachten had, werd fluorescentieangiografie (FAG) verricht, waarmee een vasculitis van meerdere vaten en één retinale vaatocclusie werd aangetoond (figuur 2). Daarmee was de klassieke trias compleet.
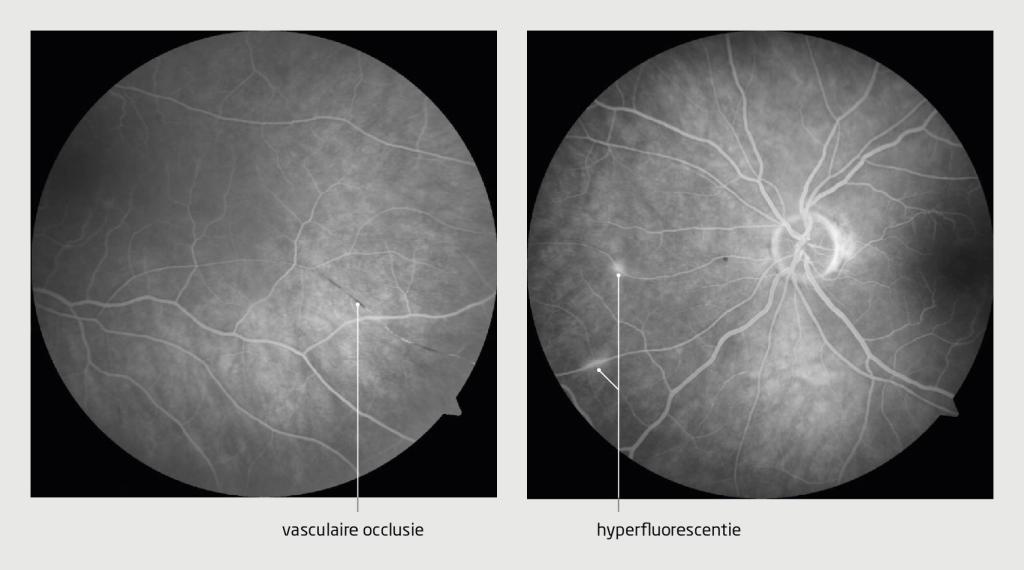
Na het stellen van de diagnose ‘syndroom van Susac’ kreeg de patiënte direct intraveneus methylprednisolon (1000 mg per dag) en immunoglobulines (2 g/kg gedurende vijf dagen) toegediend, gevolgd door oraal prednisolon. In reactie op de hoge dosering prednisolon ontwikkelde zij een psychose, die goed reageerde op haloperidol.
In twee maanden tijd verbeterde zij geleidelijk aan op het cognitieve vlak, maar bij afbouw van prednisolon had zij toenemend last van draaiduizeligheid. Hierop werd prednisolon tijdelijk niet verder afgebouwd. Enkele maanden later volgde opnieuw een plotselinge terugval met afasie en een n.-facialisparese rechts, waarna de patiënte kortdurend werd opgenomen. Zij kreeg azathioprine, een immunosupressivum, met als doel de prednisolon verder te kunnen afbouwen.
Inmiddels is de patiënte goed hersteld, op het gehoorverlies na, en heeft zij de prednisolon verder afgebouwd.
Beschouwing
Het syndroom van Susac werd in 1979 geïntroduceerd door de Amerikaanse neuroloog John Susac. Hij beschreef twee vrouwen met psychiatrische en neurologische symptomen die tevens gehoor- en visusklachten hadden door microangiopathie.3 Sindsdien is duidelijk geworden dat het syndroom een trias van encefalopathie, retinopathie en gehoorverlies omvat.1 Het blijft een zeldzame aandoening met een vrouw/man-ratio van 3:1.2,4 De geschatte prevalentie in Centraal-Europa is 0,14 per 100.000 mensen en het syndroom wordt vooral gezien bij mensen tussen het 20e en 40e levensjaar.5,6
Pathofysiologie
Auto-immuniteit speelt een grote rol bij het ontstaan van dit syndroom, waarbij antistoffen tegen het endotheel van de microvasculatuur in de hersenen, retina en het binnenoor (cochlea en semicirculaire kanalen) worden gevormd.2 Inmiddels zijn endotheelcel-geassocieerde IgG-antistoffen aangetoond bij 25% van de patiënten, tegenover > 5% in de controlegroep.7 Micro-infarcten ontstaan door proliferatie van de arteriolenwand, infiltratie van lymfocyten, destructie van de capillairen en verdikking van de lamina basalis in zowel de witte als grijze stof.8 Ook het feit dat langdurige immunomodulerende behandelingen de ziekteactiviteit onderdrukken, bevestigt de auto-immuungenese.9
Klinisch beeld
Het klinische beeld varieert sterk, afhankelijk van waar de micro-infarcten zijn gelokaliseerd. Aanvankelijk vertonen patiënten vaak een beeld dat past bij encefalopathie, zoals cognitieve en gedragsmatige achteruitgang (problemen met het kortetermijngeheugen, concentratie- en executieve stoornissen, desoriëntatie en stemmingswisselingen).2,4 Opvallend is de migraineuze of beklemmende hoofdpijn die bij bijna 80% van de patiënten tot zes maanden voorafgaand aan andere symptomen ontstaat; waarschijnlijk treedt deze hoofdpijn op door beschadiging van de leptomeningeale bloedvaten.4,8
Minder dan 15% van de patiënten vertoont bij klinische presentatie de complete trias van symptomen. De retinale vaatocclusies zijn aanvankelijk namelijk vaak asymptomatisch door hun lokalisatie in de perifere of midperifere vaten. De tijdsduur tussen het eerste symptoom en de volledige trias bedraagt gemiddelde 21 weken; uiteindelijk treedt bij 85% van alle patiënten de volledige trias op.4
Diagnostiek
De hoekstenen van diagnostiek zijn MRI van de hersenen, FAG van de retina en een audiogram. De MRI van de hersenen moet multifocale hyperintense, ronde, kleine afwijkingen laten zien, waarvan minimaal één in het corpus callosum, zoals bij onze patiënte (zie figuur 1). Verder hoeven er geen visusproblemen te zijn, maar moet minimaal één retinale vaatocclusie of hyperfluorescentie van de arteriële wand worden aangetoond. Bij onze patiënte was zowel een retinale vaatocclusie te zien als meerdere hyperfluorescenties (zie figuur 2). Tot slot moet er sprake zijn van tinnitus of gehoorverlies, aangetoond met een audiogram zoals bij onze patiënte, of perifere vertigo.9 Op dit moment loopt nog onderzoek naar de plaats van een antistoffenbepaling in de diagnostiek.2,7
Behandeling
De behandeling bestaat uit immunosuppressiva, waarbij intraveneus methylprednison gevolgd door oraal prednison de eerste stap vormt.10 Daarnaast zijn aanvullende behandelingen beschreven met immunoglobulines, mycofenolaatmofetil, cyclofosfamide, azathioprine en rituximab afhankelijk van de ernst van de ziekte.10 Verder is het advies om te beginnen met plaatjesaggregatieremming in verband met de frequente micro-infarcering. Voor al deze behandeladviezen geldt dat ze zijn gebaseerd op observationeel onderzoek en ‘expert opinion’.
De periode tussen de eerste klachten en het begin van de behandeling is vaak lang door de zeldzaamheid van het ziektebeeld en de gevarieerde klinische presentatie.2,10 Kennis en herkenning van de ziekte zijn dus een vereiste. De encefalopathie en retinopathie kunnen goed reageren op behandeling, maar het gehoorverlies is vaak irreversibel.2 Levenslang monitoren is daarom van belang, met name gezien het risico op een relaps.
Conclusie
Het syndroom van Susac is een zeldzaam ziektebeeld dat tijdige herkenning vereist voor spoedige behandeling. De klinische presentatie varieert, waarbij het ook op oudere leeftijd kan voorkomen. Vroegtijdige behandeling geeft betere resultaten en follow-up is noodzakelijk.
Literatuur
- Susac JO, Egan RA, Rennebohm RM, Lubow M. Susac’s syndrome: 1975-2005 microangiopathy/autoimmune endotheliopathy. J Neurol Sci. 2007;257(1-2):270-272. doi:10.1016/j.jns.2007.01.036. Medline
- Pereira S, Vieira B, Maio T, Moreira J, Sampaio F. Susac’s Syndrome: An Updated Review. Neuroophthalmology. 2020;44(6):355-360. doi:10.1080/01658107.2020.1748062. Medline
- Susac JO, Hardman JM, Selhorst JB. Microangiopathy of the brain and retina. Neurology. 1979;29(3):313-316. doi:10.1212/WNL.29.3.313. Medline
- Sauma J, Rivera D, Wu A, et al. Susac’s syndrome: an update. Br J Ophthalmol. 2020;104(9):1190-1195 Medline.
- Seifert-Held T, Langner-Wegscheider BJ, Komposch M, et al. Susac’s syndrome: clinical course and epidemiology in a Central European population. Int J Neurosci. 2017;127(9):776-780. doi:10.1080/00207454.2016.1254631. Medline
- Koenen M, Djadoenath AC. Syndroom van Susac: psychose door zeldzame angiopathie. Ned Tijdschr Geneeskd. 2015;159:A8237 Medline.
- Jarius S, Kleffner I, Dörr JM, et al. Clinical, paraclinical and serological findings in Susac syndrome: an international multicenter study. J Neuroinflammation. 2014;11(1):46. doi:10.1186/1742-2094-11-46. Medline
- Kleffner I, Duning T, Lohmann H, et al. A brief review of Susac syndrome. J Neurol Sci. 2012;322(1-2):35-40. doi:10.1016/j.jns.2012.05.021. Medline
- Kleffner I, Dörr J, Ringelstein M, et al; European Susac Consortium (EuSaC). Diagnostic criteria for Susac syndrome. J Neurol Neurosurg Psychiatry. 2016;87(12):1287-1295. doi:10.1136/jnnp-2016-314295. Medline
- Rennebohm RM, Asdaghi N, Srivastava S, Gertner E. Guidelines for treatment of Susac syndrome - An update. Int J Stroke. 2020;15(5):484-494. doi:10.1177/1747493017751737. Medline




Reacties