Toets voor nascholing (verlopen)
Aan dit leerartikel was een toets gekoppeld waarmee je nascholingspunten kon verdienen.
Samenvatting
-
Verbloeding is een belangrijke doodsoorzaak van traumapatiënten.
-
Bij massaal bloedverlies ontstaat een combinatie van coagulopathie, acidose en hypothermie, die zonder juiste correcties een hoge morbiditeit en mortaliteit met zich meebrengt.
-
Onderzoek bij gewonde militairen laat zien dat een hoge ratio versbevroren plasma/rodebloedcelconcentraat (FFP:PRBC-ratio) een positief effect heeft op de overleving.
-
De studies geven nog geen uitsluitsel over de ideale verhouding FFP:PRBC; de ratio waarbij nog een positief effect wordt aangetoond varieert van 1:1 tot 1:3.
-
Onnodige FFP-transfusies bij traumapatiënten zonder dreigende verbloeding geven een verhoogde kans op complicaties zoals multi-orgaanfalen en acuut respiratoir ‘distress’-syndroom.
-
Er is meer onderzoek nodig naar de accuraatheid van het diagnosticeren van een acute coagulopathie.
artikel
Verbloeding is een belangrijke oorzaak van overlijden van traumaslachtoffers.1 Een deel van deze verbloedingen is volgens nieuwe inzichten potentieel te voorkomen. Recente literatuur laat een verbetering in overleving zien bij traumapatiënten met ernstig acuut bloedverlies wanneer stollingsstoornissen vroeg met een agressief transfusiebeleid gecorrigeerd worden.
Wereldwijd is trauma een belangrijke oorzaak voor ernstige morbiditeit en mortaliteit. In Nederland sterven jaarlijks ruim 5000 mensen ten gevolge van een traumatisch letsel.2 Ondanks ontwikkelingen op het gebied van resuscitatie, chirurgie en intensivecaregeneeskunde is de verwachting dat in de nabije toekomst de trauma-gerelateerde sterfte verder zal toenemen.3
In dit artikel beschrijven wij de huidige stand van zaken over het transfusiebeleid bij traumapatiënten met massaal bloedverlies. Voor deze beschrijvende review hebben wij een zoekactie verricht in de databases van Medline en Embase. Als zoektermen hebben wij gebruikgemaakt van verschillende relevante Engelstalige termen waaronder ‘blood transfusion’, ‘trauma’, ‘coagulopathy’ en ‘hemorrhage’.
Historie van bloedtransfusie bij trauma
Kennis op het gebied van bloedtransfusies is onlosmakelijk verbonden met oorlogsgeweld en de daarbij behorende traumatologie. Nadat de Oostenrijkse arts Karl Landsteiner in 1901 het bloedgroepensysteem ontdekt had, pasten Amerikaanse en Canadese legerchirurgen tijdens de Eerste Wereldoorlog voor het eerst incidenteel de transfusie van volbloed toe. Dit was mogelijk omdat in 1914 werd ontdekt dat een kleine hoeveelheid natriumcitraat de bloedstolling buiten het lichaam voorkwam. Het grote belang hiervan werd overtuigend aangetoond gedurende de Tweede Wereldoorlog. Toen kregen gewonde militairen op diverse slagvelden op grote schaal bloedtransfusies. Het succes dat hiermee werd geboekt op het slagveld, maakte dat bloedtransfusie al snel werd overgenomen voor civiele toepassing in vredestijd.
In de jaren 70 van de vorige eeuw bestond optimale resuscitatie van patiënten met een verbloedingsshock uit het toedienen van 1-2 l cristalloïden in combinatie met volbloed.4 Sinds de tweede helft van de jaren 80 werden bloedproducten in diverse componenten aangeleverd waardoor efficiënter en veiliger transfunderen mogelijk werd. Volbloed werd bijna compleet vervangen door eenheden rodebloedcelconcentraat (‘packed red blood cells’ (PRBC)), versbevroren plasma, (‘fresh frozen plasma’ (FFP)) en trombocytensuspensies. Er werden transfusieprotocollen ontwikkeld voor traumapatiënten met massaal bloedverlies,5 waarbij als definitie voor ‘massaal bloedverlies’ gehanteerd wordt, dat er toediening nodig is van meer dan 10 units PRBC’s binnen 24 h. Dat staat ongeveer gelijk aan het vervangen van het totale bloedvolume. Bij deze patiënten wordt in de literatuur een mortaliteit van 25 tot meer dan 50% beschreven.6 De traditionele transfusieprotocollen adviseerden gebruik te maken van colloïden, cristalloïden en PRBC’s, zonder stollingsfactoren, om het zuurstoftransport naar de weefsels te garanderen. Eventuele stollingstoornissen konden vervolgens op geleide van de kliniek en laboratoriumparameters gecorrigeerd worden door toediening van FFP en trombocytensuspensie.
Dodelijke trias
Stollingsstoornissen en verbloeding hebben bij traumapatiënten een andere pathofysiologie dan bij patiënten met ernstige bloedingen die bijvoorbeeld ontstaan gedurende een operatie. Bij operatiepatiënten is de locatie van een bloeding vaak unifocaal en de omliggende weefselschade vaak beperkt. Daarom kan een dergelijke bloeding vaak relatief eenvoudig operatief tot staan worden gebracht. Traumapatiënten hebben vaak bloedingen op meerdere en moeilijk te bereiken locaties met uitgebreide omliggende weefselschade op microscopisch en macroscopisch niveau. Bovendien is er bij de ontdekking van een operatieve bloeding meestal nog geen grote hoeveelheid bloedverlies; bij de meeste traumapatiënten is de hoeveelheid en de snelheid van het bloedverlies echter groot.
Ernstige bloedingen na een traumatisch letsel leiden tot een cascade van pathologische effecten. Die omvatten alle componenten van het hemostatische systeem. Het stollingsproces bestaat uit multipele enzymreacties die onder andere beïnvloed worden door wisselingen in lichaamstemperatuur en de zuurgraad van het bloed.
Hypothermie veroorzaakt een vermindering van de functie van trombocyten en remt de stolselvorming. Een ander gevolg van hypothermie is hyperfibrinolysis, waarbij een ontstaan stolsel sneller afgebroken wordt en dus minder stabiel is.
Het falen van het stollingssysteem wordt verergerd door een remming van de enzymactiviteit als gevolg van acidose. Deze acidose ontstaat door het progressieve bloedverlies wat leidt tot een verminderde weefseloxygenatie en shock.
Als gevolg van de combinatie van bloedverlies en toediening van grote hoeveelheden infusievloeistoffen kan verdunning (hemodilutie) optreden. Deze hemodilutie in combinatie met een verhoogd gebruik van de stollingsfactoren en trombocyten ter plaatse van de bloeding, zorgt voor een systemische verlaging van alle componenten van het stollingssysteem. Daardoor verergert de stollingstoornis, de coagulopathie. Als gevolg van het bloedverlies en de hemodilutie ontstaan tevens elektrolytstoornissen, zoals een hypocalciëmie, die de coagulopathie ook nadelig beïnvloeden.
Trias: coagulopathie, acidose en hypothermie De bovenbeschreven combinatie van coagulopathie, acidose en hypothermie vormt de dodelijke trias (‘lethal triad’). De trias leidt bij de traumapatiënt tot een vicieuze cirkel (figuur), die zonder juiste correcties een hoge morbiditeit en mortaliteit met zich meebrengt.7 In de afgelopen decennia zijn diverse strategieën ontwikkeld om deze cirkel te doorbreken, waaronder het snel chirurgisch behandelen van de levensbedreigende letsels zonder meteen definitieve behandeling uit te voeren (‘damage control’-chirurgie), het accepteren van een lage bloeddruk tot de bloeding onder controle is (‘permissive hypotension’-resuscitatie) en het actief bestrijden van de hypothermie middels verwarmde infusievloeistoffen.8 Daarnaast zijn producten als tranexaminezuur en stollingsfactorconcentraten waaronder fibrinogeen, protrombinecomplex en recombinant factor VIIa ontwikkeld, waarmee direct wordt ingegrepen op de stolling van traumapatiënten met acuut ernstig bloedverlies.
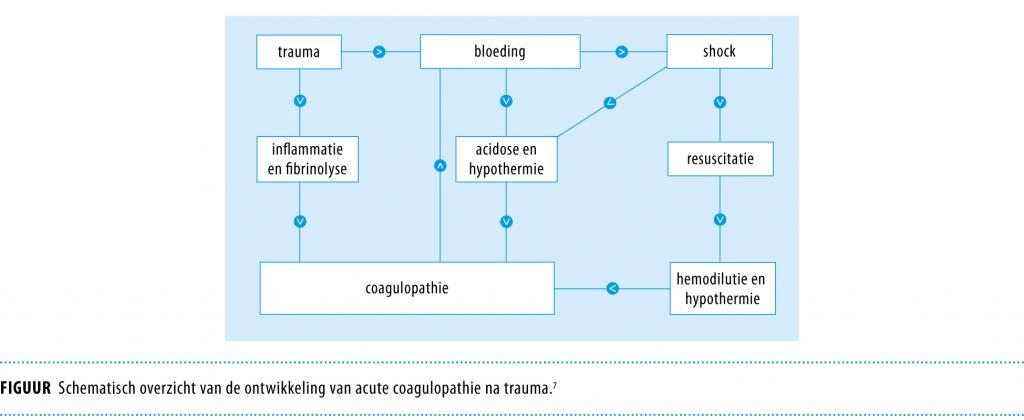
Agressieve correctie Voorheen werd gedacht dat coagulopathie na trauma uitsluitend het gevolg was van hemodilutie en hypothermie over een tijdsbestek van een aantal uren. Recentelijk is echter beschreven dat bij 25% van de ernstig gewonde traumapatiënten al een acute coagulopathie aanwezig was bij aankomst op de traumakamer.9,10 Aanwezigheid van deze acute coagulopathie was tevens geassocieerd met een verhoogde mortaliteit.9,10
Met deze kennis hebben artsen in Irak en Afghanistan een studie verricht naar de effecten van een transfusiebeleid gericht op het vroeg en agressief corrigeren van de acute coagulopathie bij oorlogsgewonden.11 Bij deze behandelstrategie werd voor de transfusie een FFP:PRBC-ratio gebruikt die een verhouding van 1:1 benaderde. Door het gebruik van deze niet-traditionele transfusiestrategie werd een afname in het aantal verbloedingen gezien met een reductie in mortaliteit van 69% naar 19%. Op basis van deze bevindingen concludeerden de auteurs dat een hoge FFP:PRBC-ratio onafhankelijk geassocieerd is met verbeterde overleving. Zij adviseren dan ook om voor alle traumapatiënten met een coagulopathie een transfusieprotocol te gebruiken met een FFP:PRBC-ratio van 1:1.
Massatransfusie
Naar aanleiding van de data uit de militaire studies besloten wereldwijd vele traumacentra na 2007 een transfusieprotocol in te voeren met een FFP:PRBC-ratio van 1:1 om hiermee het effect van volbloedtransfusies te evenaren. In de literatuur verschijnen de laatste tijd dan ook veel resultaten van studies naar het effect van hoge FFP:PRBC-ratio’s op klinische uitkomsten bij civiele traumapatiënten. De mortaliteitscijfers in deze studies bleken lager te zijn als men hoge transfusieratio’s gebruikte, dat wil zeggen veel FFP’s in verhouding tot PRBC’s.6,12-14 Het ging hier overigens niet om direct vergelijkend prospectief onderzoek. De tabel geeft een overzicht van de uitkomsten van de studies.
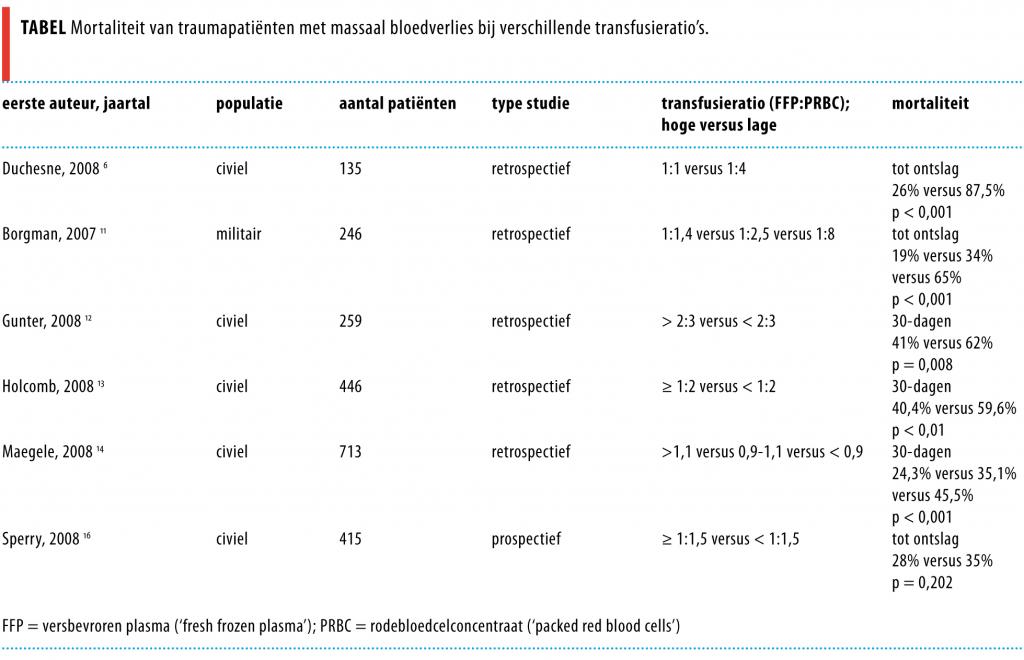
In een van die studies, uitgevoerd bij 1175 traumapatiënten, concludeerden de auteurs dat FFP-transfusie geassocieerd was met een mortaliteitsreductie van 2,9% voor elke eenheid die werd getransfundeerd. Daarnaast zagen zij dat elke toediening van 1 eenheid FFP onafhankelijk geassocieerd was met een 2,1% hoger risico op multi-orgaanfalen en 2,5% op acuut respiratoir ‘distress’-syndroom (ARDS).15 Deze sterke associatie met de ontwikkeling van ARDS werd ook gevonden in een andere studie waarin hoge FFP:PRBC-ratio’s (van > 1:1,5) werden vergeleken met ratio’s van ≤ 1:1,5. De incidentie van ARDS was in die groepen respectievelijk 47% en 24% (p = 0,001) Er was ook een niet-significante toename van multi-orgaanfalen in de groep patiënten die een hogere FFP:PRBC-ratio kregen: 64% versus 54% (p = 0,085).16
Tegengestelde resultaten werden gevonden bij 2 andere studies, bij respectievelijk 133 en 806 patiënten.17,18 Deze studies concludeerden dat transfusieratio van 1:1 geen positief effect had op de overleving.17,18 Een van de auteurs beschrijft dat de ideale verhouding voor een verbetering van de overleving waarschijnlijk ligt tussen de 1:2 en 1:3.17
Weer een ander onderzoek vond een significante mortaliteitsreductie bij een toegenomen FFP:PRBC-ratio. Er werd echter geen verdere toename in overleving gezien nadat een FFP:PRBC-ratio van 1:3 was bereikt.19
Beschouwing
Traditionele transfusieprotocollen zijn toereikend voor ongeveer 90% van de traumapatiënten. Het gaat dan om degenen die niet in ernstige hemorragische shock verkeren en die een adequate stolling hebben na hun letsel.20 Voor de overige patiënten, die wel in ernstige hemorragische shock verkeren, lijkt een hoge FFP:PRBC-ratio een positief effect te hebben op de klinische uitkomsten, volgens de eerder genoemde studies. De beste resultaten met een hoge transfusieratio zijn echter behaald in militaire studies en het is de vraag of deze resultaten geprojecteerd mogen worden op civiele traumapatiënten.
Er zijn namelijk verschillen tussen de beide patiëntenpopulaties, waardoor belangrijke verstorende factoren (confounders) meespelen zoals specifieke traumamechanismen, letselernst, de snelheid en mate van bloedverlies en de snelheid en het tijdstip van toediening van transfusieproducten en stollingsfactoren. Daarnaast zijn er demografische verschillen, bijvoorbeeld in leeftijd. De snelheid en mate van bloedverlies worden meestal niet gerapporteerd en het toedienen van 10 eenheden bloedproducten gedurende de eerste 12 h na opname verschilt wezenlijk van de behoefte aan 10 units tijdens de eerste 90 min van resuscitatie. Er bestaat momenteel dan ook veel discussie over de definities van een massatransfusie en ernstig acuut bloedverlies.21
In de beschreven civiele studies speelt vaak ook een belangrijke bias in tijd van overleving mee. In de onderzochte populaties was er sprake van een hoog sterftepercentage direct na binnenkomst op de traumakamer. Resultaat hiervan is een hogere mortaliteit binnen de lage transfusiegroep aangezien er geen tijd was voor het toedienen van een grote hoeveelheid FFP bij deze patiënten. 1 studie die in eerste instantie een associatie vond tussen hoge transfusieratio’s en een verbeterde overleving, concludeerde dan ook dat na correctie voor de bovenbeschreven tijdsfactor de associatie niet langer significant was.22
Naast de eerder genoemde discussiepunten maakt het retrospectieve karakter van zowel de meeste militaire als civiele studies een vergelijking tussen verschillende transfusieratio’s moeilijk. Ook de beperkte eindpunten als mortaliteit, beademingsafhankelijke dagen, ICU- en ziekenhuisopnamedagen kunnen door diverse andere factoren beïnvloed worden.
Daarnaast moet men ook rekening houden met het verhoogde risico op complicaties van hoge FFP:PRBC-ratio’s zoals multi-orgaanfalen, ARDS of ‘transfusion related acute lung injury’ (TRALI).15;17
Toekomst en aanbeveling
Op basis van de huidige studieresultaten kan nog geen uniform 1:1-transfusiebeleid worden voorgesteld voor traumapatiënten met massaal bloedverlies. Resuscitatie van de ernstig bloedende traumapatiënt is een dynamisch en complex proces en vereist een multidisciplinaire aanpak. Consensus over de behandeling wordt bemoeilijkt doordat zelden sprake is van een standaard klinische situatie. Het uitvoeren van klinische studies is daardoor ook lastig.
Het identificeren van de traumapatiënt met een ernstige coagulopathie die potentieel baat heeft bij een FFP: PRBC-ratio van 1:1 is een uitdaging. Standaard laboratoriumstollingstesten, ontwikkeld voor het monitoren van orale antistollingstherapieën, zijn niet geschikt voor het diagnosticeren en vervolgen van acute traumagerelateerde stollingsstoornissen bij de massaal bloedende patiënt. Bij standaard en routinematig toegepast stollingsonderzoek zoals protrombinetijd (PT), geactiveerde partiële tromboplastinetijd (APTT) en de INR wordt in vitro de temperatuur en de pH gecorrigeerd. Hierdoor wordt de coagulopathie onderschat. Daarnaast is er vaak een vertraging in het bekend worden van laboratoriumuitslagen. De kans wordt daardoor groter dat de patiënt te veel, dan wel te weinig transfusievloeistof krijgt toegediend.
Trombo-elastografie Mede hierdoor is hernieuwde aandacht ontstaan voor functionele stollingstesten aan het bed zoals trombo-elastografie.23 Waar standaard stollingsonderzoek informatie geeft over wanneer een stolsel zich vormt, geeft trombo-elastografie informatie over hoe een stolsel wordt gevormd en over de sterkte en stabiliteit van het gevormde stolsel. In de uitslagen wordt specifieke informatie gegeven over de mate van hyperfibrinolysis en verdunningscoagulopathie. Trombo-elastografie geeft daarmee informatie aan de clinicus over de noodzaak tot fibrinogeen- of trombocytentransfusie. Deze meting geeft dus met een eenvoudige handeling binnen 10 min meer informatie over de algehele hemostase van de patiënt dan alleen over de mate van aanwezigheid van bepaalde stollingsfactoren. Met een dergelijke analyse kunnen ook pre-existente stollingsafwijkingen gediagnosticeerd worden. Hiervan is overigens de invloed op de verbloedende traumapatiënt ook nog niet duidelijk in kaart gebracht. Met de kennis die de trombo-elastografie oplevert, zou een meer oorzakelijk gerichte therapie ingesteld kunnen worden voor de behandeling van de coagulopathie.
Deze methode zou mogelijk toepasbaar kunnen worden op de traumakamer, de operatiekamer en angiografiekamer. Onderzoek naar de accuraatheid van het diagnosticeren van een acute coagulopathie en het vervolgen van therapie en validatie van de uitslagen met betrekking tot klinische uitkomsten is momenteel gaande.
Trombocytentransfusie Een ander belangrijk punt is dat de invloed van trombocytentransfusie in combinatie met de verschillende transfusieratio’s nog niet goed onderzocht is. Trombocyten spelen een belangrijke rol binnen de hemostase. Zowel de hoeveelheid als de functie van trombocyten is bij traumapatiënten verminderd. In de praktijk wordt hier door sommigen op geanticipeerd met het toepassen van een PRBC:FFP:T-ratio (T = trombocyten) van 1:1:1. Verder onderzoek zal nodig zijn om de effecten hiervan te bepalen en om te kijken of er een maximum hoeveelheid vastgesteld kan worden, gezien de mogelijke complicaties van hoge FFP-transfusies. Tevens zou in dergelijke toekomstige studies de effecten van toediening van stollingsfactorconcentraten geanalyseerd moeten worden. In de bestaande studies zijn die namelijk niet onderzocht.
Een goede selectie van patiënten die daadwerkelijk baat zouden kunnen hebben van een transfusieratio van 1:1(:1) zou overmatig gebruik van bloedproducten kunnen voorkomen en de kosten verminderen. Belangrijk is dan ook om onderscheid te maken tussen een traumapatiënt met een dreigende verbloeding of een traumapatiënt met bloedverlies. Om patiënten met een driegende verbloeding in een vroeg stadium te kunnen identificeren, zal in toekomstig onderzoek geanalyseerd moeten worden wat de waarde is van klinische parameters naast een toestand van shock, zoals het traumamechanisme en locatie van letsels. Ook de waarde van bevindingen in het bloedonderzoek, zoals de base excess en de aanwezigheid van acidose, moet geanalyseerd worden.
Als er uiteindelijk evidencebased transfusieprotocollen voor verbloedende traumapatiënten ingevoerd gaan worden, zullen er goede logistieke voorzieningen en afspraken met de bloedbank gemaakt moeten worden voor de verhoogde aanvraag van plasmaproducten.
Toekomstig prospectief kwalitatief hoogwaardig onderzoek zal moeten uitwijzen of de gevonden positieve resultaten op de overleving daadwerkelijk het gevolg zijn van de verhoogde FFP: PRBC-ratio’s.
Conclusie
Bij traumapatiënten met al dan niet acuut massaal bloedverlies moet de coagulopathie worden gecorrigeerd. Toediening van plasmaproducten in een hoge verhouding met PRBC’s lijkt een positief effect te hebben op klinische uitkomsten in militaire studies, maar is in de meerderheid van de civiele traumapopulatie nog omstreden. Verder onderzoek naar de juiste FFP:PRBC-ratio zal deze positieve effecten moeten aantonen, waarbij ook de nadelige effecten van het toedienen van grote volumina plasma meegenomen moeten worden.
Leerpunten
-
Massaal bloedverlies na trauma kan leiden tot de dodelijke trias van acidose, hypothermie en coagulopathie.
-
Vroege correctie van acute coagulopathie bij een traumapatiënt met massaal bloedverlies is noodzakelijk.
-
Een hoge ratio van versbevroren plasma/rodebloedcelconcentraat (FFP:PRBC-ratio die nadert tot 1:1) lijkt een positief effect te hebben op de klinische uitkomsten van gewonde militairen.
-
Onnodige FFP-transfusies bij traumapatiënten zonder dreigende verbloeding geven een verhoogde kans op complicaties zoals multi-orgaanfalen en acuut respiratoir ‘distress’-syndroom.
-
Bij 90% van de traumapatiënten is het niet nodig om onmiddellijk een FFP-transfusie te geven; zij verkeren niet in ernstige hemorragische shock en hebben een adequate stolling.
Literatuur
-
Sauaia A, Moore FA, Moore EE, et al. Epidemiology of trauma deaths: a reassessment. J Trauma. 1995;38:185-93 Medline. doi:10.1097/00005373-199502000-00006
-
Cijfers ‘Gezondheid en welzijn’. Heerlen: Centraal Bureau voor de Statistiek; 2009. http://www.cbs.nl/nl-NL/menu/themas/gezondheid-welzijn/cijfers/default…
-
Peden M, McGee K, Sharma G. The injury chart book: a graphical overview of the global burden of injuries. Geneve: World Health Organization; 2002. http://whqlibdoc.who.int/publications/924156220X.pdf
-
Carrico CJ, Canizaro PC, Shires GT. Fluid resuscitation following injury: rationale for the use of balanced salt solutions. Crit Care Med. 1976;4:46-54 Medline. doi:10.1097/00003246-197603000-00002
-
Bishop MH, Shoemaker WC, Appel PL, et al. Prospective, randomized trial of survivor values of cardiac index, oxygen delivery, and oxygen consumption as resuscitation endpoints in severe trauma. J Trauma. 1995;38:780-7 Medline. doi:10.1097/00005373-199505000-00018
-
Duchesne JC, Hunt JP, Wahl G, et al. Review of current blood transfusions strategies in a mature level I trauma center: were we wrong for the last 60 years? J Trauma. 2008;65:272-6 Medline. doi:10.1097/TA.0b013e31817e5166
-
Hess JR, Brohi K, Dutton RP, Hauser CJ, Holcomb JB, Kluger Y. The Coagulopathy of Trauma: A Review of Mechanisms. J Trauma. 2008;65:748-54.
-
Spahn DR, Cerny V, Coats TJ, et al. Management of bleeding following major trauma: a European guideline. Crit Care. 2007;11:R17 Medline. doi:10.1186/cc5686
-
Brohi K, Singh J, Heron M, Coats T. Acute traumatic coagulopathy. J Trauma. 2003;54:1127-30 Medline. doi:10.1097/01.TA.0000069184.82147.06
-
MacLeod JB, Lynn M, McKenney MG, Cohn SM, Murtha M. Early coagulopathy predicts mortality in trauma. J Trauma. 2003;55:39-44 Medline. doi:10.1097/01.TA.0000075338.21177.EF
-
Borgman MA, Spinella PC, Perkins JG, et al. The ratio of blood products transfused affects mortality in patients receiving massive transfusions at a combat support hospital. J Trauma. 2007;63:805-13 Medline. doi:10.1097/TA.0b013e3181271ba3
-
Gunter OL Jr, Au BK, Isbell JM, Mowery NT, Young PP, Cotton BA. Optimizing outcomes in damage control resuscitation: identifying blood product ratios associated with improved survival. J Trauma. 2008;65:527-34 Medline. doi:10.1097/TA.0b013e3181826ddf
-
Holcomb JB, Wade CE, Michalek JE, et al. Increased plasma and platelet to red blood cell ratios improves outcome in 466 massively transfused civilian trauma patients. Ann Surg. 2008;248:447-58 Medline.
-
Maegele M, Lefering R, Paffrath T, Tjardes T, Simanski C, Bouillon B. Red-blood-cell to plasma ratios transfused during massive transfusion are associated with mortality in severe multiple injury: a retrospective analysis from the Trauma Registry of the Deutsche Gesellschaft fur Unfallchirurgie. Vox Sang. 2008;95:112-9 Medline. doi:10.1111/j.1423-0410.2008.01074.x
-
Watson GA, Sperry JL, Rosengart MR, et al. Fresh frozen plasma is independently associated with a higher risk of multiple organ failure and acute respiratory distress syndrome. J Trauma. 2009;67:221-7 Medline. doi:10.1097/TA.0b013e3181ad5957
-
Sperry JL, Ochoa JB, Gunn SR, et al. An FFP:PRBC transfusion ratio >/=1:1.5 is associated with a lower risk of mortality after massive transfusion. J Trauma. 2008;65:986-93 Medline. doi:10.1097/TA.0b013e3181878028
-
Kashuk JL, Moore EE, Johnson JL, et al. Postinjury life threatening coagulopathy: is 1:1 fresh frozen plasma:packed red blood cells the answer? J Trauma. 2008;65:261-70 Medline. doi:10.1097/TA.0b013e31817de3e1
-
Scalea TM, Bochicchio KM, Lumpkins K, et al. Early aggressive use of fresh frozen plasma does not improve outcome in critically injured trauma patients. Ann Surg. 2008;248:578-84 Medline.
-
Teixeira PG, Inaba K, Shulman I, et al. Impact of plasma transfusion in massively transfused trauma patients. J Trauma. 2009;66:693-7 Medline. doi:10.1097/TA.0b013e31817e5c77
-
Holcomb JB, Jenkins D, Rhee P, et al. Damage control resuscitation: directly addressing the early coagulopathy of trauma. J Trauma. 2007;62:307-10 Medline. doi:10.1097/TA.0b013e3180324124
-
Riskin DJ, Tsai TC, Riskin L, et al. Massive transfusion protocols: the role of aggressive resuscitation versus product ratio in mortality reduction. J Am Coll Surg. 2009;209:198-205 Medline. doi:10.1016/j.jamcollsurg.2009.04.016
-
Snyder CW, Weinberg JA, McGwin G Jr, et al. The relationship of blood product ratio to mortality: survival benefit or survival bias? J Trauma. 2009;66:358-62 Medline. doi:10.1097/TA.0b013e318196c3ac
-
Martini WZ, Cortez DS, Dubick MA, Park MS, Holcomb JB. Thrombelastography is better than PT, aPTT, and activated clotting time in detecting clinically relevant clotting abnormalities after hypothermia, hemorrhagic shock and resuscitation in pigs. J Trauma. 2008;65:535-43 Medline. doi:10.1097/TA.0b013e31818379a6





Reacties