Op de hoogte blijven van nieuwe leerartikelen, compleet met geaccrediteerde toetsvragen en luisterversie?
⚡Schrijf je gratis in op een e-mail alert door het dossier leerartikelen te volgen.⚡
De impact van osteoporotische fracturen op het dagelijks functioneren is aanzienlijk, onder andere door pijn, afgenomen zelfstandigheid en verlies aan arbeidscapaciteit. De beschikbare diagnostiek en goedkope behandelopties maken osteoporose geschikt voor primaire en secundaire preventie. In dit leerartikel geven wij antwoord op vragen uit de praktijk over osteoporose.
Toets voor nascholing (verlopen)
Aan dit leerartikel was een toets gekoppeld waarmee je nascholingspunten kon verdienen.
Leerdoelen
- Overzicht krijgen van de risicofactoren en onderliggende oorzaken van osteoporose.
- Diagnostiek van osteoporose kennen en het fractuurrisico van de individuele patiënt kunnen inschatten.
- Op de hoogte zijn van de medicamenteuze en niet-medicamenteuze behandelopties van osteoporose.
- De optimale behandelduur en follow-up van patiënten met osteoporose kunnen bepalen.
artikel
Primaire osteoporose is een chronische aandoening die voornamelijk op oudere leeftijd en bij vrouwen voorkomt. De aandoening wordt gekarakteriseerd door een verlaagde botdichtheid en een veranderde microarchitectuur van het bot, die resulteren in een verminderde botsterkte en daardoor een verhoogd fractuurrisico. Osteoporose wordt lang niet altijd gediagnosticeerd, waardoor mensen met primaire osteoporose ook lang niet allemaal adequaat behandeld worden. Dat leidt in combinatie met de toenemende vergrijzing tot een toenemend aantal fracturen.
Epidemiologie
Hoe vaak komt osteoporose voor en wat zijn de risicofactoren?
In 2018 hadden naar schatting 495.000 mensen osteoporose, van wie ruim 80% vrouw, afgaand op huisartsenregistraties.1 Nederlandse cijfers uit 2010 laten zien dat het totaal aantal klinische fracturen bij mensen ouder dan 50 jaar bijna 120.000 bedroeg, waarvan 40.000 op basis van aangetoonde osteoporose. Geschat wordt dat het aantal osteoporotische fracturen toeneemt tot 55.000 in 2030.2
Het merendeel van de fracturen komt voor bij patiënten zonder osteoporose.3,4 Daarom is er in de literatuur en huidige richtlijnen meer aandacht voor het inschatten van het fractuurrisico, waar het vaststellen van osteoporose een onderdeel van is. De risicofactoren voor osteoporose zijn weergegeven in tabel 1.
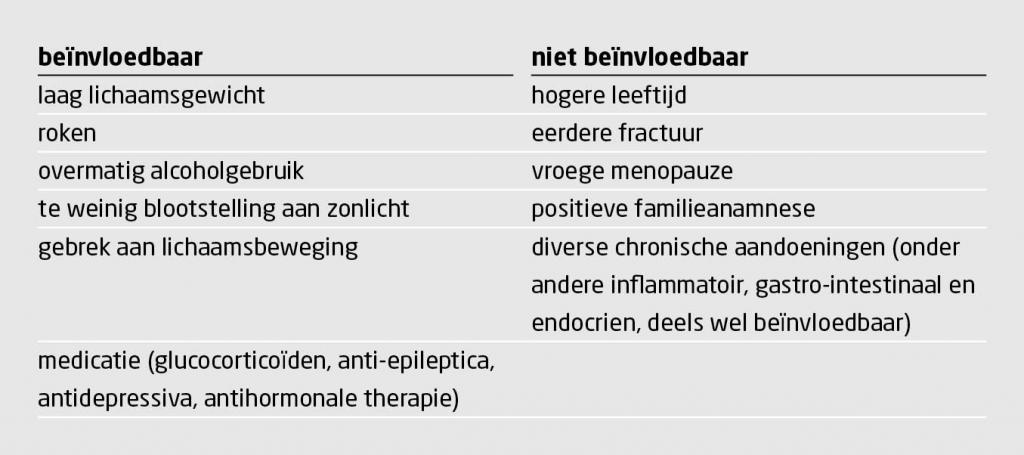
Diagnostiek
Is het zinvol om te screenen op osteoporose? Zo ja, bij welke patiënten?
De Nederlandse richtlijn ‘Osteoporose en fractuurpreventie’ adviseert om in de vorm van ‘case-finding’ na te gaan of er sprake is van osteoporose bij patiënten met een hoog fractuurrisico (tabel 2).5 Bij een fractuurrisicoscore van ten minste 4 punten is aanvullend onderzoek naar de botmineraaldichtheid (BMD) en wervelinzakkingen geïndiceerd.5,6 De best gevalideerde meetmethode voor BMD is de ‘dual-energy X-ray absorptiometry’(DEXA)-scan.5 Omdat vooral in het eerste jaar na een fractuur het risico op nieuwe fracturen sterk verhoogd is, wordt geadviseerd de analyse kort na de fractuur te verrichten.7

Screenen op osteoporose in de algemene populatie met een DEXA-meting is weinig effectief, aangezien de meeste fracturen voorkomen bij patiënten zonder osteoporose. De ‘number needed to screen’ – het aantal personen dat je moet screenen om één fractuur te voorkomen – ligt boven de 200.8
Hoe wordt de diagnose ‘osteoporose’ gesteld?
Bij een BMD-meting wordt een zogenoemde T-score bepaald van de lumbale wervelkolom, de heup en specifiek de femurhals. De T-score is het aantal standaarddeviaties (SD) waarmee de BMD van de patiënt afwijkt van die van een jongvolwassene (30 jaar) van hetzelfde geslacht.
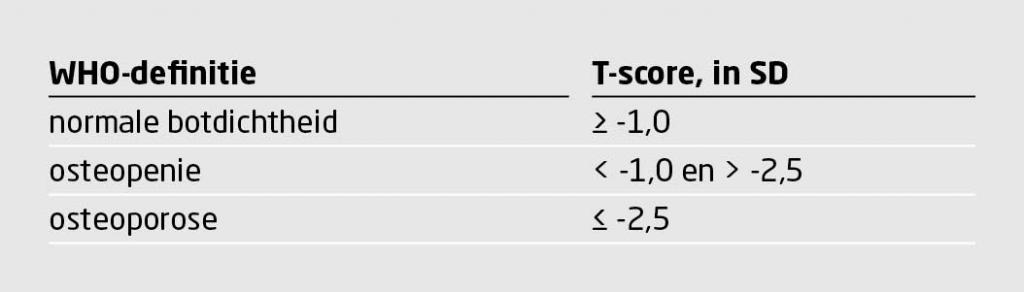
De WHO-definitie van de diagnose ‘osteoporose’ gaat uit van de laagste T-score voor de BMD (tabel 3).9 Bij een DEXA-meting hoort een ‘vertebral fracture assessment’ (VFA) om de aanwezigheid van wervelinzakkingen te beoordelen. Een wervelinzakking ≥ 25% wordt beschouwd als klinisch relevant. Figuur 1 geeft een praktijkvoorbeeld van een DEXA-scan en VFA-meting.10
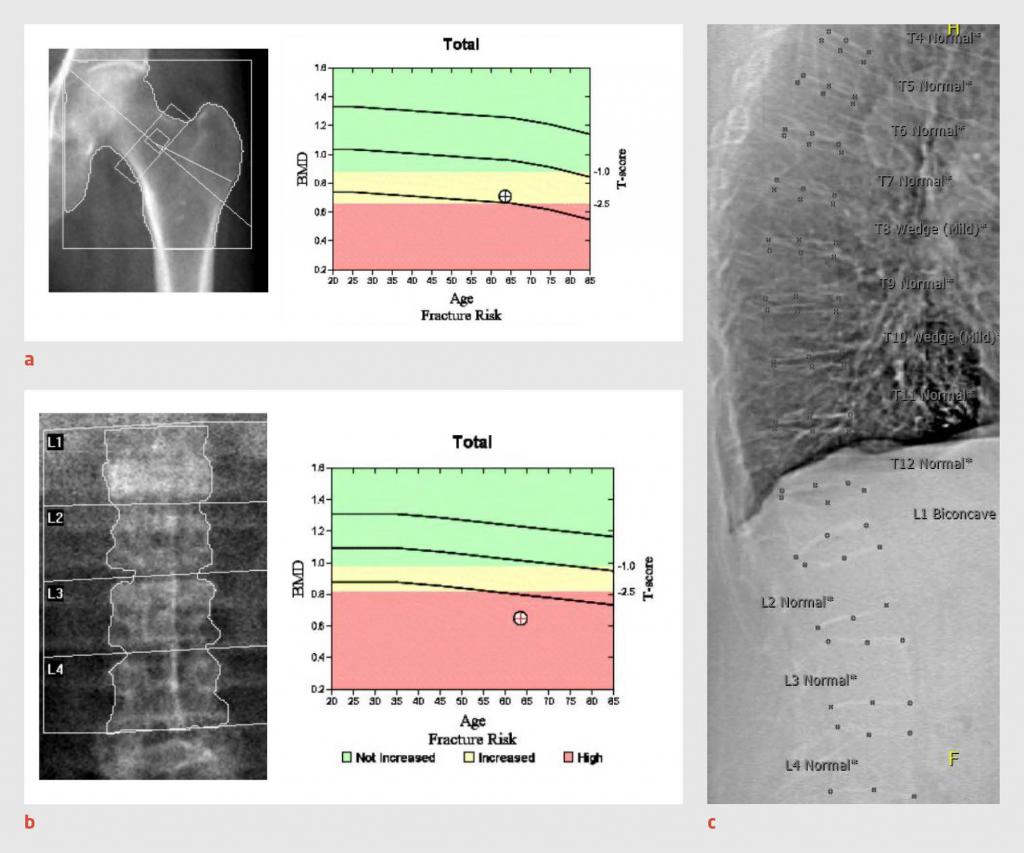
Hoe wordt het fractuurrisico ingeschat?
De ‘fracture risk assesment tool’ (FRAX) kan gebruikt worden als na de DEXA nog onduidelijk is of de patiënt wel voor osteoporose behandeld moet worden. Op basis van risicofactoren, zonder of met een BMD-meting, berekent het FRAX-model het 10-jaarsrisico op een heupfractuur en op een osteoporotische fractuur (heup-, proximale humerus-, pols- en klinische wervelfractuur). Het FRAX-model is gevalideerd voor de Nederlandse populatie van 40-90 jaar.11,12 Een fractuurrisico wordt in de literatuur als ‘hoog’ beschouwd bij de aanwezigheid van een heup- of wervelfractuur, of een BMD-T-score ≤ -2,5 SD, of een FRAX-score ≥ 3% of ≥ 20% voor respectievelijk heupfractuur en osteoporotische fracturen. Een matig verhoogd fractuurrisico wordt gedefinieerd als osteopenie zonder eerdere wervel- of heupfractuur met een FRAX-score < 3% en < 20% voor respectievelijk heup- en osteoporotische fracturen. Is hierbij de BMD-T-score > -1,0 SD, dan wordt het fractuurrisico als ‘laag’ ingeschat.
Bij welke patiënten is welk laboratoriumonderzoek geïndiceerd?
Als er een indicatie is om te behandelen, worden een uitgebreide anamnese, lichamelijk onderzoek en bloedonderzoek geadviseerd om secundaire oorzaken van osteoporose uit te sluiten (tabel 4).

In tabel 5 wordt de aanbevolen diagnostiek per patiëntengroep weergegeven. Omdat secundaire osteoporose vaker voorkomt bij patiënten met een recente fractuur dan bij patiënten zonder fractuur, wordt onderscheid gemaakt tussen deze groepen. Bepaling van 25-hydroxyvitamine D wordt geadviseerd bij verdenking op een zeer ernstig vitamine D-tekort of wanneer suppletie met 800 IE per dag, zoals de huidige richtlijnen adviseren, onvoldoende wordt geacht door een probleem met de inname of opname (malabsorptie).13 Als er aanwijzingen zijn voor secundaire osteoporose kan gericht aanvullende diagnostiek worden ingezet naar de onderliggende oorzaken. Extreme osteoporose op jonge leeftijd verdient aparte aandacht en valt buiten beschouwing van dit artikel. Botmarkers als N-terminaal procollageen type 1 (P1NP) en C-terminaal telopeptide type 1 collageen (CTx) hebben geen plaats in de diagnostiek.14
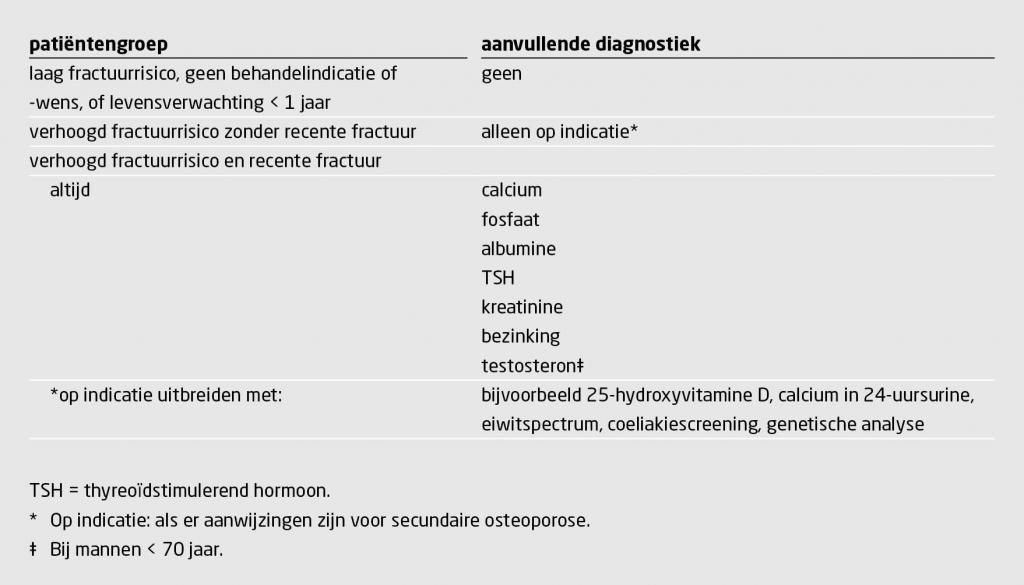
Behandeling en follow-up
Welke niet-medicamenteuze adviezen zijn er voor osteoporose?
Het doel van de behandeling bij een verhoogd fractuurrisico is het voorkomen van nieuwe fracturen. Voor iedereen gelden leefstijl- en voedingsadviezen. De leefstijladviezen bestaan uit lichaamsbeweging (minstens 150 minuten per week matig intensieve inspanning verspreid over diverse dagen), stoppen met roken, matigen van alcoholgebruik, een gevarieerd eetpatroon en voldoende blootstelling aan zonlicht.5 De aanbevolen calciuminname is minimaal 1000-1200 mg per dag, wat gelijk staat aan gezonde voeding met circa 3-4 zuivelconsumpties per dag. Bij onvoldoende calciuminname wordt geadviseerd dit aan te vullen met supplementen. Voor iedere patiënt met osteoporose is het advies om 800 IE (20 μg) vitamine D per dag te gebruiken.
Daarnaast is het essentieel voor iedere patiënt het valrisico in te schatten. Bij een verhoogd valrisico kan een valpreventieprogramma nuttig zijn.
Welke medicamenteuze opties zijn er voor osteoporose?
Als er sprake is van een behandelindicatie omdat het fractuurrisico verhoogd is, moet de winst van de medicamenteuze behandeling met de bijbehorende voor- en nadelen met de patiënt worden besproken. De FRAX-score kan gebruikt worden voor de gezamenlijke besluitvorming. De medicamenteuze opties kunnen verdeeld worden in twee groepen: remmers van de botafbraak (osteoclasten) en middelen die de botaanmaak (osteoblasten) stimuleren. Bisfosfonaten, denosumab en raloxifeen behoren tot de eerste groep en teriparatide is een middel dat de botaanmaak stimuleert. Bisfosfonaten zijn beschikbaar in meer dan 10 verschillende preparaten. De meeste fractuurstudies zijn verricht met alendroninezuur, risedroninezuur (orale preparaten) en zoledroninezuur (intraveneus).
Tabel 6 laat zien welke risicoreductie van de afzonderlijke middelen te verwachten is, met de kanttekening dat een directe vergelijking van middelen onderling niet gerechtvaardigd is, vanwege verschillen in studiepopulatie, therapie- en observatieduur.15-18
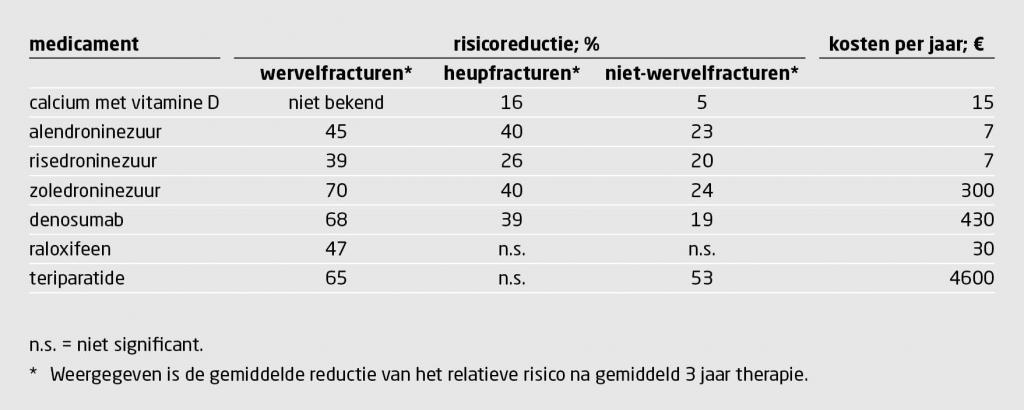
Welk middel de eerste keus verdient, wordt bepaald op basis van het fractuurrisico en andere patiëntfactoren (figuur 2). Orale bisfosfonaten zijn voor het merendeel van de patiënten een effectieve, relatief veilige en goedkope eerste keus. De belangrijkste frequente bijwerkingen zijn gastro-intestinale klachten en musculoskeletale pijn. Wanneer de patiënt bisfosfonaten in tabletvorm niet verdraagt, kunnen zij in drankvorm of parenteraal worden aangeboden; bij gastro-intestinale intolerantie en bij hoog-risicopatiënten wordt parenterale toediening geadviseerd.

Teriparatide Teriparatide (recombinant parathyreoïdhormoon, eenmaal daags subcutane toediening) is toegankelijker geworden voor de behandeling van patiënten met een verhoogd fractuurrisico doordat de vergoedingscriteria vervallen zijn. Het kan als therapie van eerste keus overwogen worden bij hoog-risicogroepen, zoals patiënten met twee matig-ernstige wervelfracturen (graad 2) of één ernstige wervelfractuur (graad 3) en een T-score ≤ 1,5. Belangrijk is dat een terugval van de BMD wordt gezien wanneer een patiënt is gestopt met teriparatide; zo’n terugval kan voorkomen worden door nabehandeling met een antiresorptief middel.
Denosumab Denosumab is een effectief middel – de effectiviteit is vergelijkbaar met die van bisfosfonaten – met als voordeel dat het halfjaarlijks met een subcutane injectie toegediend kan worden. Een groot nadeel is echter dat denosumab een reboundeffect geeft wanneer de patiënt met dit middel stopt en dat het fractuurrisico na staken duidelijk verhoogd is, met name het risico op wervelinzakkingen; dat is ook de reden dat dit middel beperkt als behandeling van eerste keus wordt ingezet. Aansluitend moet de patiënt dus altijd met andere antiresorptieve therapie beginnen. Een goede optie kan zijn om minimaal éénmaal zolendroninezuur toe te dienen als nabehandeling. Anabole therapie na het staken van denosumab lijkt ongunstiger uit te pakken en wordt niet geadviseerd.16
Raloxifeen De plaats van raloxifeen, een selectieve oestrogeenreceptormodulator, in de behandeling van osteoporose is beperkt. Dit middel kan als alternatief worden gegeven bij intolerantie of een contra-indicatie voor bisfosfonaten en denosumab, of aan patiënten met een hoog risico op mammacarcinoom, gezien het oestrogeenantagonerende effect op het borstklierweefsel. Nadelen van raloxifeen zijn de beperkte effectiviteit en een ongunstig bijwerkingenprofiel, waaronder een verhoogd tromboserisico.17
Wat is de optimale duur van medicamenteuze therapie?
De optimale duur van de behandeling varieert per middel. Voor orale bisfosfonaten wordt geadviseerd gedurende 5 jaar te behandelen om vervolgens het fractuurrisico opnieuw te bepalen met DEXA en een VFA-meting. Voor zoledroninezuur geldt een evaluatietermijn van 3 jaar. Wanneer het fractuurrisico na 5 respectievelijk 3 jaar matig tot laag is en de BMD-T-score van de heup en femurhals ≥ -2,5 bedraagt, kan gezien de lange werkingsduur van bisfosfonaten een therapiepauze worden ingelast waarin om de 2 à 3 jaar het fractuurrisico opnieuw bepaald moet worden middels DEXA en VFA. Wanneer het fractuurrisico na 5 respectievelijk 3 jaar nog steeds verhoogd is, kan een oraal bisfosfonaat gedurende 10 jaar en zoledroninezuur in totaal 6 jaar veilig worden gecontinueerd; de winst hiervan is een kleine daling in het risico op nieuwe wervelfracturen.19,20 De risico’s bij langdurig bisfosfonaatgebruik zijn, hoewel zeer zeldzaam, het optreden van een atypische femurfractuur en osteonecrose van de kaak. Als het fractuurrisico na het staken van de therapie weer toeneemt, kan besloten worden om opnieuw met bisfosfonaten te beginnen of een andere therapie te geven.16
Voor denosumab luidt het advies om na behandeling gedurende 5 jaar het fractuurrisico te evalueren en als dit risico nog steeds verhoogd is, nog eens 5 jaar te behandelen met denosumab of een alternatief middel.21
De therapietrouw voor osteoporosemedicatie is vaak beperkt. Het is belangrijk om de therapietrouw te bespreken wanneer de patiënt met de medicatie begonnen is. Bij twijfel aan de therapietrouw kan eerdere follow-up na 3-6 maanden plaatsvinden met bepaling van markers voor de botturn-over, of na 2 jaar met een DEXA-scan.22
Zijn er contra-indicaties voor medicatie tegen osteoporose?
Een belangrijke contra-indicatie voor osteoporosemedicatie is een verminderde nierfunctie (eGFR < 30 ml/min). Omdat het bij patiënten met een verminderde nierfunctie moeilijk is om onderscheid te maken tussen adynamisch bot (lage botturn-over) en hyperdynamisch bot (hoge botturn-over) kan soms een botbiopt geïndiceerd zijn. In het algemeen geldt dat het goed is deze patiënten te verwijzen naar een gespecialiseerde nefroloog of endocrinoloog voor analyse en behandeling.
Gebitsproblemen kunnen soms een reden zijn de behandeling met bisfosfonaten of denosumab uit te stellen, gezien het risico op het ontwikkelen van kaaknecrose.23
Er is geen leeftijdsbeperking bij de medicamenteuze behandeling van osteoporose.
Wat te doen bij patiënten die glucocorticoïden gebruiken?
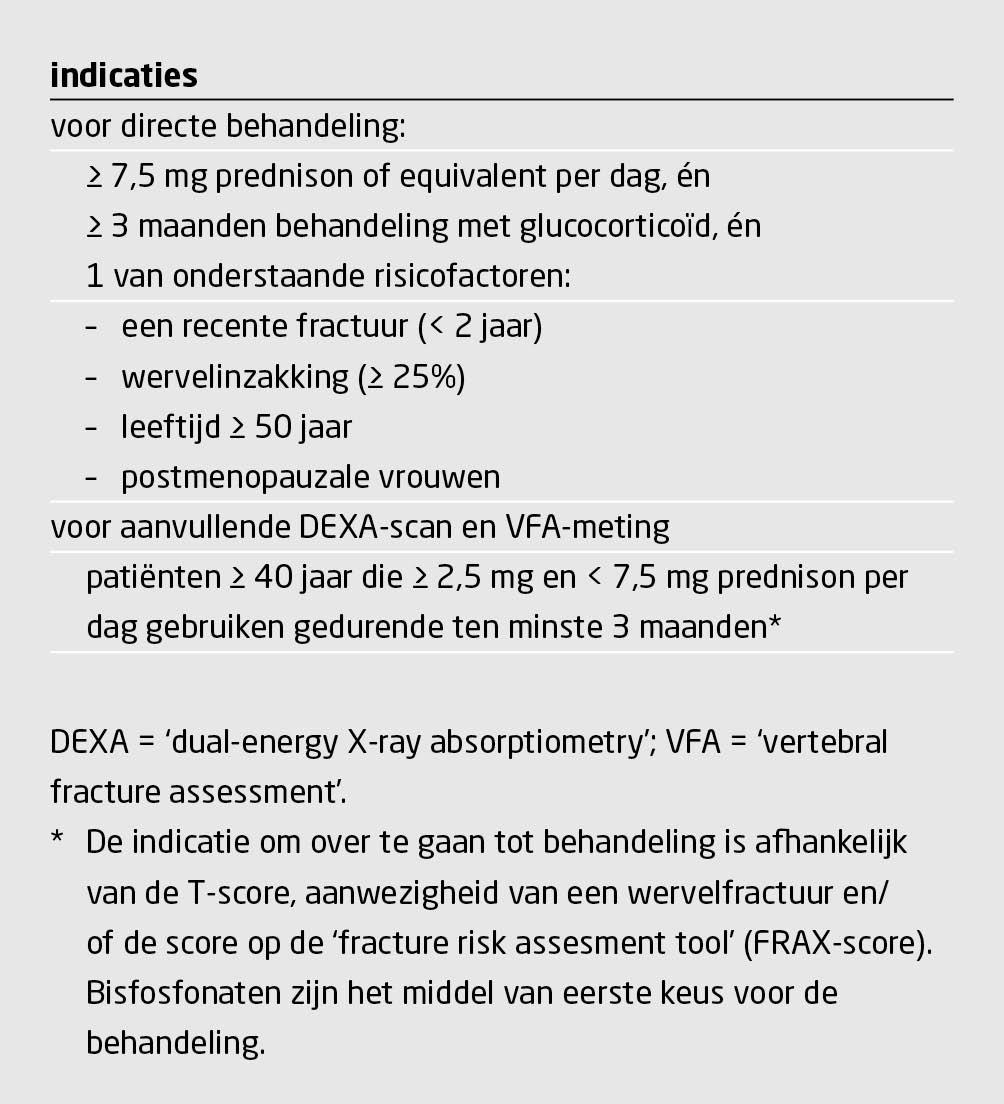
Glucocorticoïd-geïnduceerde osteoporose is de meest voorkomende vorm van secundaire osteoporose. Deze vorm uit zich met name in fracturen van het trabeculaire bot (wervels en ribben). Bij gebruik van systemische glucocorticoïden is het noodzakelijk om direct te beginnen met osteoporosepreventie. Algemene maatregelen voor iedere patiënt die een glucocorticoïd gebruikt zijn de inname van voldoende calcium en vitamine D, valpreventie, stoppen met roken en het beperken van alcoholgebruik. Bij patiënten die een hoge dosering prednison gebruiken is het fractuurrisico vooral hoog door de combinatie met een hoge ziekteactiviteit.24 Tabel 7 geeft adviezen voor osteoporosepreventie bij gebruik van systemische glucocorticoïden. Orale bisfosfonaten zijn eerste keus, maar een sterk verhoogd fractuurrisico kan een reden zijn direct te beginnen met een parenteraal middel als denosumab, teriparatide of zoledroninezuur.25
Wat zijn de toekomstige ontwikkelingen?
In de komende jaren wordt een nieuwe Nederlandse richtlijn over osteoporose en fractuurpreventie verwacht. Het nieuwe medicijn romosozumab is in december 2019 goedgekeurd door het Europese medicijnagentschap (EMA). Dit is een monoklonaal antilichaam dat via remming van sclerostine de botaanmaak stimuleert. Het dient maandelijks te worden geïnjecteerd gedurende een periode van 12 maanden en laat een sterke afname zien van wervel- en niet-wervelfracturen in vergelijking met placebo en met alendronaat.26
Tot besluit
Dit artikel biedt een op de dagelijkse praktijk gericht overzicht van de etiologie van osteoporose, onderliggende oorzaken en de aanbevolen diagnostiek en behandeling bij patiënten met een verhoogd fractuurrisico (figuur 3). Wanneer osteoporose is vastgesteld, zijn leefstijladviezen en behandeling met calcium en vitamine D geïndiceerd, in combinatie met medicatie tegen osteoporose. Het doel van de behandeling is de vermindering van het risico op nieuwe fracturen en de daarmee gepaard gaande comorbiditeit.

Literatuur
-
Volksgezondheid en zorg. Osteoporose. www.volksgezondheidenzorg.info/onderwerp/osteoporose, geraadpleegd op 13 juli 2020.
-
Lötters FJ, van den Bergh JP, de Vries F, Rutten-van Mölken MP. Current and future incidence and costs of osteoporosis-related fractures in The Netherlands: combining claims data with BMD measurements. Calcif Tissue Int. 2016;98:235-43. doi:10.1007/s00223-015-0089-z. Medline
-
Van der Velde RY, Wyers CE, Geusens P, et al. Incidence of subsequent fractures in the UK between 1990 and 2012 among individuals 50 years or older. Osteoporosis Int. 2018;29:2469-75. Medline
-
Malgo F, Appelman-Dijkstra NM, Termaat MF, et al. High prevalence of secondary factors for bone fragility in patients with a recent fracture independently of BMD. Arch Osteoporos. 2016;11:12. doi:10.1007/s11657-016-0258-3. Medline
-
Richtlijn Osteoporose en Fractuurpreventie – derde herziening (2011). Utrecht: Nederlandse Vereniging voor Reumatologie; 2011.
-
Elders PJM, Dinant GJ, van Geel T, et al. NHG-standaard Fractuurpreventie (tweede herziening). Utrecht: Nederlands Huisartsen Genootschap; 2012.
-
Van Geel TA, Huntjens KM, van den Bergh JP, Dinant GJ, Geusens PP. Timing of subsequent fractures after an initial fracture. Curr Osteoporos Rep. 2010;8:118-22. doi:10.1007/s11914-010-0023-2. Medline
-
Merlijn T, Swart KMA, van der Horst HE, Netelenbos JC, Elders PJM. Fracture prevention by screening for high fracture risk: a systematic review and meta-analysis. Osteoporosis Int. 2020;31:251-7. Medline
-
Kanis JA. Assessment of fracture risk and its application to screening for postmenopausal osteoporosis: synopsis of a WHO report. WHO Study Group. Osteoporosis Int. 1994;4:368-81. Medline
-
Genant HK, Wu CY, van Kuijk C, Nevitt MC. Vertebral fracture assessment using a semiquantitative technique. J Bone Miner Res. 1993;8:1137-48.
-
Fracture Risk Assessment Tool. www.sheffield.ac.uk/FRAX, geraadpleegd op 13 juli 2020.
-
Lalmohamed A, Welsing PM, Lems WF, et al. Calibration of FRAX 3.1 to the Dutch population with data on the epidemiology of hip fractures. Osteoporosis Int. 2012;23:861-9. Medline
-
Bours SP, van den Bergh JP, van Geel TA, Geusens PP. Secondary osteoporosis and metabolic bone disease in patients 50 years and older with osteoporosis or with a recent clinical fracture: a clinical perspective. Curr Opin Rheumatol. 2014;26:430-9. doi:10.1097/BOR.0000000000000074. Medline
-
Vlot MC, den Heijer M, de Jongh RT, et al. Clinical utility of bone markers in various diseases. Bone. 2018;114:215-25. doi:10.1016/j.bone.2018.06.011. Medline
-
European Medicines Agency. Summary of Product Characteristics - Teriparatide. Londen: EMA; 2019.
-
Eastell R, Rosen CJ, Black DM, Cheung AM, Murad MH, Shoback D. Pharmacological management of osteoporosis in postmenopausal women: an endocrine society clinical practice guideline. J Clin Endocrinol Metab. 2019;104:1595-622. doi:10.1210/jc.2019-00221. Medline
-
Ettinger B, Black DM, Mitlak BH, et al; Multiple Outcomes of Raloxifene Evaluation (MORE) Investigators. Reduction of vertebral fracture risk in postmenopausal women with osteoporosis treated with raloxifene: results from a 3-year randomized clinical trial. JAMA. 1999;282:637-45. doi:10.1001/jama.282.7.637. Medline
-
Bouillon R, Marcocci C, Carmeliet G, et al. Skeletal and extraskeletal actions of vitamin D: current evidence and outstanding questions. Endocr Rev. 2019;40:1109-51. doi:10.1210/er.2018-00126. Medline
-
Black DM, Schwartz AV, Ensrud KE, et al; FLEX Research Group. Effects of continuing or stopping alendronate after 5 years of treatment: the Fracture Intervention Trial Long-term Extension (FLEX): a randomized trial. JAMA. 2006;296:2927-38. doi:10.1001/jama.296.24.2927. Medline
-
Black DM, Reid IR, Boonen S, et al. The effect of 3 versus 6 years of zoledronic acid treatment of osteoporosis: a randomized extension to the HORIZON-Pivotal Fracture Trial (PFT). J Bone Miner Res. 2012;27:243-54. Medline
-
Bone HG, Wagman RB, Brandi ML, et al. 10 years of denosumab treatment in postmenopausal women with osteoporosis: results from the phase 3 randomised FREEDOM trial and open-label extension. Lancet Diabetes Endocrinol. 2017;5:513-23. doi:10.1016/S2213-8587(17)30138-9. Medline
-
Silverman S, Gold DT. Compliance and persistence with osteoporosis medications: a critical review of the literature. Rev Endocr Metab Disord. 2010;11:275-80. doi:10.1007/s11154-010-9138-0. Medline
-
Iskender SY, Eekhof EMW, van der Waal I. Bisfosfonaatgerelateerde osteonecrose van de kaak. Ned Tijdschr Tandheelkd. 2012;119:206-11. doi:10.5177/ntvt.2012.04.11203.
-
Buckley L, Humphrey MB. Glucocorticoid-Induced Osteoporosis. N Engl J Med. 2018;379:2547-56. doi:10.1056/NEJMcp1800214. Medline
-
Raterman HG, Bultink IEM, Lems WF. Current treatments and new developments in the management of glucocorticoid-induced osteoporosis. Drugs. 2019;79:1065-87. doi:10.1007/s40265-019-01145-6. Medline
-
Cosman F, Crittenden DB, Grauer A. Romosozumab treatment in postmenopausal osteoporosis. N Engl J Med. 2017;376:396-7 Medline.




Depoprovera en osteoporose
Hoewel Depoprovera een anticonceptief middel is dat steeds minder wordt voorgeschreven, is het wel een aandachtspunt dat langdurig gebruik ervan het risico op osteoporose verhoogt.
Arja van Wijgerden, huisarts