Samenvatting
- De meest voorkomende vormen van huidkanker zijn het basaalcelcarcinoom (BCC) en het plaveiselcelcarcinoom (PCC).
- Conventionele excisie is nog steeds de behandeling van eerste keus bij deze maligne tumoren.
- Gezien de vele subtypes en de hoge incidentie is behandeling van deze huidtumoren niet enkel een kwestie van chirurgisch ingrijpen. Er diverse therapeutische mogelijkheden, van smeren tot snijden.
- Behandelaars van patiënten met non-melanoma huidkanker moeten op de hoogte zijn van de voor- en nadelen van de vele behandelopties.
- Bij de chirurgische behandeling is radicaliteit gewenst, maar moeten ruime marges vermeden worden.
- Micrografische chirurgie volgens Mohs is een behandelmogelijkheid voor BCC’s en PCC’s in het gelaat.
- Superficiële BCC’s kunnen op diverse niet-invasieve manieren effectief behandeld worden met een optimaal cosmetisch resultaat.
artikel
Elders in het themanummer ‘Dermatologie’ kunt u lezen dat de incidentie van huidkanker nog steeds stijgt. Ondanks preventieve campagnes waarin duidelijk wordt gemaakt dat overmatige zonblootstelling huidkanker kan veroorzaken, hebben deze niet gezorgd voor een gedragsverandering bij de mens en een daling van de incidentiecijfers. Naar schatting zal ongeveer 1 op de 6 Nederlanders huidkanker krijgen voor het 85e levensjaar. Omdat veel patiënten verschillende of meerdere dezelfde vormen van huidkanker krijgen, is de behandeldruk voor dermatologen en andere behandelaars nog hoger. Hierdoor bestaat er een constante zoektocht naar de meest effectieve en kosteneffectieve behandeling.
Dit artikel richt zich op de behandeling van de 2 meest voorkomende huidkankers, het basaalcelcarcinoom (BCC) en het plaveiselcelcarcinoom (PCC). Deze zijn tezamen goed voor circa 90% van alle maligniteiten van de huid. Klik HIER voor stroomdiagrammen van de zoekacties van de auteurs naar literatuur over de behandeling van het BCC en het PCC. Deze stroomdiagrammen zijn niet eindredactioneel bewerkt door het NTvG.
Kliniek
Basaalcelcarcinoom
Een BCC ontstaat waarschijnlijk vanuit pluripotente stamcellen in het stratum basale van de huid of vanuit epitheelcellen van een haarfollikel. Mutaties in genen die coderen voor eiwitten die betrokken zijn bij de signaaltransductie in de zogenoemde ‘hedgehog pathway’ vervullen een rol bij het erfelijke basaalcelnaevussyndoom en bij het sporadisch BCC.1 Naast deze genetische factoren zijn ook ander factoren causaal gerelateerd aan het ontstaan van een BCC, zoals overmatige zonexpositie, zonschade op jonge leeftijd, radiotherapie in het verleden en arseengebruik. Onder invloed van UV-straling kunnen nucleotideveranderingen ontstaan in de tumorsupressorgenen p53 en ‘patched homolog’(PTCH)-1. Dergelijke DNA-schade speelt een rol bij de vroege ontwikkeling van een BCC.2 Een BCC kan zich presenteren als een erythemateuze, schilferende plaque, een erythemateuze papel die gemakkelijk bloedt, een ulcus of als een verlittekenend huidgebied (figuren 1a-c). Met histologisch onderzoek kan de klinische diagnose worden bevestigd en het subtype van de tumor worden bepaald.
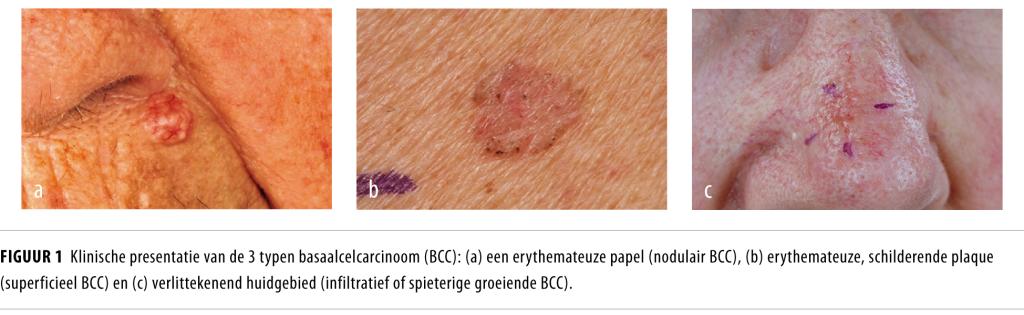
Er zijn verschillende typen BCC, die zowel klinisch als histologisch van elkaar onderscheiden kunnen worden. Deze onderverdeling is belangrijk, aangezien de kans op een lokaal recidief en de behandeling daarvan verschillen. Men onderscheidt 3 grote groepen BCC op basis van het beeld bij histologisch onderzoek, te weten superficiële BCC’s, nodulaire BCC’s en infiltratieve of sprieterig groeiende BCC’s (figuren 2a-c).
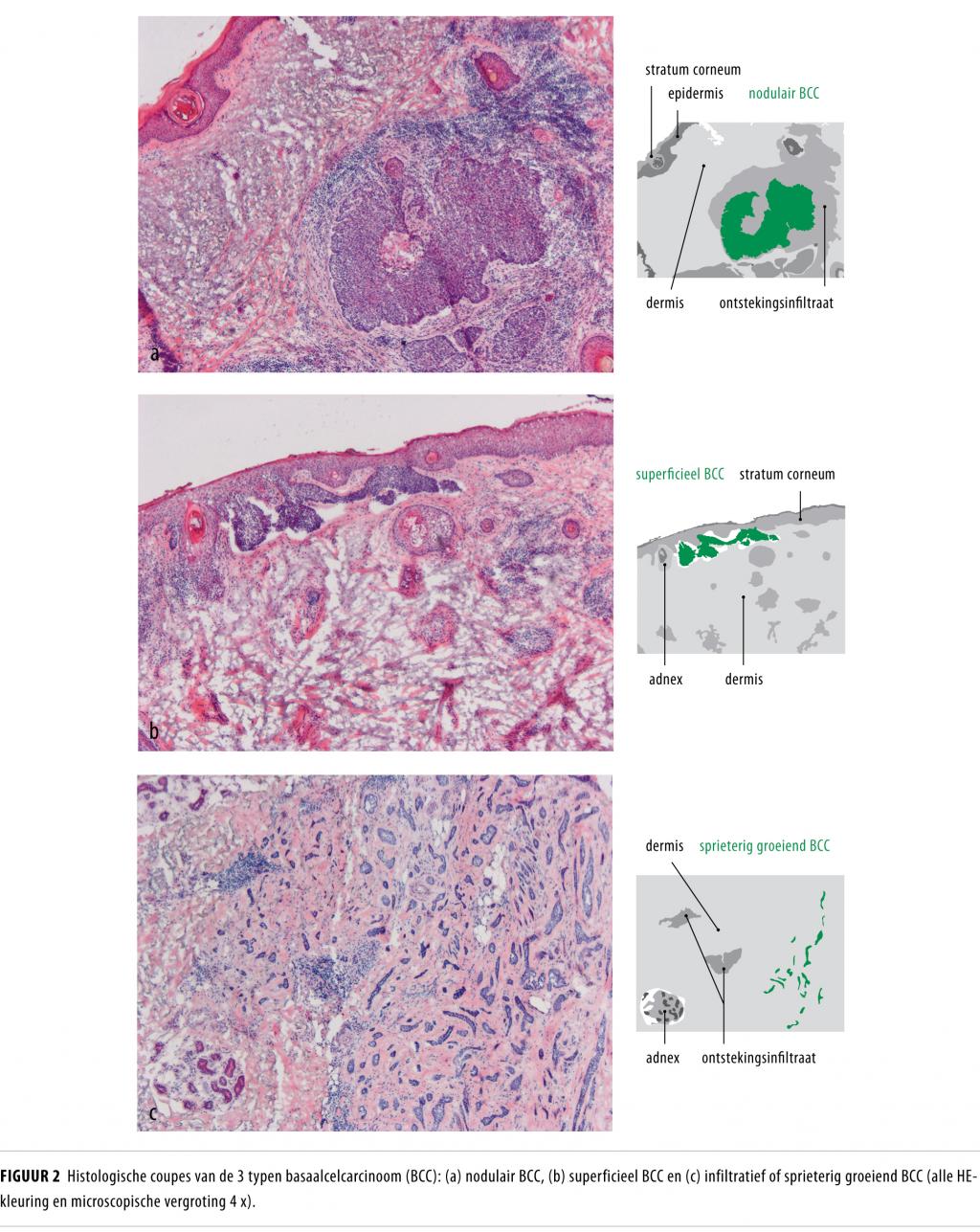
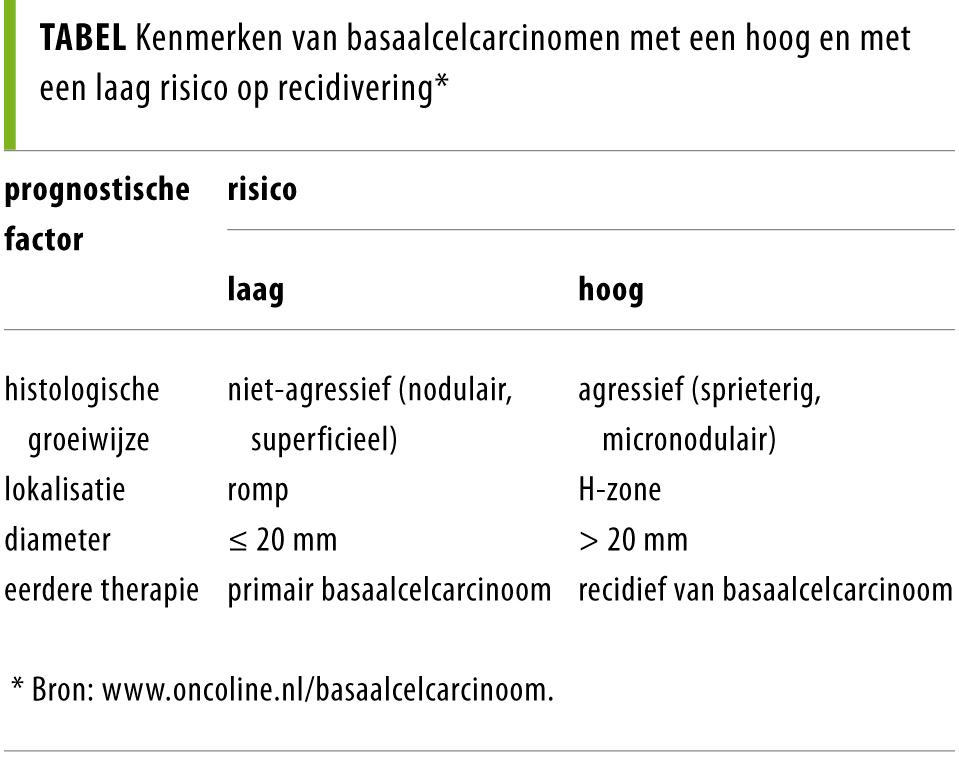
De prognose van BCC’s is over het algemeen goed; metastasen zijn bij deze vorm van huidkanker uitzonderlijk, wel kan er lokale doorgroei in onderliggende weefsels optreden. Vooral BCC’s in de zogenoemde H-zone (dit is het gebied rond de ogen, de oren en de neus), sprieterig groeiende BCC’s en grote tumoren hebben een uitgebreide, subklinische groeiwijze en een hogere recidiefkans (tabel).3,4 Adequate therapie van een primair BCC is essentieel, omdat recidieven moeilijker te behandelen zijn en kunnen leiden tot ernstige cosmetische en functionele klachten.5
Na histologisch onderzoek is aanvullende diagnostiek slechts zelden noodzakelijk. Een CT- of MRI-scan kan geïndiceerd zijn bij onduidelijkheden over eventuele doorgroei in onderliggende weke delen of bot.
Plaveiselcelcarcinoom
Een PCC ontstaat uit keratinocyten, met name als gevolg van overmatige blootstelling aan schadelijke UV-straling. Een PCC kan de novo ontstaan of uit een premaligne afwijking zoals actinische keratose en de ziekte van Bowen (PCC in situ). Mensen met een lichte huid en personen die langdurig aan zonlicht zijn blootgesteld, hebben een sterk verhoogd risico op het ontwikkelen van een PCC.6 UVB-straling speelt hierbij de belangrijkste rol; UVA-straling levert een extra bijdrage door directe remming van het immuunsysteem.7 Patiënten die immuunmodulerende medicijnen gebruiken na orgaantransplantatie of patiënten die om andere redenen een gestoord immuunsysteem hebben, lopen een verhoogd risico op het ontwikkelen van multipele PCC’s.8 Ook het humaan papillomavirus speelt een rol in de ontwikkeling van het PCC, met name bij immuungecompromitteerde patiënten.9
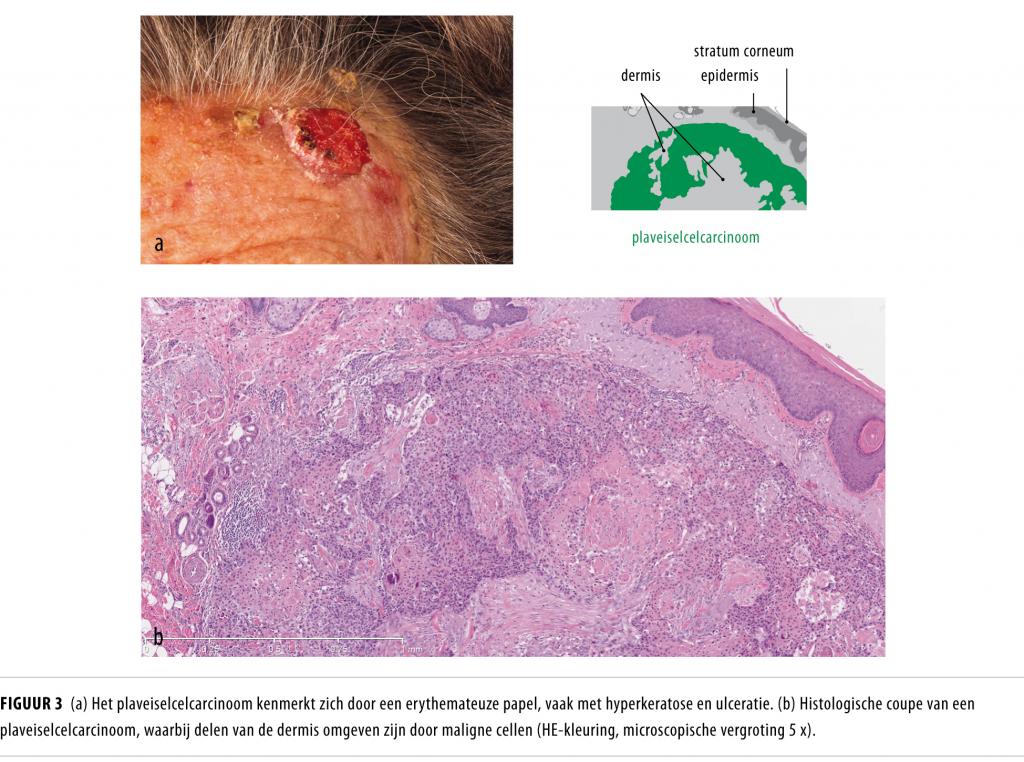
Een PCC presenteert zich als erythemateuze papel die pijnlijk kan zijn en die vaak gepaard gaat met hyperkeratose en ulceratie (figuur 3a). De klinische diagnose kan worden bevestigd met histologisch onderzoek, waarbij atypische, invasief groeiende keratinocyten kenmerkend zijn (figuur 3b). De patholoog-anatoom dient behalve de diagnose ‘PCC’ ook de diepte en de differentiatiegraad – slecht, matig of goed – van de tumor en de aanwezigheid van eventuele perineurale groei of lymfovasculaire invasie te vermelden.
Voor de behandeling en de stadiëring van een PCC is het belangrijk om de risicofactoren voor het ontwikkelen van een lymfklier- of een afstandsmetastase te analyseren. Deze risicofactoren zijn grotendeels besloten in de TNM-classificatie en bestaan uit de grootte, diepte, locatie en de differentiatiegraad van de tumor en of er sprake is van perineurale groei.10 Tumoren die geclassificeerd zijn als stadium 2 of hoger worden beschouwd als tumoren met een hoog risico op metastasering. Hoewel de immuunstatus van de patiënt niet wordt meegewogen in de TNM-classificatie, bestaat er bij patiënten met een verlaagde immuniteit die tevens een recidief van een PCC hebben ook een verhoogd risico op metastasering.10,11
Bij tumoren in stadium 1 is de kans op metastasering naar regionale lymfklieren kleiner dan 5%; bij tumoren in stadium 2 is deze 10-20%.12 Geadviseerd wordt dan ook om bij tumoren in stadium 2 de lymfklieren echografisch te evalueren en zo nodig een aanvullende cytologische punctie te verrichten. Stadium 2-tumoren in het hoofd-halsgebied worden bij voorkeur besproken in een multidisciplinair overleg voor hoofd-halstumoren en naar aanleiding daarvan behandeld.10
Therapie
Conventionele excisie
De belangrijkste behandeling van zowel het BCC en als het PCC is conventionele excisie met vooraf vastgestelde marges. Bij het bepalen van deze marges spelen risicofactoren voor het optreden van een recidief en metastasering een rol.
In een meta-analyse van onderzoeken naar excisiemarges bij BCC’s concluderen de auteurs dat een chirurgische marge van 3 mm een kans van 95% op genezing geeft bij niet-infiltratief groeiende tumoren kleiner dan 2 cm.13 Recidieftumoren en sprieterig groeiende tumoren vereisen grotere marges. In de landelijke richtlijn ‘Behandeling van het basaalcelcarcinoom’ maakt men een afweging tussen curatie en behoud van vitaal weefsel. Er wordt geadviseerd om BCC’s met een laag risico op metastasering te excideren met een marge van 3 mm, en BCC’s met een hoog risico op metastasering en recidieven van BCC’s met een marge van 5 mm.4 BCC’s in het gelaat met een hoog risico op metastasering worden bij voorkeur behandeld met micrografische chirurgie volgens Mohs. Deze procedure leggen wij verderop in de tekst uit.
Er is veel minder onderzoek verricht naar excisiemarges bij het PCC. Een beperkte studie met 111 patiënten toont een radicaliteit van 95% als een marge van 4 mm wordt aangehouden bij tumoren tot 2 cm. Deze 95%-radicaliteit wordt in geval van tumoren in stadium 2 gehaald bij een marge van 6 mm marge.14 In de richtlijn ‘Plaveiselcelcarcinoom van de huid’ is gekozen voor een marge van 5 mm bij tumoren in stadium 1 en voor een marge van 10 mm bij tumoren in stadium 2.10 Daar waar bij een BCC geen minimale vrije histologische marge wordt gehanteerd, wordt bij het PCC met name bij tumoren met een hoog risico op metastasering een minimale vrije histologische marge van 2 mm geadviseerd. Het is dan ook van belang om het histologieverslag adequaat te interpreteren.10 Zowel de vrije histologische marges als de uiteindelijke stadiëring worden hiermee bepaald.
Micrografische chirurgie volgens Mohs
Micrografische chirurgie volgens Mohs is een excisietechniek waarbij peroperatief vriescoupes worden gemaakt. Hierdoor kunnen de resectievlakken volledig in beeld worden gebracht, dit in tegenstelling tot de conventionele histologie waarbij slechts een klein percentage van de resectievlakken kan worden bekeken.15 Indicaties voor micrografische chirurgie volgens Mohs zijn niet scherp omschreven. In Maastricht werd in een prospectieve, gerandomiseerde studie aangetoond dat deze procedure voordelen biedt ten opzichte van conventionele excisie voor de behandeling van een primair infiltratief groeiend BCC groter dan 1 cm in het gelaat en bij een recidief van een BCC in het gelaat.3,5
Er zijn diverse studies die aantonen dat micrografische chirurgie volgens Mohs leidt tot lage recidiefpercentages bij de behandeling van het PCC, maar gerandomiseerd onderzoek hiernaar ontbreekt. In de richtlijn ‘Plaveiselcelcarcinoom van de huid’ wordt daarom geadviseerd om micrografische chirurgie volgens Mohs toe te passen bij patiënten met PCC’s met een hoog risico op metastasering waarbij een ruime excisie zou kunnen resulteren in functionele klachten.
Radiotherapie
In de richtlijn ‘Basaalcelcarcinoom van de huid’ wordt radiotherapie genoemd als een therapeutische mogelijkheid voor alle typen BCC, maar het is niet de voorkeursbehandeling. Verschillende vormen van radiotherapie zijn mogelijk, zoals bestraling met elektronen of met röntgen (orthovolt) en interstitiële radiotherapie. Het effect van de therapie wordt beïnvloed door de ‘4 R’en’, te weten reparatie, redistributie, repopulatie en re-oxygenatie. Het doel is selectieve destructie van tumorcellen waarbij vitaal weefsel gespaard blijft. Bij bestraling is geen uitspraak te doen over histologische radicaliteit. Op de lange termijn zou radiotherapie nieuwe huidtumoren kunnen induceren, waardoor deze behandeling minder gewenst is bij jonge patiënten. In de regel zijn de cosmetisch resultaten goed, maar deze zijn afhankelijk van het gekozen bestralingsschema.16
Voor het PCC wordt in de richtlijn een goede genezingskans beschreven bij een radiotherapeutische behandeling van zowel kleine als grotere tumoren.10 Als chirurgisch ingrijpen op voorhand teveel functionele schade aanricht of het te verwachten resultaten cosmetisch niet acceptabel is, is radiotherapie een goed alternatief.17 Postoperatief wordt radiotherapie aanbevolen in geval van een irradicale resectie waarbij een re-resectie niet mogelijk is, zoals bij een tumorgrootte > 4 cm en bij een tumordikte > 2 cm. Locoregionale radiotherapie is postoperatief geïndiceerd als er tumorpositieve lymfklieren zijn aangetoond. Relatieve behandelindicaties voor postoperatieve radiotherapie zijn perineurale groei of vaso-invasieve groei.
Wij hebben geen recente literatuur kunnen vinden waarin radiotherapie prospectief vergeleken wordt met chirurgie. In 2010 is een onderzoek gepubliceerd waarin patiënten met een BCC of een PCC bestraald werden met een dosis van 54 of 44 Gy. Bij poliklinische controle na 3 jaar had 97,6% van de patiënten met een BCC geen recidief ontwikkeld na bestraling met 54 Gy; bij een dosis van 44 Gy was het recidiefvrije percentage 96,9. Bij patiënten met een PCC waren deze percentages bij stralingsdoses van 54 en 44 Gy respectievelijk 97,0 en 93,6%.16 Eerder is beschreven dat primaire tumoren na behandeling minder vaak recidiveren dan recidieftumoren, respectievelijk 7 versus 20%.18
Fotodynamische therapie
Fotodynamische therapie kan worden ingezet bij intra-epitheliale maligne en premaligne huidafwijkingen. Het effect van de deze behandelvorm berust op het activeren van een lichtgevoelige stof (chromofoor) in aanwezigheid van zuurstof onder invloed van licht met een geschikte frequentie. Dit licht wordt geabsorbeerd door de chromofoor (‘fotosensitiser’), waardoor een chemische reactie ontstaat met onder andere vorming van reactieve zuurstofradicalen. De zuurstofradicalen zijn verantwoordelijk voor het therapeutische effect, omdat deze bij een maligne of premaligne huidafwijking celdood induceren door apoptose of necrose. In Nederland worden voornamelijk 5-aminolevulinezuur (5-ALA) en 5-methylaminolevulinezuur (MAL) als chromofoor gebruikt. Meer gedetailleerde informatie over fotodynamische therapie kunt u nalezen in een artikel in het NTvG uit 2005.19
De behandeling vindt poliklinisch plaats en deze is relatief eenvoudig uit te voeren. Een nadeel van fotodynamische therapie is pijn, die zich met name voordoet wanneer grotere huidgebieden behandeld moeten worden. Hoewel de kortetermijneffecten van fotodynamische therapie voor superficiële BCC’s en de ziekte van Bowen veelbelovend zijn, is er weinig literatuur verschenen over de langetermijneffecten.20 Op verschillende manieren is onderzocht hoe de effectiviteit verbeterd kan worden. In Rotterdam is uitgebreid gekeken naar het effect van diverse belichtingsschema’s. De onderzoekers concludeerden dat een gefractioneerd schema bij patiënten met een superficieel BCC leidt tot een complete respons van circa 90% na 5 jaar.21
Imiquimod
Imiquimod-crème is een lokaal immuunmodulerende behandeling. Door het vrijkomen van cytokines wordt een lokale afweerreactie in gang gezet die een antiviraal en antitumoraal effect heeft. Deze lokale afweerreactie gaat gepaard met erytheem, oedeem en erosies. Ook ervaart een klein percentage van patiënten griepachtige verschijnselen als gevolg van een systemische afweerreactie. Het voordeel van deze behandeling is dat het een niet-invasieve behandeling betreft en dat deze thuis kan plaatsvinden. Imiquimod-crème is niet geschikt voor de behandeling van het PCC, maar geeft wel goede resultaten bij de behandeling van het superficieel BCC.20 De gebruikelijke dosering bij behandeling van het superficieel BCC is 1 dd aanbrengen van de crème, 5 dagen per week gedurende 6 weken. In een recente trial werden fotodynamische therapie, imiquimod-crème en 5-fluorouracil(5-FU)-crème onderling met elkaar vergeleken voor de behandeling van het superficieel BCC (Arits, schriftelijke mededeling, 2012). Fotodynamische therapie bleek minder effectief dan imiquimod-crème en aanmerkelijk duurder dan imiquimod- en 5FU-crème. De vergelijking was niet conclusief wat betreft de effectiviteit van imiquimod- versus 5FU-crème.
5-Fluorouracil
5-Fluorouracil (5FU) is een bekend chemotherapeuticum dat binnen de dermatologie in een crème wordt gebruikt. De behandeling met 5FU-crème gaat gepaard met erytheem en erosies, wat tegelijkertijd ook de effectiviteit van het middel bepaalt. Het is niet geschikt voor de behandeling van patiënten met een PCC, maar wel voor de behandeling van superficiële BCC’s (Arits, schriftelijke mededeling, 2012). Daarbij is het meest gebruikte behandelschema 2 dd aanbrengen gedurende 4 weken. Voordelen van 5FU-crème zijn de lage kosten van het middel en dat de behandeling thuis plaats kan vinden.
Hedgehog-pathway-remmer
Een nieuwe behandelmethode voor patiënten met een BCC is de hedgehog-pathway-remmer vismodegib. Het betreft een systemische behandeling voor uitgebreide en gemetastaseerde BCC’s.22 Dit medicijn geeft bij 21% van de patiënten met uitgebreide BCC’s een volledige genezing en bij 43% een gedeeltelijke genezing. Helaas gaat het bij ongeveer de helft van de patiënten gepaard met bijwerkingen zoals spierspasmen, haarverlies en smaakverandering. Daarmee is dus niet elke patiënt met een uitgebreid BCC gebaat bij deze therapie.
Follow-up
De richtlijnen voor de behandeling van het BCC en van het PCC geven elk duidelijke adviezen voor follow-up. Het is belangrijk te realiseren dat een derde van de patiënten een secundaire huidkanker ontwikkelt.23 Dit betekent dat een zorgvuldige overweging gemaakt moet worden bij wie follow-up beëindigd kan worden. Goede voorlichting van de dermatoloog aan de huisarts en aan de patiënt is daarom essentieel. Vanwege het risico op een 2e huidkanker moet de gehele huid van elke patiënt die zich presenteert met huidkanker bij controle geïnspecteerd worden.
Conclusie
Het palet van mogelijkheden voor de behandeling van patiënten met een basaalcelcarcinoom of een plaveiselcelcarcinoom van de huid is sinds de vorige eeuw aanzienlijk uitgebreid. De hedendaagse dermatoloog moet adequaat inspelen op de epidemie van huidkanker. Daarbij heeft deze een uitgebreide keus aan therapeutische opties, van smeren tot snijden.
Leerpunten
Huidkanker is door de toenemende incidentie een probleem dat voor de diverse behandelaars steeds groter wordt.
Behandeling van patiënten met non-melanoma huidkanker is niet langer slechts een kwestie van chirurgisch ingrijpen.
Behandelaars van patiënten met non-melanoma huidkanker moeten op de hoogte zijn van de voor- en nadelen van de vele behandelopties.
Literatuur
Youssef KK, Van Keymeulen A, Lapouge G, et al. Identification of the cell lineage at the origin of basal cell carcinoma. Nat Cell Biol. 2010;12:299-305 Medline.
Zhang H, Ping XL, Lee PK, et al. Role of PTCH and p53 genes in early-onset basal cell carcinoma. Am J Pathol. 2001;158:381-5 Medline. doi:10.1016/S0002-9440(10)63980-6
Smeets NW, Krekels G, Ostertag J, et al. Surgical excision versus Mohs’ micrographic surgery for basal cell carcinoma of the face; a prospective randomized trial. Lancet. 2004;364:1766-72 Medline. doi:10.1016/S0140-6736(04)17399-6
Nederlandse Vereniging voor Dermatologie en Venereologie. Evidence-based richtlijn ‘Behandeling van het basaalcelcarcinoom’. Utrecht: NVDV/Kwaliteitsinstituut voor de Gezondheidszorg CBO; 2007.
Mosterd K, Krekels GA, Nieman FH, et al. Surgical excision versus Mohs’ micrographic surgery for primary and recurrent basal-cell carcinoma of the face: a prospective randomised controlled trial with 5-years’ follow-up. Lancet Oncol. 2008;9:1149-56. Medline. doi:10.1016/S1470-2045(08)70260-2
Scherer D, Kumar R. Genetics of pigmentation in skin cancer--a review. Mutat Res. 2010;705:141-53 Medline. doi:10.1016/j.mrrev.2010.06.002
De Gruijl FR, Rebel H. Early events in UV carcinogenesis--DNA damage, target cells and mutant p53 foci. Photochem Photobiol. 2008;84:382-7. Medline doi:10.1111/j.1751-1097.2007.00275.x
Kuschal C, Thoms KM, Schubert S, et al. Skin cancer in organ transplant recipients: effects of immunosuppressive medications on DNA repair. Exp Dermatol. 2012;21:2-6 Medline. doi:10.1111/j.1600-0625.2011.01413.x
Iannacone MR, Gheit T, Waterboer T, et al. Case-Control study of cutaneous human papillomaviruses in squamous cell carcinoma of the skin. Cancer Epidemiol Biomarkers Prev. 2012;21:1303-13 Medline. doi:10.1158/1055-9965.EPI-12-0032
Nederlandse Vereniging voor Dermatologie en Venereologie. Richtlijn ‘Plaveiselcelcarcinoom van de huid’. Utrecht: NVDV; 2010.
Brantsch KD, Meisner C, Schönfisch B, et al. Analysis of risk factors determining prognosis of cutaneous squamous-cell carcinoma: a prospective study. Lancet Oncol. 2008;9:713-20 Medline. doi:10.1016/S1470-2045(08)70178-5
Veness MJ, Palme CE, Morgan GJ. High-risk cutaneous squamous cell carcinoma of the head and neck: results from 266 treated patients with metastatic lymph node disease. Cancer. 2006;106:2389-96 Medline. doi:10.1002/cncr.21898
Gulleth Y, Goldberg N, Silverman RP, Gastman BR. What is the best surgical margin for a Basal cell carcinoma: a meta-analysis of the literature. Plast Reconstr Surg. 2010;126:1222-31 Medline. doi:10.1097/PRS.0b013e3181ea450d
Brodland DG, Zitelli JA. Surgical margins for excision of primary cutaneous squamous cell carcinoma. J Am Acad Dermatol. 1992;27:241-8 Medline. doi:10.1016/0190-9622(92)70178-I
Van Baardwijk AA, Verhaegh ME, Krekels GA, Vermeulen AH, Neumann HA. Micrografische chirurgie volgens Mohs als behandeling van recidief basalecelcarcinoom. Ned Tijdschr Geneeskd. 1997;141:524-9 Medline.
Van Hezewijk M, Creutzberg CL, Putter H, et al. Efficacy of a hypofractionated schedule in electron beam radiotherapy for epithelial skin cancer: Analysis of 434 cases. Radiother Oncol. 2010;95:245-9 Medline. doi:10.1016/j.radonc.2010.02.024
Schulte KW, Lippold A, Auras C, et al. Soft x-ray therapy for cutaneous basal cell and squamous cell carcinomas. J Am Acad Dermatol. 2005;53:993-1001 Medline. doi:10.1016/j.jaad.2005.07.045
Locke J, Karimpour S, Young G. Radiotherapy for epithelial skin cancer. Int J Radiat Oncol Biol Phys. 2001;51:748-55 Medline. doi:10.1016/S0360-3016(01)01656-X
Thissen MR, Kuijpers DI, Neumann HA. Ruimere toepassing van fotodynamische therapie in de dermatologie. Ned Tijdschr Geneeskd. 2005;149:232-7 Medline.
Roozeboom MH, Arits AH, Nelemans PJ, Kelleners-Smeets NW. Overall treatment success after treatment of primary superficial basal cell carcinoma: a systematic review and meta-analysis of randomized and non-randomized trials. Br J Dermatol. 2012;167:733-56 Medline. doi:10.1111/j.1365-2133.2012.11061.x
De Vijlder HC, Sterenborg HJCM, Neumann HAM, Robinson DJ, de Haas ERM. Light fractionation significantly improves the response of superficial basal cell carcinoma to aminolaevulinic acid photodynamic therapy: five-year follow-up of a randomized, prospective trial. Acta Derm Venereol. 2012;92:641-7 Medline.
Sekulic A, Migden MR, Oro AE, et al. Efficacy and safety of vismodegib in advanced basal-cell carcinoma. N Engl J Med. 2012;366:2171-9 Medline. doi:10.1056/NEJMoa1113713
Flohil SC, Koljenović S, de Haas ER, Overbeek LI, de Vries E, Nijsten T. Het blijft vaak niet bij één basaalcelcarcinoom. Ned Tijdschr Geneeskd. 2011;155:A4110 Medline.





Reacties