Dames en Heren,
Een deel van de patiënten die vanwege covid-19 langdurig zijn opgenomen op de afdeling Intensive Care ontwikkelt pijn en bewegingsbeperkingen van de gewrichten. In dit artikel illustreren we aan de hand van de ziektegeschiedenis van 2 patiënten het belang van tijdige herkenning en diagnostiek van de aandoening die hieraan ten grondslag ligt.
Kernpunten
- Heterotope ossificatie treedt op bij naar schatting 10-25% van de patiënten met een covid-19-pneumonie die langdurig beademd worden op de Intensive Care.
- Deze ossificaties worden vooral gezien rond grote gewrichten, zoals heupen en schouders.
- Aan de hand van röntgenfoto’s kan de diagnose worden gesteld; een verhoogde concentratie van het alkalisch fosfatase in het bloed kan de diagnose ondersteunen.
- In de acute fase kan men behandeling met indometacine overwegen om botvorming te remmen.
- Fysiotherapeutische behandeling bestaat uit het inzetten van vroege, regelmatige en voorzichtige mobilisatie van de gewrichten.
- Onderzoek moet uitwijzen of profylactische behandeling met indometacine zinvol is.
artikel
De afgelopen maanden zagen wij tientallen patiënten die langdurig op de afdeling Intensive Care (IC) opgenomen waren vanwege een covid-19-pneumonie. Een deel van deze patiënten had veel pijn en bewegingsbeperkingen van de gewrichten, met name van de schouders en heupen. De juiste diagnose had bij deze patiënten mogelijk eerder gesteld kunnen worden wanneer men alerter was geweest op het vóórkomen van de onderliggende aandoening bij deze patiëntengroep. In deze klinische les beschrijven we 2 patiënten met heterotope ossificaties rondom de grote gewrichten nadat zij een covid-19-pneumonie hadden doorgemaakt.
Patiënt A, een 59-jarige man met in de voorgeschiedenis astma, hypertensie, jicht, prostaatcarcinoom en een recente operatie van de rechter schouder, werd opgenomen vanwege een covid-19-pneumonie. Hij werd 4 dagen later vanwege respiratoire insufficiëntie geïntubeerd en overgeplaatst naar de IC-afdeling. Bijna een maand later was hij voldoende hersteld om gedetubeerd te worden. De revalidatiearts werd in consult gevraagd om te beoordelen of patiënt een indicatie had voor medisch specialistische revalidatie.
Bij lichamelijk onderzoek zagen wij een man die, naast ernstige zwakte aan de armen en benen, last had van pijn en passieve bewegingsbeperkingen van met name de schouders, ellebogen en heupen. Aanvankelijk duidden wij deze klachten als algehele verstijving van de gewichtskapsels en verkorting van de spieren door de langdurige immobilisatie in combinatie met de pre-existente schouderklachten. De fysiotherapeut probeerde de bewegingsuitslag van de gewrichten zo goed mogelijk te behouden door passieve gewrichtsmobilisaties, maar uitvoering hiervan werd gehinderd door de hevige pijn.
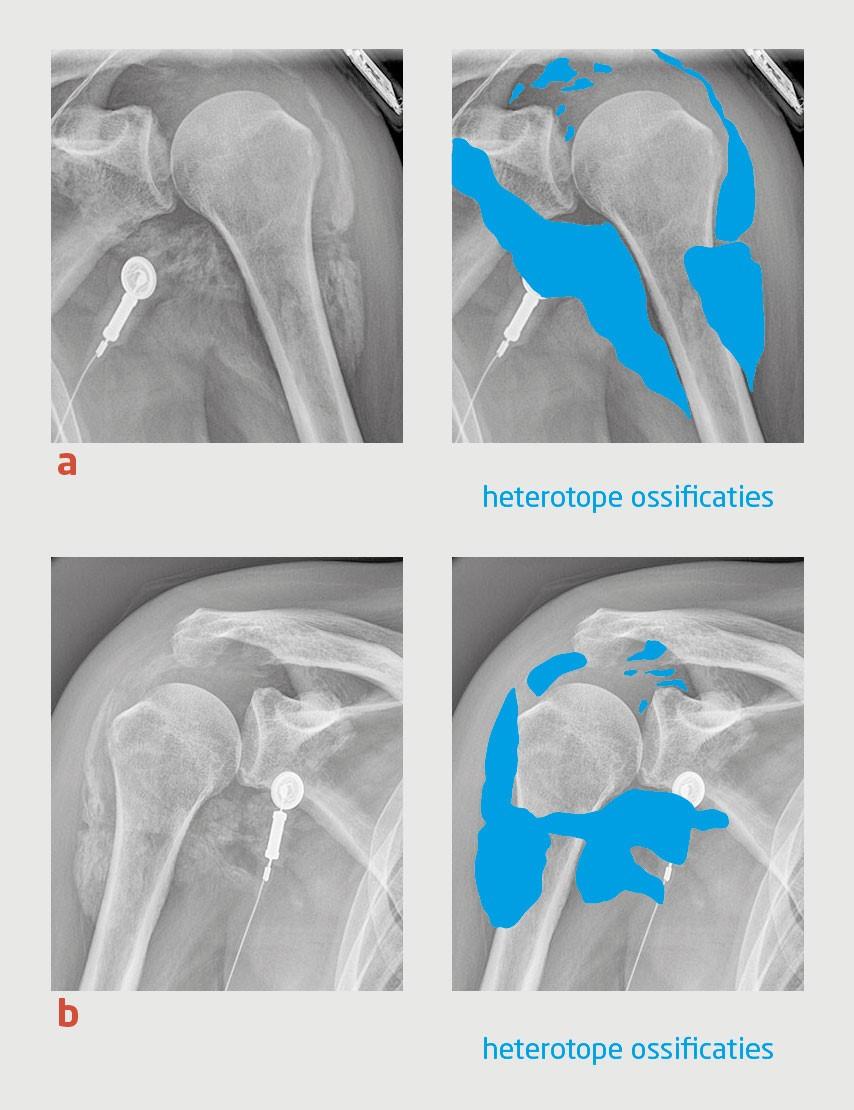
Omdat de pijn bij patiënt aanhield werden 2 weken later röntgenfoto’s van beide schouders gemaakt. Deze röntgenfoto’s lieten uitgebreide ossificaties in de weke delen rondom beide glenohumerale gewrichten zien; zogenoemde heterotope ossificaties (figuur 1). Terugkijkend in zijn laboratoriumuitslagen bleek patiënt al langer een opzichzelfstaande verhoging van de concentratie alkalisch fosfatase in het bloed te hebben.
Bij de telefonische controle 3 maanden na opname verbleef patiënt in een revalidatiecentrum. Hij had nog steeds forse pijn en bewegingsbeperkingen in de gewrichten, vooral in de rechter schouder, hetgeen hem ernstig beperkte in het gebruik van de rechter arm. Inmiddels is patiënt verwezen naar de orthopedisch chirurg om te beoordelen of chirurgische verwijdering van de heterotope ossificaties mogelijk en zinvol is.
Patiënt B, een 53-jarige man met blanco voorgeschiedenis, werd opgenomen met klachten van koorts en dyspneu op basis van een covid-19-pneumonie, die 1,5 week eerder was ontstaan. Vanwege respiratoire insufficiëntie werd de man 2 dagen na opname geïntubeerd en overgeplaatst naar de IC-afdeling. Tijdens de IC-opname traden verschillende complicaties op, waaronder een recidiverende pneumothorax, empyeem en een diepe veneuze trombose. Na 10 weken werd patiënt naar de afdeling Medium Care overgeplaatst en werd de tracheacanule verwijderd. De revalidatiearts werd in consult gevraagd.

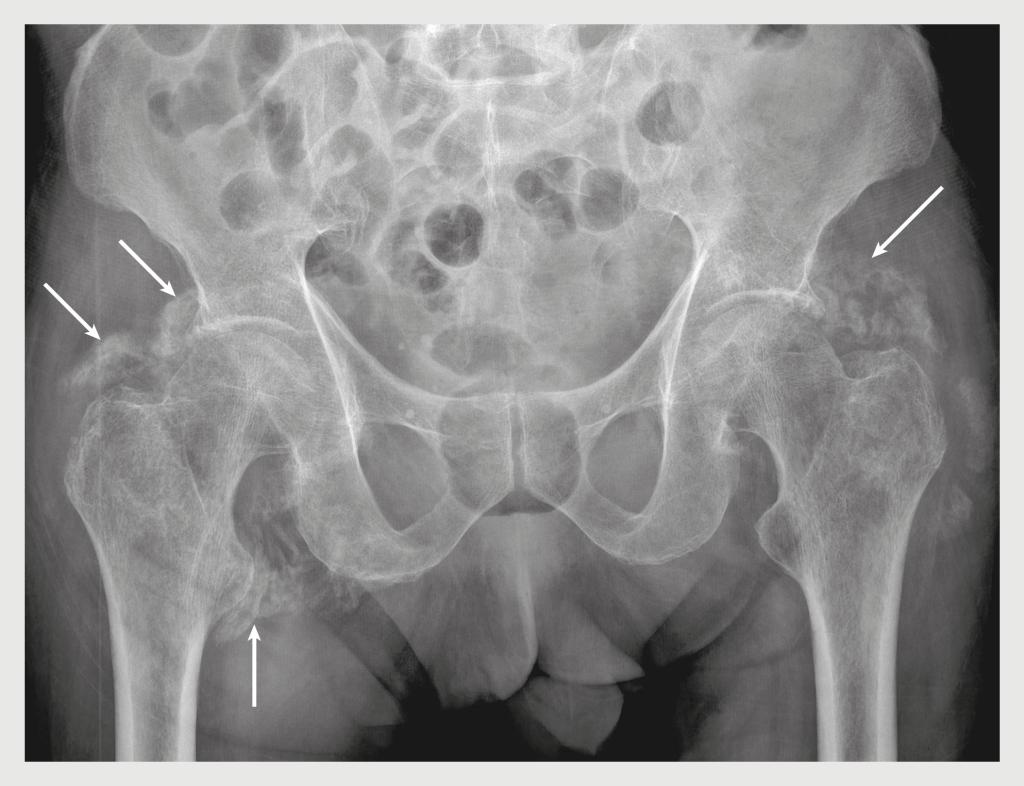
Bij lichamelijk onderzoek zagen wij zeer ernstige zwakte en atrofie aan beide armen en benen. Daarnaast had patiënt pijn en bewegingsbeperkingen in de beide heupen en schouders. Hierop maakten wij röntgenfoto’s van beide schouders en het bekken vanwege het vermoeden op heterotope ossificaties. Deze röntgenfoto’s lieten uitgebreide heterotope ossificaties rondom beide glenohumerale en coxofemorale gewrichten zien (figuur 2 en 3). De concentratie alkalisch fosfatase in het bloed was tijdens de opname gestegen van 94 naar 397 U/l (referentiewaarde < 115U/l). Omdat de ossificaties al uitgebreid gevormd waren en vanwege mogelijke interacties met de reeds voorgeschreven medicatie, behandelden wij patiënt niet met indometacine. De fysiotherapeut behandelde patiënt met passieve gewrichtsmobilisaties, binnen de pijngrens en met weinig weerstand.
15 weken na opname verbleef de patiënt nog steeds in het ziekenhuis. Zowel zijn actieve als passieve schoudermobiliteit waren nog ernstig beperkt, hetgeen hem ernstig belemmerde bij het opbouwen van zijn zelfstandigheid.
Beschouwing
Incidentie
Heterotope ossificatie is de vorming van bot in de weke delen. Deze botvorming treedt vaak op rond de grote gewrichten en kan daarom leiden tot ernstige bewegingsbeperkingen. Heterotope ossificatie is uitgebreid beschreven bij patiënten met een traumatische dwarslaesie of traumatisch hersenletsel en wordt dan meestal neurogene heterotope ossificatie genoemd. Daarnaast komt heterotope ossificatie vaak voor na operaties, met name heupoperaties. Meestal zijn de afwijkingen minder uitgebreid dan bij onze patiënten.
Voor zover wij weten is heterotope ossificatie niet eerder beschreven bij patiënten met een covid-19-pneumonie. Het is wel duidelijk dat heterotope ossificatie vaker voorkomt bij patiënten die langdurig kunstmatig zijn beademd. In een Amerikaanse studie werden 109 patiënten die op de IC opgenomen waren met het ‘acute respiratory distress syndrome’ (ARDS) gevolgd. Bij 5% van deze patiënten trad heterotope ossificatie op.1 Wij hebben niet alle covid-19-patiënten die langdurig op de IC zijn beademd systematisch gescreend op de aanwezigheid van heterotope ossificaties. Op basis van onze ervaring schatten we dat 10-25% van de patiënten met een covid-19-pneumonie die langdurig zijn beademd heterotope ossificatie ontwikkelt, een hoger percentage dan eerder bij patiënten met ARDS werd gerapporteerd. Toekomstig onderzoek moet uitwijzen of ons vermoeden klopt.
Klinisch beeld
Heterotope ossificatie kan zich op verschillende manieren uiten. Vaak hebben patiënten pijn rond het aangedane gewricht die wordt uitgelokt door zowel passief als actief bewegen van het gewricht. Onze patiënten ervoeren aanvankelijk geen pijn door langdurige sedatie, waardoor de juiste diagnose waarschijnlijk later werd gesteld.
Bij lichamelijk onderzoek kan bij patiënten met heterotope ossificatie roodheid, warmte of zwelling van het aangedane gewricht worden gezien. Daarnaast hebben patiënten meestal een bewegingsbeperking van het aangedane gewricht, variërend van een geringe bewegingsbeperking tot volledige ankylose (gewrichtsverstijving). In ernstige gevallen kan neurologische schade optreden door zenuwbeklemming. Bij patiënt A werden de passieve bewegingsbeperkingen aanvankelijk toegeschreven aan verstijving van het gewrichtskapsel en verkorting van de spieren tijdens de IC-opname. Achteraf gezien was de hevige pijn bij actief en passief bewegen van de gewrichten een belangrijke aanwijzing dat er meer aan de hand was.
Zowel bij patiënt A als patiënt B zagen wij geen roodheid, zwelling en warmte van de aangedane gewrichten. Deze ontstekingsverschijnselen zijn duidelijker te zien bij oppervlakkigere gewrichten, zoals de ellebogen en knieën, dan bij dieper gelegen gewrichten, zoals de schouders en heupen.
Pathofysiologisch mechanisme
Het onderliggende pathofysiologische mechanisme van heterotope ossificatie is grotendeels onbekend.2,3 Waarschijnlijk spelen zowel systemische als lokale factoren een rol, zoals langdurige immobilisatie, systemische alkalose bij mechanische beademing en algehele metabole ontregeling. Het proces van ossificatie begint als een inflammatoire reactie, waarna mesenchymale stamcellen vervolgens differentiëren tot osteoblasten. Deze osteoblasten zorgen voor vorming van osteoïd en de afzetting van botmatrix in de weke delen. Door mineralisatie van het osteoïd wordt bot gevormd, wat uiteindelijk op röntgenfoto’s te zien is. De afzetting van bot vindt vooral plaats in het bindweefsel.
Diagnostiek
Diagnostiek is aangewezen wanneer men op basis van het klinische beeld heterotope ossificatie vermoedt. Het vroegtijdig stellen van de diagnose is van belang voor duiding van de klachten en om de patiënt tijdig medicamenteus of niet-medicamenteus te kunnen behandelen. De concentratie alkalisch fosfatase in het bloed is doorgaans verhoogd bij patiënten met heterotope ossificatie. Verhoging van de concentratie alkalisch fosfatase kan meerdere oorzaken hebben, waaronder de leverfunctiestoornissen die bij patiënten met covid-19 kunnen voorkomen.4 Een verhoogde concentratie alkalisch fosfatase kan dus wijzen op de diagnose, maar de diagnose kan niet op basis van deze waarde alleen worden gesteld.
De diagnose wordt gesteld aan de hand van kenmerkende afwijkingen op een röntgenfoto. Röntgenfoto’s geven ook een beeld van de uitgebreidheid van de heterotope ossificatie, maar zijn in een vroege fase – wanneer de botmatrix wordt gevormd – vaak nog niet afwijkend. Met een 3-fasenskeletscintigram met technetium-99m kunnen heterotope ossificaties wel al in een vroeg stadium worden opgespoord. Dit onderzoek is echter kostbaar en is bovendien niet in alle ziekenhuizen beschikbaar. Een goedkoper alternatief voor diagnostiek in de vroege fase is echografie.
Preventie en behandeling
Behandeling met NSAID’s is effectief om heterotope ossificatie te voorkómen na bijvoorbeeld een dwarslaesie of heupoperatie.5 Vooral van indometacine in een dosering van 25 mg 3 dd gedurende 3 weken is de preventieve werking op heterotope ossificatie onderzocht.2,5
Toekomstige onderzoeken zijn nodig om te bepalen of het zinvol is om patiënten met covid-19 op de IC preventief met indometacine te behandelen, met als doel om heterotope ossificaties te voorkomen. Aangezien deze patiënten vaak met antistolling worden behandeld ter preventie van trombo-embolieën, leidt de toevoeging van een NSAID tot een verhoogd bloedingsrisico.2 Andere nadelen van NSAID’s zijn onder andere het risico op peptische ulcera of verminderde nierfunctie.
Het is niet duidelijke of NSAID’s ook zinvol zijn als de aanwezigheid van heterotope ossificatie al is vastgesteld. In de praktijk worden patiënten met heterotope ossificatie vaak wel met NSAID’s behandeld, zeker als de diagnose in een relatief vroege fase is gesteld.6 Toekomstig onderzoek moet uitwijzen of deze behandeling gerechtvaardigd is.
Er zijn studies die laten zien dat naast NSAID’s ook bisfosfonaten de progressie van heterotope ossificatie vertragen als met behandeling wordt begonnen voordat afwijkingen op de röntgenfoto zichtbaar worden.5 Als röntgenfoto’s eenmaal afwijkingen laten zien, zijn bisfosfonaten minder effectief.7 Bovendien bestaat het risico op een ‘rebound’-fenomeen waarbij alsnog heterotope ossificaties ontstaan nadat de behandeling met bisfosfonaten is gestopt.3
Kortdurende bestraling met een lage dosis kan heterotope ossificaties na een heupoperatie voorkomen. Er zijn ook aanwijzingen dat kortdurende bestraling bij dwarslaesiepatiënten met heterotope ossificaties progressie van botvorming voorkomt.8 Het belangrijkste nadeel van deze kortdurende bestraling is het potentieel carcinogene effect.
Vroege, regelmatige en voorzichtige mobilisatie van IC-patiënten kan helpen om de gewrichtskapsels zo soepel mogelijk te houden en om verkorting van spieren en contracturen te voorkomen.2 Mogelijk wordt de ontwikkeling van heterotope ossificatie versterkt door microtraumata die ontstaan wanneer door de pijngrens heen of tegen weerstand in wordt bewogen.9
De mobiliteit van het gewricht kan door heterotope ossificatie zodanig beperkt of pijnlijk zijn dat er belemmeringen ontstaan bij het uitvoeren van dagelijkse activiteiten als lopen, zitten of het gebruik van de armen. Dit was ook het geval bij onze patiënten. Wanneer patiënten zo sterk beperkt zijn in het dagelijks functioneren, kan chirurgische verwijdering van de ossificaties worden overwogen.10 Het doel van de operatie is om de ossificaties volledig te verwijderen, om het risico op een recidief zo laag mogelijk te maken. Over het algemeen wordt aangenomen dat het bot voldoende uitgerijpt moet zijn voordat tot een operatie kan worden overgegaan. Totdat de ossificaties zijn uitgerijpt kan de pijn namelijk nog afnemen, waardoor de indicatie voor operatie mogelijk komt te vervallen. Volledige uitrijping van het bot duurt meestal 6-12 maanden.
Dames en heren, denk bij een patiënt die langdurig op de afdeling Intensive Care is opgenomen vanwege een covid-19-pneumonie en die pijn en bewegingsbeperkingen heeft van de grote gewrichten, aan de diagnose ‘heterotope ossificatie’. Beeldvormend onderzoek is nodig om de diagnose te kunnen stellen en een verhoogde concentratie alkalisch fosfatase in het bloed kan de diagnose ondersteunen. Het tijdig stellen van de diagnose is niet alleen van groot belang om het klinische beeld te begrijpen, maar ook om zo vroeg mogelijk het ossificatieproces te kunnen remmen en zo de functionele gevolgen voor de patiënt te verkleinen.
Literatuur
Herridge MS, Cheung AM, Tansey CM, et al; Canadian Critical Care Trials Group. One-year outcomes in survivors of the acute respiratory distress syndrome. N Engl J Med. 2003;348:683-93. doi:10.1056/NEJMoa022450. Medline
Van Kuijk AA, Geurts ACH, van Kuppevelt HJM. Neurogenic heterotopic ossification in spinal cord injury. Spinal Cord. 2002;40:313-26. doi:10.1038/sj.sc.3101309. Medline
Claes S, Populaire J. Heterotope ossificatie. Tijdschr Geneeskd. 2006;62:1206-14.
Kumar-M P, Mishra S, Jha DK, et al. Coronavirus disease (COVID-19) and the liver: a comprehensive systematic review and meta-analysis. Hepatol Int. 2020;4:1-12. doi:10.1007/s12072-020-10071-9. Medline
Teasell RW, Mehta S, Aubut JL, et al; SCIRE Research Team. A systematic review of the therapeutic interventions for heterotopic ossification after spinal cord injury. Spinal Cord. 2010;48:512-21. doi:10.1038/sc.2009.175. Medline
Ziekenhuisprotocol Dwarslaesie. Amstelveen: Nederlands Vereniging voor Donorgeneeskunde; 2010.
Banovac K, Gonzalez F, Renfree KJ. Treatment of heterotopic ossification after spinal cord injury. J Spinal Cord Med. 1997;20:60-5. doi:10.1080/10790268.1997.11719457. Medline
Müseler AC, Grasmücke D, Jansen O, et al. In-hospital outcomes following single-dose radiation therapy in the treatment of heterotopic ossification of the hip following spinal cord injury-an analysis of 444 cases. Spinal Cord. 2017;55:244-6. doi:10.1038/sc.2016.112. Medline
Silver J. Comment on ‘Neurogenic heterotopic ossification in spinal cord injury’. Spinal Cord. 2003;41:421-2. doi:10.1038/sj.sc.3101445. Medline
Van Ooij A, van Kollenburg JAPAC, Pons C, Walenkamp GH. Chirurgisch verwijderen van invaliderende neurogene heterotope ossificaties van de heup. Ned Tijdschr Geneeskd. 2005;149:37-41 Medline.





Vitamine D en heterotope calcificaties.
Een te laag vitamine D, een serum 25 OHD-spiegel < 50 nmol/l, werd bij 11 van de 12 patiënten met heterotope calcificaties gevonden (1). Maar bij COVID-19 patiënten zonder deze calcificaties, is het ook verstandig de serum 25 OHD-spiegel te bepalen en te behandelen als die spiegel lager is dan 50 nmol/l (2). Eveneens lijkt het wenselijk de parenterale voeding op de IC aan te passen want die bevat op dit moment niet de geadviseerde 10 mcg, maar slechts 5,5 mcg colecalciferol (3).
Samenvattend, meet bij iedere COVID-19 patiënt de serum 25 OHD spiegel en handel naar bevinden, veel leed zal worden bespaard.
Referenties
1. Oleson C, Seidel Benjamin J , Zhan T. Association of vitamin D deficiency, secondary hyperparathyroidism, and heterotopic ossification in spinal cord injury. J Rehabil Res Dev 2013;50(9):1177-86.
2. Castillo ME, Entrenas Costa LM, Vaquero Barrios JM, Alcalá Di´az JF, Miranda JL, Bouillon R, Quesada Gomez JM Effect of Calcifediol treatment and best available therapy versus best available therapy on Intensive Care Unit admission and mortality among patients hospitalized for COVID-19: A pilot randomized clinical study. J. Steroid Biochem 2020 in press.
3. https://icv-erasmusmc.nl/protocol/voeding-2/
J. van der Meulen, basis-arts, mede namens:
Hosein Aziz; huisarts in opleiding, Annemarie Schop; huisarts in opleiding, Jasper Hartman; huisarts en opleider van de huisartsenpraktijk de Jagerweg Dordrecht.