Ziekenhuisinfecties met methicilline-resistente Staphylococcus aureus (MRSA) brengen hoge mortaliteit en kosten met zich mee.1,2 Om deze redenen is het belangrijk MRSA-infecties zoveel mogelijk te voorkomen. In 2008 werd 0,7% van alle S. aureus-bacteriëmieën in Nederlandse ziekenhuizen veroorzaakt door MRSA (bron: RIVM. European Antimicrobial Resistance Surveillance System: http://www.rivm.nl/earss/database). De belangrijkste oorzaak voor deze lage prevalentie is het MRSA-beleid (ook wel ‘search and destroy’ genoemd), dat in de Nederlandse ziekenhuizen in de huidige vorm sinds 1988 wordt toegepast (tabel 1).3 Bij dit beleid worden MRSA-dragers actief opgespoord en behandeld en patiënten bij wie men MRSA-dragerschap vermoedt, in isolatie verpleegd totdat MRSA is uitgesloten. De maatregelen zijn destijds gebaseerd op twee epidemiologische kenmerken: MRSA-dragerschap bij gezonde mensen is verwaarloosbaar en de belangrijkste risicofactor voor MRSA-dragerschap is opname in een buitenlands ziekenhuis.
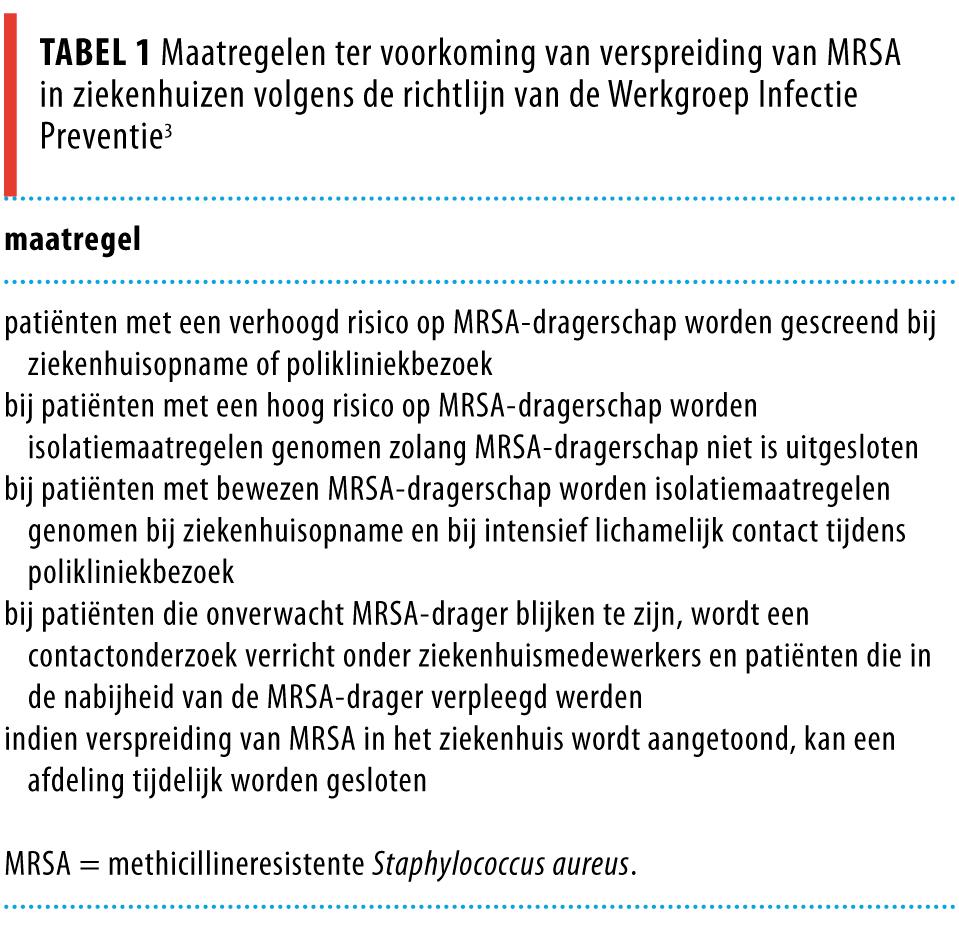
Hoewel dit beleid effectief is, vraagt het veel inspanning van medewerkers in de gezondheidszorg en gaat het…





Bewijsvoering MSRA-beleid
Een boeiend ter discussie stuk, maar deze passage vond ik tegenstrijdig:
''Waarschijnlijk zijn niet alle maatregelen ter voorkoming van verspreiding van MRSA noodzakelijk om de lage MRSA-prevalentie te waarborgen, maar dit is niet getoetst in klinisch onderzoek. Recent zijn echter zowel de epidemiologie van MRSA als de diagnostische mogelijkheden om dragerschap aan te tonen belangrijk veranderd en het is dan ook tijd voor een kritische beschouwing van het beleid''.
Het argument dat iets niet getoetst is in klinisch onderzoek wordt hier als argument tegen de gangbare strategie en als argument voor het nieuwe in te voeren beleid aangevoerd.
Aangezien het huidige MRSA beleid succesvol lijkt [1], moet een nieuwe strategie eerst goed worden onderbouwd met klinisch onderzoek. De afwezigheid van bewijs is geen bewijs dat iets niet werkt, de afwezigheid van goed bewijs is mi wel reden om een nieuwe behandeling niet in te voeren.
Gijs Landman
1. Ned Tijdschr Geneeskd. 2010;154:C753
Het Nederlandse MRSA beleid
Wij danken collega Landman voor zijn reactie. Wij zijn het volledig met hem eens dat ‘het argument dat iets niet getoetst is in klinisch onderzoek’ niet als argument tegen een gangbare strategie (en voor een nieuw beleid) kan worden aangevoerd. Dat is ook geenszins onze intentie. De argumenten om het huidige beleid te herzien zijn de veranderde epidemiologie, het beschikbaar zijn van sneldiagnostiek en voortschrijdend inzicht op gebied van transmissie van MRSA. Overigens gaat het hier niet om de invoering van een nieuwe behandeling, maar een zeer beperkte aanpassing in een uitgebreid pakket van infectiepreventie maatregelen ter voorkoming van MRSA transmissie in Nederlandse ziekenhuizen. Het Nederlandse MRSA-beleid bestaat uit meerdere componenten die in gezamenlijkheid en zonder wetenschappelijke onderbouwing in 1988 zijn geïmplementeerd.Inmiddels weten we (uit modelleringonderzoek)1 dat niet alle maatregelen nodig zijn om de lage MRSA prevalentie te waarborgen, maar dat is niet getoetst in klinisch onderzoek. Behoudens de logistieke hindernissen om een dergelijke klinische studie uit te voeren, zou het ook jaren duren om het relatieve aandeel van elk van de onderdelen vast te stellen en te onderzoeken of het achterwege laten van één component gevolgen heeft. Sommige zaken kun je nou eenmaal niet met klinisch onderzoek vaststellen. Vasthouden aan het oude beleid zou betekenen dat we daar jaren aan vastzitten, ook al zijn er sterke redenen om daarvan af te wijken. Aangezien het aantal te isoleren patiënten alleen maar zal toenemen door opkomst van andere multiresistente micro-organismen, stellen wij voor het beleid aan te passen aan de nieuwe diagnostische mogelijkheden en epidemiologische inzichten.
Marjan Wassenberg en Marc Bonten
1. Bootsma MC et al. Proc Natl Acad Sci USA 2006;103:5620-5625.
Het Nederlandse MRSA-beleid kan en moet anders
Het Nederlandse MRSA beleid schrijft strenge isolatie voor van mogelijke MRSA dragers: de patiënt verblijft op een eenpersoonskamer en eenieder die de kamer betreedt draagt schort, muts, masker en handschoenen. Wassenberg en Bonten beargumenteren dat dit onnodig streng is: het aantal patiënten dat MRSA meebrengt uit het buitenland is klein, wat dus veel onnodige isolatie betekent. Strikte isolatie van varkensboeren is ook te streng, omdat de 'varkensMRSA' zich minder gemakkelijk onder mensen lijkt te verspreiden dan de humane variant. Al met al, veel isolatiedagen voor niets.
Hoe moet het dan wel? Wassenberg en Bonten stellen voor om risicopatiënten helemaal niet meer te isoleren en hier pas toe over te gaan als de uitslag van de test op MRSA positief is. De vraag is of dit verstandig is.
Allereerst komt MRSA weinig voor in Nederland mede dankzij het tot nu toe gevoerde beleid. Zeggen dat het beleid niet nodig is omdat MRSA weinig voorkomt is een kringredenering. Ten tweede heeft onderzoek enkele jaren geleden aangetoond dat MRSA verspreiding in Nederlandse ziekenhuizen alleen plaats vindt wanneer niet bekend is dat patiënten drager zijn, d.w.z. wanneer géén isolatiemaatregelen genomen worden1. Als wij het voorstel van Wassenberg zouden volgen betekent dit dat bij een aantal patiënten die drager zijn gedurende een aantal dagen géén maatregelen genomen worden. Ten derde blijkt uit Engels onderzoek dat diagnostiek gevolgd door isolatie pas wanneer de uitslag van de test positief is, geen effect heeft op het voorkómen van MRSA verspreiding2. De conclusie van de Engelse onderzoekers is dat isoleren op eenpersoonskamers niet nuttig is. In het licht van de geciteerde Nederlandse studie lijkt het meer waarschijnlijk dat pas isoleren bij het positief worden van de kweken te laat is.
De conclusie van Wassenberg, dat wij veel patiënten streng isoleren, terwijl het aantal patiënten dat daadwerkelijk MRSA drager is klein is, onderschrijf ik. De vraag is of geen enkele maatregel nemen, zoals zij voorstaat, de juiste oplossing is. MRSA wordt vooral overgedragen via direct contact, in mindere mate aërogeen. Handschoenen, schorten en handdesinfectie behoren tot de maatregelen die genomen moeten worden bij contactisolatie. Waarom dan niet de strikte isolatie in afwachting van de testuitslag versoepelen tot contactisolatie i.p.v. geen enkele maatregel meer nemen? De contactisolatie kan dan bij een negatieve test opgeheven worden, bij een positieve test omgezet in strikte isolatie. Daarmee blijven we met een minimale belasting voor patiënt en medewerker toch alert op MRSA, om de gunstige situatie die we nu hebben in Nederland verder te waarborgen.
Christina Vandenbroucke-Grauls
M.I. Esveld et al, Ned Tijdschr Geneeskd. 1999;143:205-8.
Cepeda JA et al Lancet 2005;365:295-304.
MRSA-beleid (antwoord 2)
De reactie van collega Vandenbroucke-Grauls heeft ons verrast, want de aangevoerde argumenten lijken haar claim allerminst te ondersteunen. Het Nederlandse MRSA-beleid bestaat uit meerdere componenten die in gezamenlijkheid en zonder solide wetenschappelijke onderbouwing zijn geïmplementeerd. Het feit dat het gehele pakket succesvol is (af te lezen aan het geringe aantal MRSA-infecties in Nederlandse ziekenhuizen) en derhalve niet veranderd mag worden, zelfs niet op basis van een veranderde epidemiologie1, snellere diagnostiek en onderzoek, vinden wij een dogmatische kringredenering. Het is waar dat "MRSA verspreiding in Nederlandse ziekenhuizen alleen plaats vindt wanneer niet bekend is dat patiënten drager zijn". Echter, de meerderheid van die patiënten behoren niet tot de risicogroepen en worden dus helemaal niet gescreend. De aangehaalde studie van Esveld2 laat duidelijk zien dat secundaire besmetting vooral optreedt bij MRSA dragers zonder geïdentificeerde risicofactor. Implementatie van ons voorstel zal hier geen enkel effect op hebben. Recente studies hebben het risico op transmissie bij onbeschermd MRSA-dragerschap gekwantificeerd3,4 en dat risico is in onze ogen, zeker gezien de voorgaande zin, en het feit dat “onbeschermde opname” van korte duur zal zijn (in afwachting van sneldiagnostiek) acceptabel. De verwijzing naar de studie van Cepada5 begrijpen we niet, omdat dat onderzoek plaatsvond op Engelse IC-afdelingen, met veel minder maatregelen en zonder sneldiagnostiek van MRSA-dragerschap. In die studie waren kweekuitslagen pas na drie dagen bekend, waarna werd overgegaan tot (cohort) isolatie.
Wij onderschrijven de wens (en noodzaak) om het aantal infecties veroorzaakt door multi-resistente bacteriën in Nederlandse ziekenhuizen zo laag mogelijk te houden volledig. We zijn het echter niet eens met de constatering dat het instellen en naleven van dergelijke maatregelen voor ziekenhuismedewerkers een minimale belasting is. Aangezien het aantal te isoleren patiënten in de toekomst alleen maar zal toenemen, stellen wij een infectiepreventiebeleid voor dat optimaal gebruik gemaakt van de diagnostische mogelijkheden en epidemiologische inzichten, gebaseerd op wetenschappelijk onderzoek.
Marjan Wassenberg, Mark Bonte
Vandenbroucke-Grauls CMJE et al. Ned Tijdschr Geneeskd. 2006;150:1710-2.
Esveld MI et al. Ned Tijdschr Geneesk. 1999;143:205-8.
Wassenberg et al. Clin Microbiol Infect. 2010; May 3 [Epub ahead of print]
Bootsma et al. J R Soc Interface. 2010 Sep 22. [Epub ahead of print]
Cepada JA et al. Lancet 2005;365:295-304.