Toets voor nascholing (verlopen)
Aan dit leerartikel was een toets gekoppeld waarmee je nascholingspunten kon verdienen.
Samenvatting
Het hepatorenaal syndroom (HRS) is een ernstige complicatie bij patiënten met levercirrose en gaat gepaard met een hoge mortaliteit.
Nieuwe inzichten in de pathofysiologie hebben geleid tot verbeterde behandelingsstrategieën, maar levertransplantatie blijft vooralsnog de enige effectieve therapie.
Levercirrose en portale hypertensie gaan gepaard met cardiovasculaire disfunctie en arteriële vaatverwijding, met name in het splanchnicusvaatbed. Dit resulteert in nierinsufficiëntie door intrarenale vasoconstrictie en wordt vaak geluxeerd door spontane bacteriële peritonitis, gastro-intestinale bloedingen en gebruik van diuretica en niet-steroïde anti-inflammatoire geneesmiddelen (NSAID’s).
Nieuwe behandelingen grijpen aan op de verstoorde hemodynamiek. Terlipressine, volume-expansie met albumine en plaatsing van een transjugulaire intrahepatische portosystemische shunt hebben geleid tot betere overlevingskansen voor patiënten met HRS.
Preventieve maatregelen die de kans op HRS verlagen zijn antibiotische profylaxe voor patiënten met een hoog risico op spontane bacteriële peritonitis en albumine-infusie bij patiënten met spontane bacteriële peritonitis.
Nieuwe behandelingsstrategieën bieden de kans om de tijd tot levertransplantatie te overbruggen en leiden tot betere resultaten na het ontvangen van het transplantaat.
artikel
Het hepatorenaal syndroom (HRS) is een relatief frequente en gevreesde complicatie, die voorkomt bij patiënten met levercirrose. Deze aandoening wordt beschouwd als het eindresultaat van extreme hemodynamische veranderingen door leverfalen. Hierbij staan ernstige nierfunctiestoornissen op de voorgrond. Levertransplantatie is vooralsnog de enige effectieve therapie voor HRS. Door het vaak snel progressieve beloop overlijden veel patiënten al voor het beschikbaar komen van een donorlever. In het Tijdschrift werd in 1981 voor het laatst uitgebreid aandacht besteed aan dit onderwerp.1 Destijds bleven nog veel vragen onbeantwoord over het ontstaansmechanisme. Een beter inzicht hierin heeft anno 2009 geleid tot nieuwe behandelingsstrategieën.2 Hiermee probeert men de tijd tussen het optreden van HRS en het beschikbaar komen van een geschikte donorlever te overbruggen.
In dit artikel bespreken wij deze recente inzichten. Ook gaan wij in op de diagnostiek, behandelingsmogelijkheden en het nut van preventie van het hepatorenaal syndroom.
Klinische presentatie
Het klinische beeld van HRS wordt gekenmerkt door ascitesvorming, hypotensie en oligurie. Patiënten hebben een lage serumnatriumconcentratie door verdunning en vertonen de bekende tekenen van vergevorderd leverfalen (dat wil zeggen icterus, verhoogde bloedingsneiging, ascites, hepatische encefalopathie); hun mediane child-pugh-score bedraagt 11,2 (zie kader Uitleg).3
Op basis van het klinische beeld wordt een onderscheid gemaakt tussen twee typen HRS.
HRS type 1 HRS type 1 komt het meest voor. Deze vorm treedt op bij patiënten met ernstige leverafwijkingen en wordt vrijwel altijd voorafgegaan door een luxerend moment, zoals een bacteriële infectie en bloedingen van de tractus digestivus. HRS type 1 betreft de acute vorm van HRS met een snel progressieve nierinsufficiëntie, maar ook disfunctie van hart, hersenen, lever, bijnieren en van de systemische circulatie.4 De klinische manifestatie omvat dan ook leverfalen met icterus, stollingsstoornissen en hepatische encefalopathie.5 Daarnaast verdubbelt de serumcreatinineconcentratie binnen een tijdsbestek van 2 weken tot waarden boven de 226 µmol/l. HRS type 1 kent een hoge mortaliteit: de mediane overleving zonder transplantatie bedraagt slechts 3-9 weken.
HRS type 2 HRS type 2 treedt op bij patiënten met progressie van leverinsufficiëntie. Vaak hebben deze patiënten therapieresistente ascites. In het algemeen ontstaat HRS type 2 zonder een duidelijke luxerende factor. De circulatoire disfunctie en de lever- en nierfunctiestoornissen nemen geleidelijk in enkele maanden toe (serumcreatinine: 133-226 µmol/l). De 2-jaarsoverleving zonder transplantatie is 30-58%.2,6
Pathofysiologie
Aan het optreden van acute nierinsufficiëntie in het kader van het HRS ligt een verstoorde hemodynamiek ten grondslag. Dergelijke circulatoire problemen worden met name gezien bij patiënten met vergevorderde levercirrose en treden in mindere mate op bij patiënten met een ernstige alcoholische hepatitis of met fulminant leverfalen.7
Vaatverwijding Bij patiënten met progressieve levercirrose leidt portale hypertensie tot vaatverwijding in de systemische circulatie (figuur 1). Deze vasodilatatie is het meest uitgesproken in het arteriële vaatbed van het splanchnicusgebied en wordt veroorzaakt door verhoogde concentraties ontstekingsmediatoren en vaatverwijdende mediatoren in het bloed. Deze chronische inflammatoire status bij levercirrose is vermoedelijk een reactie op translocatie van bacteriën vanuit het darmlumen naar mesenteriale lymfklieren. Dit is mogelijk door de verminderde barrièrefunctie van de darmwand als gevolg van de verhoogde druk in het portale vaatbed.8
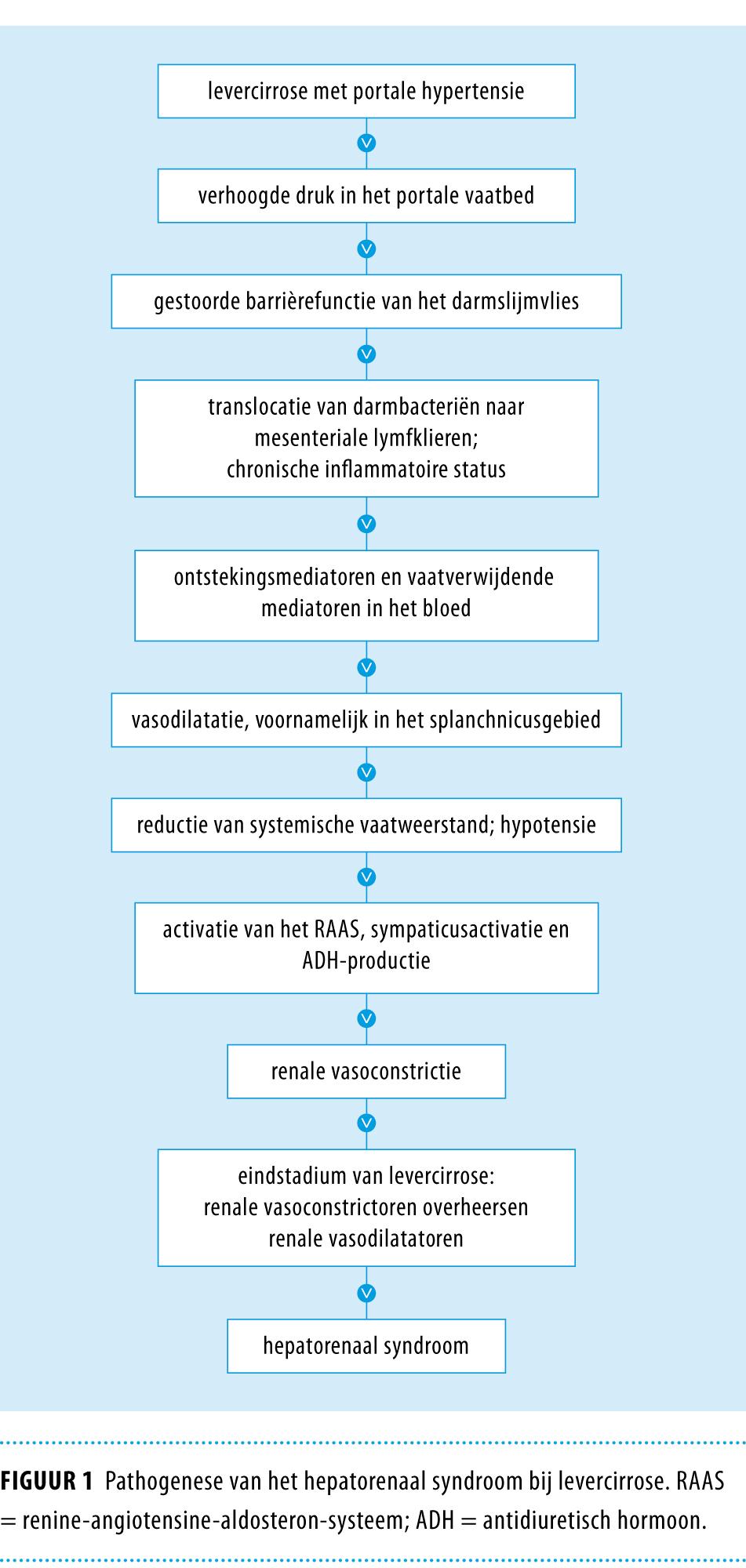
Cirrotische cardiomyopathie Circulerende vasodilatatoren die verantwoordelijk zijn voor de vaatverwijding zijn onder andere stikstofmonoxide (NO), glucagon en vasoactief intestinaal polypeptide (VIP).9 Naast een verhoogde productie van vasodilatatoren bij een verhoging van de portale druk, is er een verminderde afbraak van vasodilatatoren in de lever door portosystemische collateralen en een verminderde leverfunctie.10 De vaatverwijding resulteert in een verlaagd effectief circulerend volume, hetgeen aanvankelijk wordt gecompenseerd door een toename van de hartfrequentie en het hartminuutvolume.
Wanneer het leverfalen voortduurt met toename van vasodilatatie in het splanchnische vaatbed schiet deze zogenaamde hyperdynamische circulatie tekort. Dit fenomeen is recent beschreven als aparte klinische entiteit en is ‘cirrotische cardiomyopathie’ genoemd. Zij onderscheidt zich van de alcoholische cardiomyopathie die vaker wordt waargenomen bij levercirrose. De cardiale afwijkingen omvatten zowel systolische als diastolische disfunctie en een verlengd QT-interval.
Renale hypoperfusie Samen met een verlaagd circulerend volume ontstaat vervolgens renale hypoperfusie.10-12 De bloeddrukdaling die hiervan het gevolg is resulteert in de activatie van het renine-angiotensine-aldosteron-systeem (RAAS), het sympatische zenuwstelsel en verhoogde secretie van het antidiuretisch hormoon (ADH) in de hypofyse. Het homeostatisch gunstige effect van deze mechanismen op de bloeddruk gaat echter ten koste van de renale circulatie. Als gevolg van de vasoconstrictie in de nierarteriën treedt een verdere reductie van de nierperfusie en van de glomerulaire filtratiesnelheid (GFR) op. In de vroege fase van gedecompenseerde levercirrose leidt dit nog niet tot problemen, omdat renale autoregulerende vaatverwijdende factoren, onder andere prostaglandine E2 en NO, de doorbloeding van de nieren waarborgen. Echter, wanneer de ziekte voortduurt, overschrijdt de activiteit van systemische vasoconstrictieve mediatoren, zoals endotheline en tromboxaan A2, de potentie van de renale vaatverwijdende autoregulatie (figuur 2).5,7,9 Hierdoor wordt de perfusie van de nieren direct afhankelijk van de systemische bloeddruk.
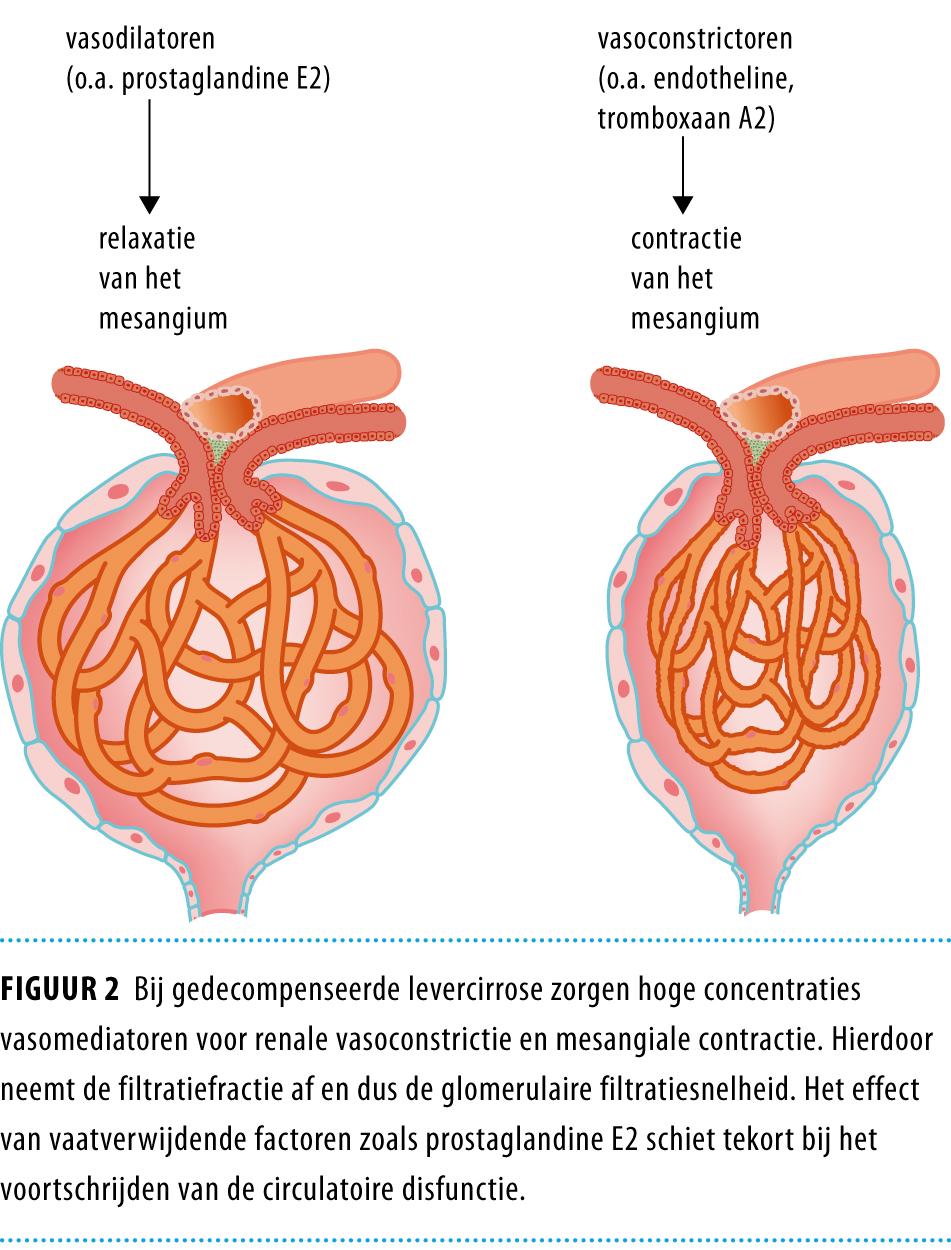
Wanneer de bloeddruk vervolgens verder afneemt, leidt dit tot progressieve renale hypoperfusie en ontwikkeling van HRS type 1. De belangrijkste oorzaken van verdere systemische bloeddrukdaling zijn paracentese zonder (adequate) volume-expansie, diarree, gastro-intestinale bloedingen, bacteriële infecties en in het bijzonder spontane bacteriële peritonitis.13 Behandeling met niet-steroïde anti-inflammatoire geneesmiddelen (NSAID’s), met name prostaglandinesynthetaseremmers, kan eveneens leiden tot acuut nierfalen doordat het vaatverwijdende effect van prostaglandinen op de renale circulatie teniet wordt gedaan. Andere nefrotoxische factoren, zoals antibiotica en intraveneuze röntgencontrastmiddelen, die niet op dit mechanisme aangrijpen, kunnen een verdere verslechtering van de nierfunctie induceren. Patiënten met levercirrose zijn gevoeliger voor de nefrotoxische effecten van deze middelen door ondervulling.
Differentiaaldiagnostiek
De diagnose ‘HRS’ wordt per exclusionem gesteld. Het onderscheid tussen HRS en andere oorzaken van nierinsufficiëntie heeft cruciale therapeutische gevolgen en verschaft inzicht in de prognose van de aandoening. Het differentiëren tussen deze oorzaken is echter niet altijd even gemakkelijk.
Bij de pathogenese van acute nierinsufficiëntie wordt traditioneel een verdeling gemaakt in prerenale, renale en postrenale oorzaken. Al deze vormen van nierfalen kunnen zich ontwikkelen bij patiënten met levercirrose. Bij deze patiënten zijn de meest voorkomende oorzaken van acuut nierfalen prerenale oorzaken ten gevolge van volumedepletie (45%), acute tubulusnecrose (32%) en HRS (23%).3
Prerenale nierinsufficiëntie op basis van hypovolemie Men kan differentiëren tussen HRS en prerenale nierinsufficiëntie op basis van volumedepletie door het circulerend volume te herstellen. Prerenale nierinsufficiëntie als gevolg van ondervulling verbetert per definitie na adequate vulling. De bepaling van het volumetekort bij patiënten met levercirrose is echter lastig. Patiënten hebben naast een verminderd circulerend volume namelijk ook ascites en perifeer oedeem. Bij patiënten met HRS treedt geen herstel op van de nierfunctie na herstellen van het intravasculaire compartiment.
Acute tubulusnecrose Acute tubulusnecrose is het syndroom dat optreedt als gevolg van de invloed van één of meer ischemische of nefrotoxische factoren die leiden tot beschadiging van niertubuli. Medicijnen die vaak een toxische tubulusnecrose tot gevolg hebben zijn NSAID’s, aminoglycosiden, diuretica en intraveneuze röntgencontrastmiddelen.
Bij ischemische tubulusnecrose wordt een hypotensieve episode voornamelijk uitgelokt door een bloeding, bijvoorbeeld een gastro-intestinale, of door een ernstige sepsis. Dezelfde omstandigheden vormen ook frequent de precipiterende factor voor het HRS. Bij acute tubulusnecrose is de tubulusfunctie gestoord. Dit onderscheidt een acute tubulusnecrose van HRS, waarbij structurele nierafwijkingen ontbreken. Bij patiënten met HRS vindt in de tubulus fysiologische terugresorptie van het natrium plaats met als doel de relatieve ondervulling te compenseren. Dit resulteert in lage natriumwaarden in de urine (Na: < 20 mmol/l) en een lage fractionele natriumexcretie bij een verhoogde urine-osmolaliteit. Daarentegen zijn de natriumwaarden in de urine bij acute tubulusnecrose juist hoog (Na: > 40 mmol//l), met een hoge fractionele natriumexcretie en een lage urine-osmolaliteit. Echter, wanneer acute tubulusnecrose optreedt bij patiënten met levercirrose volgen deze waarden een ander patroon, waarbij juist een lage fractionele natriumexcretie wordt gezien. Dit maakt het gebruik van urine-Na-waarden en de fractionele natriumexcretie minder geschikt om te differentiëren tussen deze twee afwijkingen en hebben zodoende geen plaats meer in de diagnostische criteria van HRS.3
Diagnostiek
De diagnostische criteria voor HRS zijn recent gewijzigd (tabel 1).2 De initiële stap in het diagnostisch proces is het vaststellen van een mogelijke nierfunctiestoornis. Echter, bij patiënten met levercirrose is het accuraat vaststellen van de nierfunctie niet eenvoudig. Het zorgvuldig bepalen van de restfunctie van de nieren is van cruciaal belang voor diagnostische en therapeutische interventies en het optimaal doseren van medicatie.
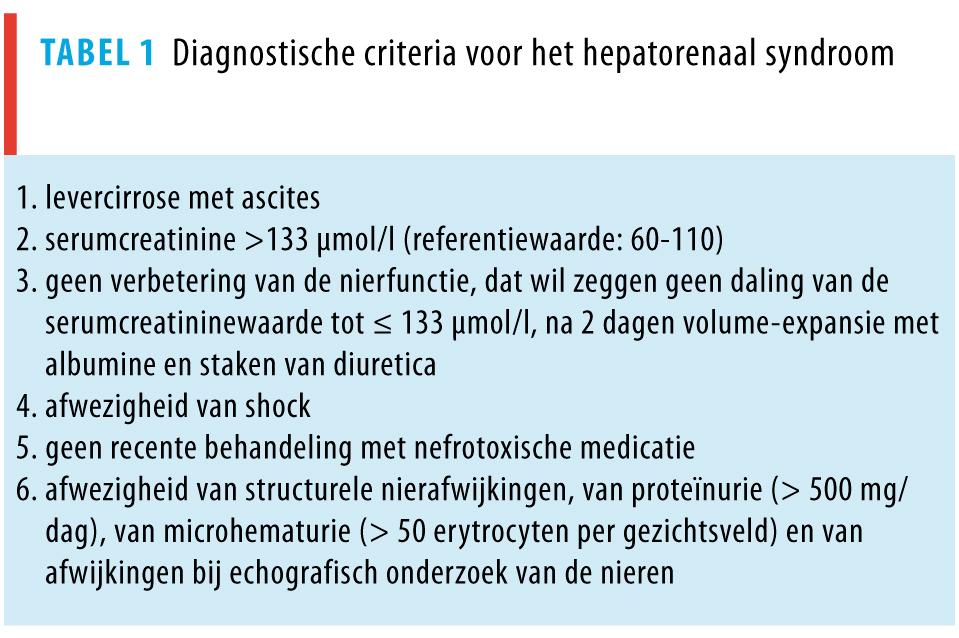
Serumcreatinineklaring onbruikbaar De creatinineklaring maakt geen deel meer uit van de geactualiseerde criteria. Het berekenen van de nierfunctie bij patiënten met levercirrose wordt mogelijk overschat als geen rekening wordt gehouden met de klinische kenmerken van deze patiënten. De creatinineklaring kan worden benaderd met behulp van de formule van Cockcroft en Gault. Deze formule is gebaseerd op de leeftijd, het gewicht en het geslacht van de patiënt en de creatininewaarde in het serum. Bij patiënten met levercirrose is de serumcreatininewaarde verlaagd, onder meer als gevolg van een slechte voedingsstatus, een afgenomen spiermassa en een verminderde aanmaak van creatine in de cirrotische lever. Dientengevolge kan de serumcreatininewaarde binnen de referentiewaarden liggen terwijl de GFR toch verlaagd is.15
Ook de berekening van de GFR met de ‘Modification of diet in renal disease’(MDRD)-formule is in het geval van acuut nierfalen ontoereikend, omdat ook bij deze berekening van de nierfunctie een serumcreatininewaarde vereist is die in een evenwicht (‘steady state’) verkeert. Bij een progressieve nierfunctiestoornis is dat per definitie niet het geval.15
Bepaling van serumcystatine C Van de nieuw ontwikkelde methoden om de klaring te berekenen is met name de bepaling van serumcystatine C veelbelovend.16 Cystatine C is een eiwit dat constant wordt afgegeven door kernhoudende cellen en vrijwel uitsluitend wordt uitgescheiden middels glomerulaire filtratie. In verschillende studies wordt een sterke correlatie gevonden tussen de uitslag van serumcystatine C en de GFR bij patiënten met levercirrose of HRS.17,18 Als kanttekening dient hierbij de grote interindividuele variabiliteit te worden geplaatst. Mede hierdoor heeft deze goedkope en eenvoudige bepaling nog geen ingang gevonden in de klinische praktijk.
Serumcreatininewaarde Tot op heden blijft de creatininewaarde in het serum de belangrijkste marker voor het diagnosticeren van acuut nierfalen bij patiënten met levercirrose (zie tabel 1). Hierbij dient de clinicus, die betrokken is bij de behandeling van de patiënten met HRS, zich bewust te zijn van de mogelijke overschatting van de nierfunctie.
Bij patiënten met levercirrose treedt in aansluiting op een infectie vaak nierinsufficiëntie op. Soms herstelt de nierfunctie dan na geslaagde behandeling met antibiotica. In de verouderde consensus gaf dit aanleiding om de diagnose ‘HRS’ pas te stellen wanneer de infectie voldoende was behandeld. Bij een aanzienlijk deel van de patiënten ontwikkelt zich echter een progressieve nierfunctiestoornis ondanks effectieve behandeling van de infectie. Dit geldt met name voor patiënten met spontane bacteriële peritonitis.
Nu nieuwe inzichten suggereren dat de ontwikkeling van acute nierinsufficiëntie bij patiënten met levercirrose en een infectie en het optreden van HRS bij patiënten zonder infectie een gemeenschappelijke pathogenese hebben, kan de diagnose ‘HRS’ ook gesteld worden bij patiënten met levercirrose en een intercurrente infectie.2 Beide entiteiten worden namelijk gekenmerkt door eenzelfde circulatoire disfunctie met activatie van endogene vasoactieve systemen en ontwikkeling van nierfunctiestoornissen.19
Preventie van HRS
Primaire antibiotische profylaxe Patiënten met cirrose zijn bijzonder gevoelig voor infecties.20 Bij deze patiëntenpopulatie kunnen infecties, met name spontane bacteriële peritonitis, de luxerende factor vormen voor ontwikkeling van HRS. Circa 30% van de patiënten met spontane bacteriële peritonitis ontwikkelt HRS.9 Met name patiënten met een child-pugh-score ≥ 9 en lage eiwitconcentraties in de ascitesvloeistof hebben een hoog risico op spontane bacteriële peritonitis.21 Primaire antibiotische profylaxe bij deze patiënten reduceert de kans op ontwikkeling van spontane bacteriële peritonitis en vertraagt de ontwikkeling van HRS in vergelijking met behandeling met een placebo. Met name patiënten met een slechte nierfunctie lijken baat te hebben bij profylaxe met antibiotica. Dit leidt tot een daling van de sterfte in de eerste 3 maanden, maar niet na 12 maanden.22 Tegenstanders wijzen op de gevaren van resistentieontwikkeling bij het gebruiken van antibiotica als profylactisch middel.
Antibiotische profylaxe wordt ook geadviseerd bij patiënten met levercirrose en een gastro-intestinale bloeding. Bloedingen van de tractus digestivus zijn nog steeds geassocieerd met een hoge sterfte, met name in de aanwezigheid van een infectie. De mortaliteit bedraagt tot 30% na 3 weken. Kortdurende behandeling, gemiddeld 7 dagen, met antibiotica is effectief gebleken in het voorkómen van infecties en gaat gepaard met een betere overleving.23
Albumine-infusie bij spontane bacteriële peritonitis Bij patiënten met levercirrose en spontane bacteriële peritonitis wordt aangenomen dat albumine-infusie de kans op het ontwikkelen van HRS verkleint. Dit werkingsmechanisme van albumine is tot op heden niet geheel opgehelderd. Naast volume-expansie en antioxidatieve eigenschappen, is een mogelijke verklaring voor het gunstige effect van albumineinfusie bij HRS de bindingscapaciteit van albumine. Hierdoor worden vasodilatatoren en cytokinen gebonden.24 Als gevolg hiervan wordt progressie van circulatoire disfunctie voorkomen. Twee gerandomiseerde studies tonen dit effect van albumine aan: intraveneuze behandeling met albumine (1,5 g albumine/kg lichaamsgewicht bij het stellen van de diagnose ‘spontane bacteriële peritonitis’, na 48 h gevolgd door 1 g albumine/kg lichaamsgewicht) leidt tot een betere overleving.25,26 Hoewel op deze onderzoeken kritiek is geuit,27 zijn de auteurs het eens over het nut van albumine bij spontane bacteriële peritonitis ter preventie van HRS. Patiënten met een ongestoorde nierfunctie lijken echter geen profijt te hebben van behandeling met albumine.
Behandeling
Centraal in de pathofysiologie van HRS staat de portale hypertensie met ernstige circulatoire disfunctie, zoals hierboven werd beschreven. Nieuwe behandelingsstrategieën grijpen aan op deze verstoorde hemodynamiek.
Volume-expansie door vasoconstrictoren Terlipressine is een vasopressine-analoog dat de tonus in de splanchnische vaten verhoogt (tabel 2). Dit leidt tot herstel van het effectief circulerend volume en van de renale perfusie, met herstel van de nierfunctie.28

In een systematische cochrane-review werden 3 gerandomiseerde studies met in totaal 48 patiënten met HRS type 1 en 2 opgenomen in de analyse.29 Intraveneuze toediening van terlipressine heeft een gunstige invloed op de overleving. In de interventiegroep stierven 5 van de 25 patiënten (20%). In de placebogroep bedroeg de sterfte 65% (15 van de 23 patiënten); het risicoverschil was -34% (95%-BI: -0,56 - -0,12). Deze mortaliteitsreductie wordt toegeschreven aan het gunstige effect van terlipressine op de nierfunctie. De serumcreatinineconcentratie daalde met gemiddeld 219 µmol/l. Er werden geen ernstige bijwerkingen gemeld. Wel is voorzichtigheid geboden bij patiënten met bekende cardiale problemen, vanwege de kans op ritmestoornissen. Een andere bekende complicatie is het optreden van ischemie, met name in de kransslagaderen en extremiteiten.30
Er zijn dus aanwijzingen dat een succesvolle behandeling met terlipressine een gunstig effect heeft op de overleving bij patiënten met HRS. Het effect van combinatietherapieën (albumine, versgevroren plasma, zout- en vochtbeperking) kon niet worden vastgesteld. Studies met grotere onderzoekspopulaties zijn nodig om definitief de plaats van terlipressine in de behandeling van HRS te bepalen. Met andere vasoconstrictoren, zoals midodrine en norepinefrine, is minder ervaring. De effecten van deze middelen worden onderzocht in een aantal lopende studies.
Volume-expansie door albumine Verschillende onderzoeken hebben aangetoond dat albumine het effect van terlipressine potentieert bij patiënten met levercirrose en HRS (zie tabel 2). Een gecombineerde behandeling met albumine en terlipressine resulteert in een significant beter herstel van de nierfunctie.31,32
Transjugulaire intrahepatische portosystemische shunt Bij toepassing van een TIPS wordt een verbinding aangelegd tussen de V. hepatica en de V. portae hepatis (figuur 3). Hierdoor daalt de druk in het portale vaatbed, stijgt het hartminuutvolume en treedt volume-expansie van de centrale circulatie op. Bij patiënten met HRS leidt deze bloeddrukstijging onder andere tot een reductie van de RAAS-activatie. Hierdoor kan de doorbloeding van de nieren herstellen en de nierfunctie verbeteren.33
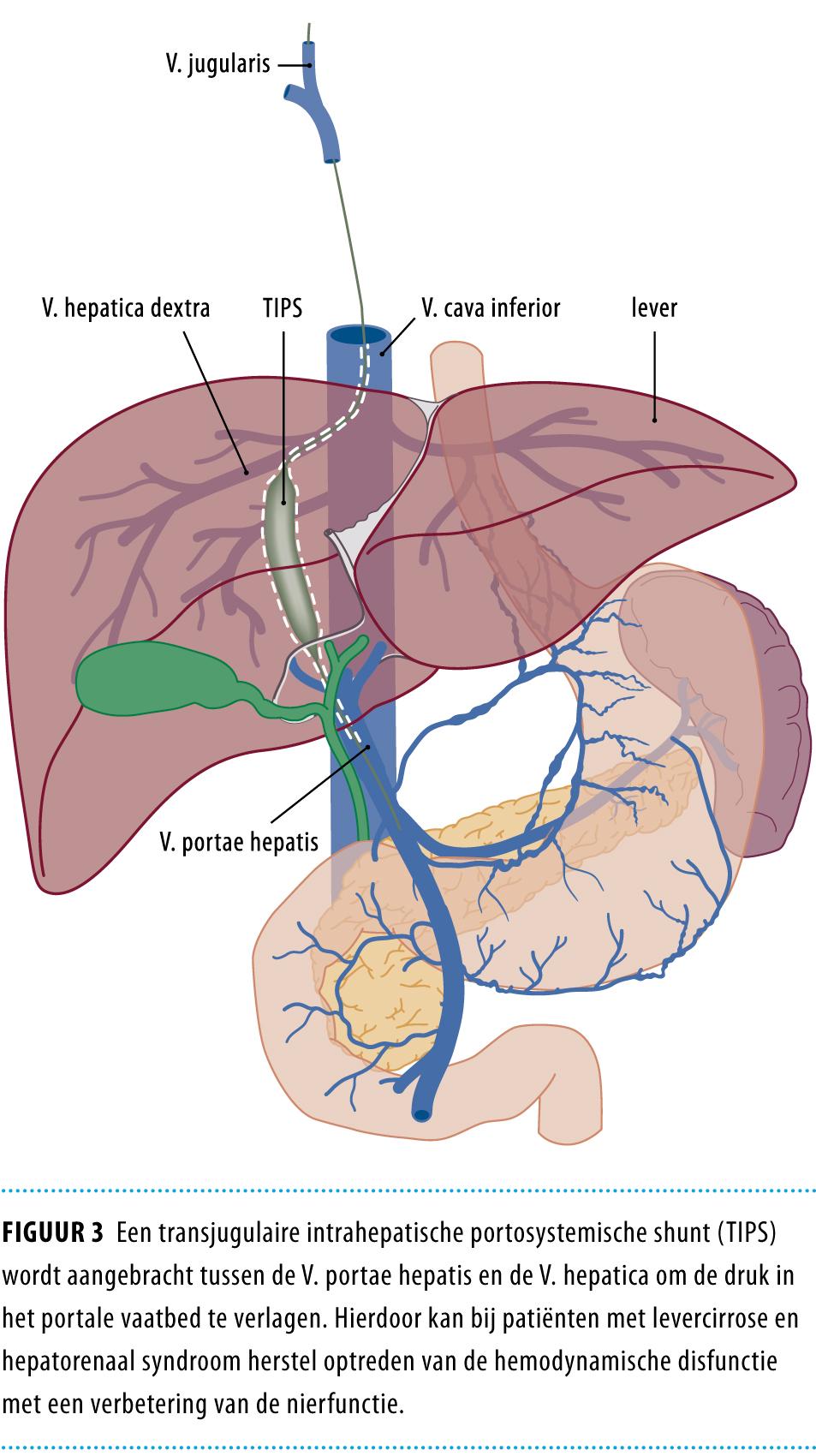
TIPS wordt al langer gebruikt bij therapieresistente bloedingen hoog in de tractus digestivus en bij refractaire ascites en kan bij sommige patiënten de voorkeur verdienen boven frequente paracentese. Wanneer bij patiënten met HRS type 1 nierfunctieherstel optreedt na behandeling met vasoconstrictoren en albumine kan een verdere verbetering of zelfs normalisering van de nierfunctie worden bereikt door plaatsing van een TIPS. De patiënten die hiervoor in aanmerking komen, dienen zorgvuldig geselecteerd te worden. Contra-indicaties voor TIPS zijn een recente actieve infectie, ernstige stollingsstoornissen, een child-pugh-score > 12 en een snelle neiging tot ontwikkeling van hepatische encefalopathie.34-36
Levertransplantatie Vóór de introductie van vasoconstrictoren en TIPS was levertransplantatie de enige effectieve therapie voor patiënten met HRS. Ook na het beschikbaar komen van deze behandelingsmogelijkheden blijft transplantatie de behandeling van eerste keuze voor deze patiënten. Veel patiënten met HRS type 1 overlijden echter voordat een donorlever beschikbaar is. Met de nieuwe behandelingsstrategieën wordt getracht de tijd tot transplantatie te overbruggen. Een donorlever biedt als voordeel dat de onderliggende leverziekte wordt genezen en dat daarna herstel kan optreden van de circulatoire en renale disfunctie. De 3-jaarsoverleving van patiënten met HRS die levertransplantatie ondergaan is 60%. De langetermijnoverleving van patiënten met levercirrose, maar zonder HRS vóór de transplantatie is 70-80%.37
Een adequate behandeling van HRS vóór transplantatie leidt tot minder morbiditeit erna. Van de patiënten met HRS vóór de transplantatie hebben er daarna meer dialyse nodig dan van de patiënten zonder HRS. De nierfunctie bij patiënten zonder HRS die een levertransplantatie krijgen, blijft beter gepreserveerd dan bij patiënten met HRS vóór de transplantatie.37
Conclusie
Het hepatorenaal syndroom is een ernstige complicatie van levercirrose in een vergevorderd stadium. Het stellen van de diagnose stelt de clinicus voor een grote uitdaging. Voortschrijdend inzicht in de pathofysiologische mechanismen achter dit ernstige syndroom leveren aangrijpingspunten voor verbeterde behandelingsmogelijkheden.
Grote gerandomiseerde multicenterstudies zijn nodig om meer richting te geven aan de optimale behandeling, zodat de slechte prognose van patiënten met HRS verder kan verbeteren.
Uitleg
Child-pugh-classificatie De child-pugh-classificatie wordt gebruikt om de prognose van chronische leverziekte in te schatten. Afhankelijk van scores voor de serumwaarden van bilirubine en albumine, de protrombinetijd, en het al dan niet aanwezig zijn van ascites en hepatische encefalopathie wordt onderscheid gemaakt in klasse A (score: 5-6), B (score: 7-9) en C (score: 10-15), waarbij de 1-jaarsoverleving varieert van 100% in klasse A tot 45% in klasse C.
Leerpunten
Centraal in de pathofysiologie van het hepatorenaal syndroom staat extreme vaatverwijding in het splanchnische vaatbed door portale hypertensie als gevolg van levercirrose.
Homeostatische mechanismen om het effectief circulerend volume te handhaven leiden tot renale hypoperfusie en ernstige nierfunctiestoornissen.
Cirrotische cardiomyopathie draagt bij aan de hypoperfusie van de renale circulatie.
Onderzoeken naar een gecombineerde behandeling met terlipressine en albumine, alsmede studies naar plaatsing van een transjugulaire intrahepatische portosystemische shunt tonen een gunstig effect op de morbiditeit en overlevingskansen bij patiënten met hepatorenaal syndroom.
Literatuur
Batenburg PL. Het hepatorenale syndroom. Ned Tijdschr Geneeskd. 1981;125:1834-9.
Salerno F, Gerbes A, Gines P, Wong F, Arroyo V. Diagnosis, prevention and treatment of hepatorenal syndrome in cirrhosis. Gut. 2007;56:1310-8.
Garcia-Tsao G, Parikh CR, Viola A. Acute kidney injury in cirrhosis. Hepatology. 2008;48:2064-77.
Gines P, Schrier RW. Renal failure in cirrhosis. N Engl J Med 2009 Sep 24;361:1279-90.
Dagher L, Moore K. The hepatorenal syndrome. Gut. 2001;49:729-37.
Angeli P. Review article: prognosis of hepatorenal syndrome--has it changed with current practice? Aliment Pharmacol Ther. 2004;20(Suppl 3):44-6.
Arroyo V, Jimenez W. Complications of cirrhosis. II. Renal and circulatory dysfunction. Lights and shadows in an important clinical problem. J Hepatol. 2000;32(1 Suppl):157-70.
Wiest R, Garcia-Tsao G. Bacterial translocation (BT) in cirrhosis. Hepatology. 2005;41:422-33.
Arroyo V, Terra C, Gines P. Advances in the pathogenesis and treatment of type-1 and type-2 hepatorenal syndrome. J Hepatol. 2007;46:935-46.
Moller S, Henriksen JH. Cardiovascular complications of cirrhosis. Gut. 2008;57:268-78.
Ma Z, Lee SS. Cirrhotic cardiomyopathy: getting to the heart of the matter. Hepatology. 1996;24:451-9.
Ruiz-del-Arbol L, Monescillo A, Arocena C, Valer P, Gines P, Moreira V, et al. Circulatory function and hepatorenal syndrome in cirrhosis. Hepatology. 2005;42:439-47.
Gines P, Guevara M, Arroyo V, Rodes J. Hepatorenal syndrome. Lancet. 2003;362:1819-27.
Stadhouders PH, Kuiper JJ, van Buuren HR, de Man RA. Spontane bacteriële peritonitis, een ernstige complicatie van levercirrose. Ned Tijdschr Geneeskd. 2007;151:509-13.
Sherman DS, Fish DN, Teitelbaum I. Assessing renal function in cirrhotic patients: problems and pitfalls. Am J Kidney Dis. 2003;41:269-78.
Hoek FJ, Kemperman FA, Krediet RT. A comparison between cystatin C, plasma creatinine and the Cockcroft and Gault formula for the estimation of glomerular filtration rate. Nephrol Dial Transplant. 2003;18:2024-31.
Demirtas S, Bozbas A, Akbay A, Yavuz Y, Karaca L. Diagnostic value of serum cystatin C for evaluation of hepatorenal syndrome. Clin Chim Acta. 2001;311:81-9.
Woitas RP, Stoffel-Wagner B, Flommersfeld S, Poege U, Schiedermaier P, Klehr HU, et al. Correlation of serum concentrations of cystatin C and creatinine to inulin clearance in liver cirrhosis. Clin Chem. 2000;46:712-5.
Terra C, Guevara M, Torre A, Gilabert R, Fernandez J, Martin-Llahi M, et al. Renal failure in patients with cirrhosis and sepsis unrelated to spontaneous bacterial peritonitis: value of MELD score. Gastroenterology. 2005;129:1944-53.
Tandon P, Garcia-Tsao G. Bacterial infections, sepsis, and multiorgan failure in cirrhosis. Semin Liver Dis. 2008;28:26-42.
Andreu M, Sola R, Sitges-Serra A, Alia C, Gallen M, Vila MC, et al. Risk factors for spontaneous bacterial peritonitis in cirrhotic patients with ascites. Gastroenterology. 1993;104:1133-8.
Fernandez J, Navasa M, Planas R, Montoliu S, Monfort D, Soriano G, et al. Primary prophylaxis of spontaneous bacterial peritonitis delays hepatorenal syndrome and improves survival in cirrhosis. Gastroenterology. 2007;133:818-24.
Bernard B, Grange JD, Khac EN, Amiot X, Opolon P, Poynard T. Antibiotic prophylaxis for the prevention of bacterial infections in cirrhotic patients with gastrointestinal bleeding: A meta-analysis. Hepatology. 1999;29:1655-61.
Quinlan GJ, Martin GS, Evans TW. Albumin: biochemical properties and therapeutic potential. Hepatology. 2005;41:1211-9.
Fernandez J, Monteagudo J, Bargallo X, Jimenez W, Bosch J, Arroyo V, et al. A randomized unblinded pilot study comparing albumin versus hydroxyethyl starch in spontaneous bacterial peritonitis. Hepatology. 2005;42:627-34.
Sort P, Navasa M, Arroyo V, Aldeguer X, Planas R, Ruiz-del-Arbol L, et al. Effect of intravenous albumin on renal impairment and mortality in patients with cirrhosis and spontaneous bacterial peritonitis. N Engl J Med. 1999;341:403-9.
Sigal SH, Stanca CM, Fernandez J, Arroyo V, Navasa M. Restricted use of albumin for spontaneous bacterial peritonitis. Gut. 2007;56:597-9.
Moreau R, Lebrec D. The use of vasoconstrictors in patients with cirrhosis: type 1 HRS and beyond. Hepatology. 2006;43:385-94.
Gluud LL, Kjaer MS, Christensen E. Terlipressin for hepatorenal syndrome. Cochrane Database Syst Rev. 2006;(4):CD005162.
Cardenas A. Hepatorenal syndrome: a dreaded complication of end-stage liver disease. Am J Gastroenterol. 2005;100:460-7.
Ortega R, Gines P, Uriz J, Cardenas A, Calahorra B, De Las HD, et al. Terlipressin therapy with and without albumin for patients with hepatorenal syndrome: results of a prospective, nonrandomized study. Hepatology. 2002;36(4 Pt 1):941-8.
Martin-Llahi M, Pepin MN, Guevara M, Diaz F, Torre A, Monescillo A, et al. Terlipressin and albumin vs albumin in patients with cirrhosis and hepatorenal syndrome: a randomized study. Gastroenterology. 2008;134:1352-9.
Huonker M, Schumacher YO, Ochs A, Sorichter S, Keul J, Rossle M. Cardiac function and haemodynamics in alcoholic cirrhosis and effects of the transjugular intrahepatic portosystemic stent shunt. Gut. 1999;44:743-8.
Guevara M, Gines P, Bandi JC, Gilabert R, Sort P, Jimenez W, et al. Transjugular intrahepatic portosystemic shunt in hepatorenal syndrome: effects on renal function and vasoactive systems. Hepatology. 1998;28:416-22.
Brensing KA, Textor J, Perz J, Schiedermaier P, Raab P, Strunk H, et al. Long term outcome after transjugular intrahepatic portosystemic stent-shunt in non-transplant cirrhotics with hepatorenal syndrome: a phase II study. Gut. 2000;47:288-95.
Wong F, Pantea L, Sniderman K. Midodrine, octreotide, albumin, and TIPS in selected patients with cirrhosis and type 1 hepatorenal syndrome. Hepatology. 2004;40:55-64.
Gonwa TA, Morris CA, Goldstein RM, Husberg BS, Klintmalm GB. Long-term survival and renal function following liver transplantation in patients with and without hepatorenal syndrome--experience in 300 patients. Transplantation. 1991;51:428-30.




Reacties