artikel
Dames en Heren,
Als een pasgeborene niet kan drinken en speekselbellen op de lippen heeft, moeten er alarmbellen gaan rinkelen. Deze symptomen kunnen wijzen op oesofagusatresie. Vroege herkenning van deze aangeboren afwijking aan de slokdarm is lastig, maar als de aandoening bij een neonaat over het hoofd wordt gezien,kan dit ingrijpende gevolgen hebben.
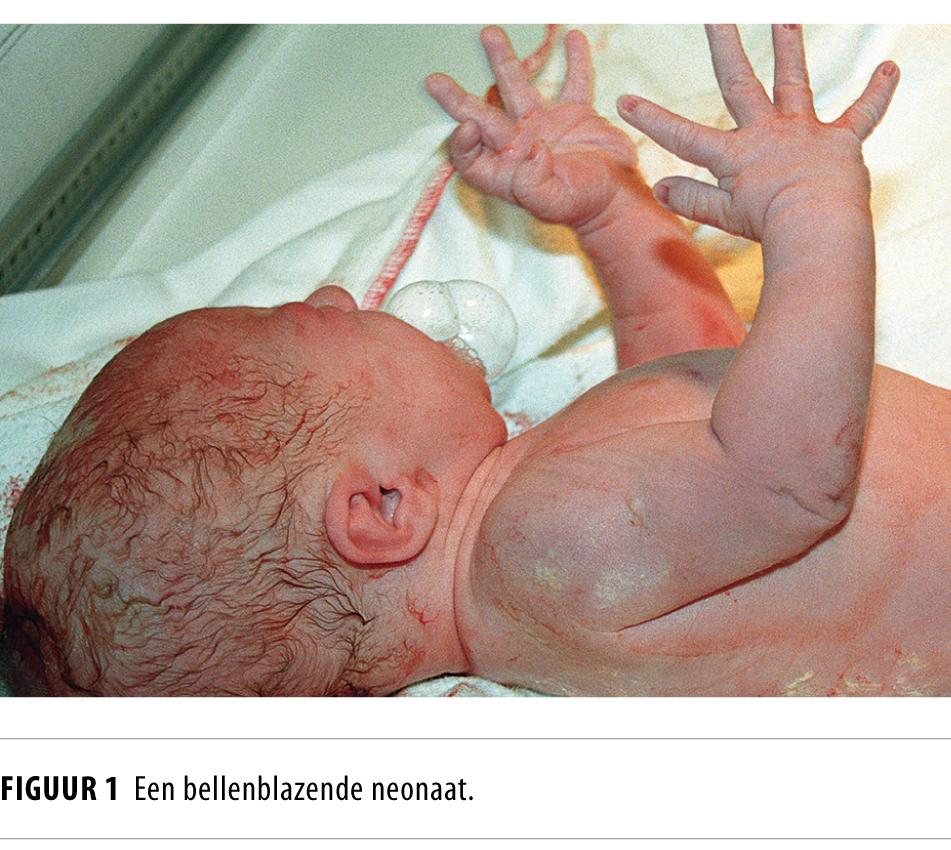
Oesofagusatresie is bij prenatale diagnostiek niet goed te herkennen. Het na de geboorte niet kunnen wegslikken van speeksel en als gevolg daarvan bellen blazen is daarentegen pathognomonisch voor de afsluiting van de slokdarm. Iedere zorgverlener die bij de zorg voor de pasgeborene betrokken is, zou de diagnose ‘oesofagusatresie’ moeten overwegen wanneer een pasgeborene niet drinkt, speekselvloed heeft, bellen blaast (figuur 1) en/of zich verslikt in de voeding. Welke gevolgen het kan hebben als oesofagusatresie niet meteen wordt herkend, laten wij aan de hand van 3 casussen zien.
Patiënt A is een jongetje dat na een ongecompliceerde zwangerschap bij een termijn van 39 3/7 weken met een gewicht van 3495 g werd geboren na een poliklinische bevalling in een algemeen ziekenhuis. Hij probeerde te drinken, maar spuugde alle borstvoeding meteen weer uit. De verloskundige vond bij lichamelijk onderzoek geen afwijkingen en de patiënt werd 3 hna de bevalling ontslagen. Thuis lukte de voeding ook niet. Patiënt spuugde, kokhalsde en had veel slijm in de mond met belvorming. De kraamhulp stelde de ouders gerust met de boodschap ‘spugen op de eerste dagen is normaal, de pasgeborene moet dan nog wennen aan de voeding’.
2 dagen na zijn geboorte brachten de inmiddels ongeruste ouders hun kind naar de Spoedeisende Hulp van een algemeen ziekenhuis. Bij opname zag men een matig-ernstig gedehydreerde neonaat met een gewicht van 3135 g. Een neus-maagsonde opvoeren bleek niet mogelijk. Op de thoraxfoto eindigde de sonde ter hoogte van de hoge thoracale wervelkolom; ook was er lucht in de maag. Hierop werd de diagnose ‘oesofagusatresie type C’ (zie beschouwing) gesteld en werd de patiënt overgeplaatst naar ons centrum. Na intraveneuze rehydratie en screening op andere aangeboren afwijkingen onderging hij op de 5e levensdag een corrigerende operatie, waarbij via een rechtszijdige thoracotomie de tracheo-oesofageale fistel werd onderbonden en een oesofago-oesofagostomie werd verricht. Postoperatief was er een voorspoedig herstel en patiënt kon snel naar huis ontslagen worden. 2 maanden na de operatie zagen wij de patiënt op de polikliniek terug. Hij dronk goed aan de borst en had inmiddels een gewicht van 4932 g.
Patiënt B is een meisje dat geboren werd bij een amenorroeduur van 36 5/7 weken middels een acute sectio caesarea in verband met maternaal bloedverlies bij een placenta praevia totalis. Haar geboortegewicht was 2900 g. In de eerste uren na de geboorte spuugde zij frequent helder slijm op en het drinken lukte niet goed. Bij lichamelijk onderzoek werden geen afwijkingen gevonden en er werd een expectatief beleid gevoerd. Ook de 2edag postpartum lukte het drinken niet en leek ze sloom en weinig alert. Daarop volgde overplaatsing van de kraamafdeling naar de neonatale intensive care.
Hier werd een matig gedehydreerde neonaat gezien van 2710 g. Er kon zonder problemen een neus-maagsonde geplaatst worden waarmee zij gevoed werd. De voeding werd goed verdragen, waardoor een anatomische afwijking uitgesloten kon worden. Differentiaaldiagnostisch werd gedacht aan een infectie dan wel een endocriene of neurologische afwijking, maar verder aanvullend onderzoek was zonder afwijkingen. Voedingen konden worden opgehoogd en weer oraal worden aangeboden. Na 3 weken dronk patiënte alle voedingen zelf en kon zij in goede conditie naar huis worden ontslagen. De voedingsproblemen werden geduid als passend bij de randprematuriteit.
Bij patiënt C was er tijdens de zwangerschap op de 20-wekenecho een geïsoleerd polyhydramnion te zien, die gedurende de zwangerschap vervolgd werd met meerdere echografieën. Er werd geen verklaring gevonden voor het polyhydramnion. Bij een termijn van 41 0/7 weken werd een meisje geboren met een gewicht van 3150 g. De poliklinische bevalling vond plaats in een algemeen ziekenhuis. In het ziekenhuis sabbelde zij wel aan de borst, maar de melkproductie was nog niet op gang. Patiënte kwijlde groen slijm, dat werd geduid als vruchtwater.
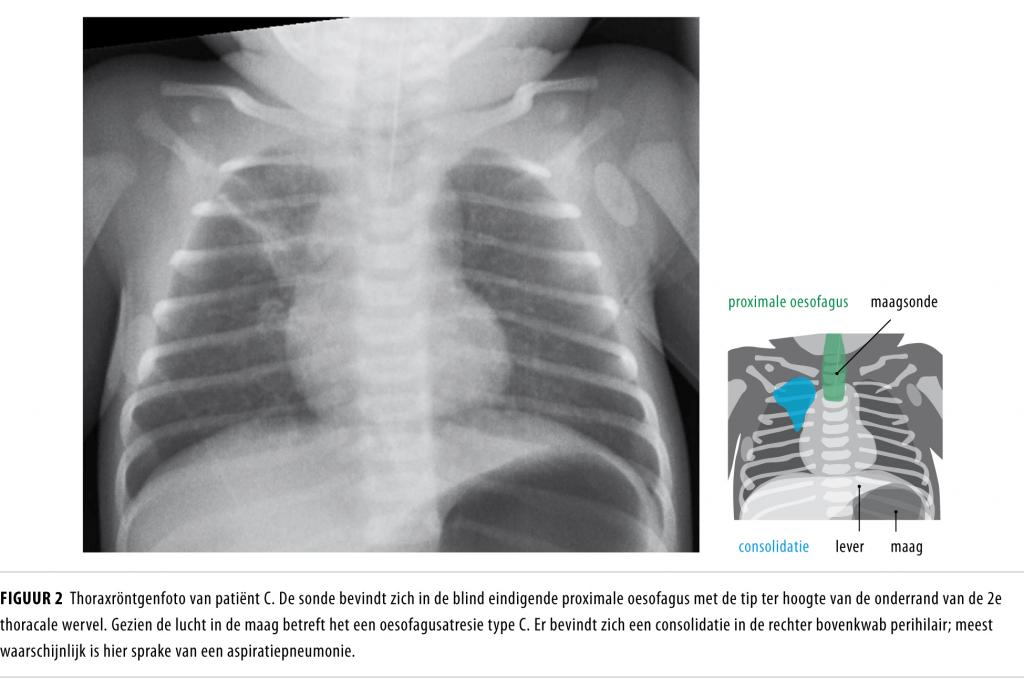
Zij werd ongeveer 7 hna de partus naar huis ontslagen. Thuis verslikte zij zich als ze probeerde te drinken en bleef ze groen vocht opgeven. De verloskundige stelde bij haar huisbezoek de ouders gerust. 30hpostpartum stopte patiënt met ademen; haar ogen draaiden weg en ze werd slap en blauw. Haar ouders pasten onder telefonische begeleiding van de alarmcentrale mond-op-mondbeademing en hartmassage toe. Op het moment dat de ambulance arriveerde ademde patiënt weer zelf. Ze werd met de ambulance vervoerd naar hetzelfde ziekenhuis waar ze was geboren en werd daar opgenomen. Bij opname werd gezien dat zij bellen blies en kwijlde. De neus-maagsonde was niet op te voeren. Op de thoraxfoto eindigde de maagsonde ter hoogte van de 2e thoracale wervel, werd er lucht in de maag gezien en was er verdenking op een aspiratiepneumonie (figuur 2). Op basis hiervan werd de diagnose ‘oesofagusatresie type C’ gesteld. Het opgeven van groen slijm, wat moet worden onderscheiden van gallig braken dat op een malrotatie kan duiden, werd verklaard door de wijde tracheo-oesofageale fistel, waardoor gal omhoog kwam en via de trachea opgehoest werd. Ze werd overgeplaatst naar ons centrum en onderging een operatie met onderbinden van de tracheo-oesofageale fistel en creëren van een oesofago-oesofagostomie via thoracotomie. Het postoperatieve beloop was ongecompliceerd. Bij poliklinische controle na 2 maanden was zij 4660 gen ging het goed met haar.
Beschouwing
Dat het vertraagd diagnosticeren van oesofagusatresie tot gevaarlijke situaties kan leiden, blijkt uit casus A en C. Voor patiënt A hebben ouders medische hulp gezocht door hun gedehydreerde kind op de 3e levensdag naar de Spoedeisende Hulp te brengen. De moeder van patiënt C heeft haar kind op de 2e dag na de geboorte moeten reanimeren. Patiënt B illustreert dat niet elke slecht drinkende zuigeling een oesofagusatresie heeft en dat deze diagnose verworpen kan worden als een sonde tot in de maag kan worden opgevoerd.
Hoewel het als belastend wordt ervaren om met een pasgeborene vanuit huis naar het ziekenhuis te gaan om een eventuele oesofagusatresie uit te sluiten, is het inbrengen van een neus-maagsonde en het maken van een röntgenfoto vervolgens weinig invasief en van grote diagnostische waarde. Het laat stellen van de diagnose ‘oesofagusatresie’ kan tot ernstige complicaties leiden. Daarom is ons advies om te proberen een neus-maagsonde in te brengen bij elke neonaat bij wie geen enkele voeding lukt.
Prevalentie en etiologie
De prevalentie van oesofagusatresie is ongeveer 1 per 4000 levendgeborenen.1 In Nederland komt dit neer op 45-50 kinderen per jaar. Gemiddeld zal 1 op de 2 verloskundigen tijdens zijn of haar carrière een kind met een oesofagusatresie tegenkomen. De afwijking ontstaat in de embryonale periode tussen het einde van de 3e en de 6e week door een verkeerde uitgroei in de voordarm van het septum dat de trachea en de oesofagus scheidt. De oorzaak is multifactorieel. Bij 45% van de kinderen met een oesofagusatresie is er sprake van een geïsoleerd geboortedefect, en bij 24% is de oesofagusatresie onderdeel van een sporadisch voorkomend syndroom.1
Classificatie en symptomen
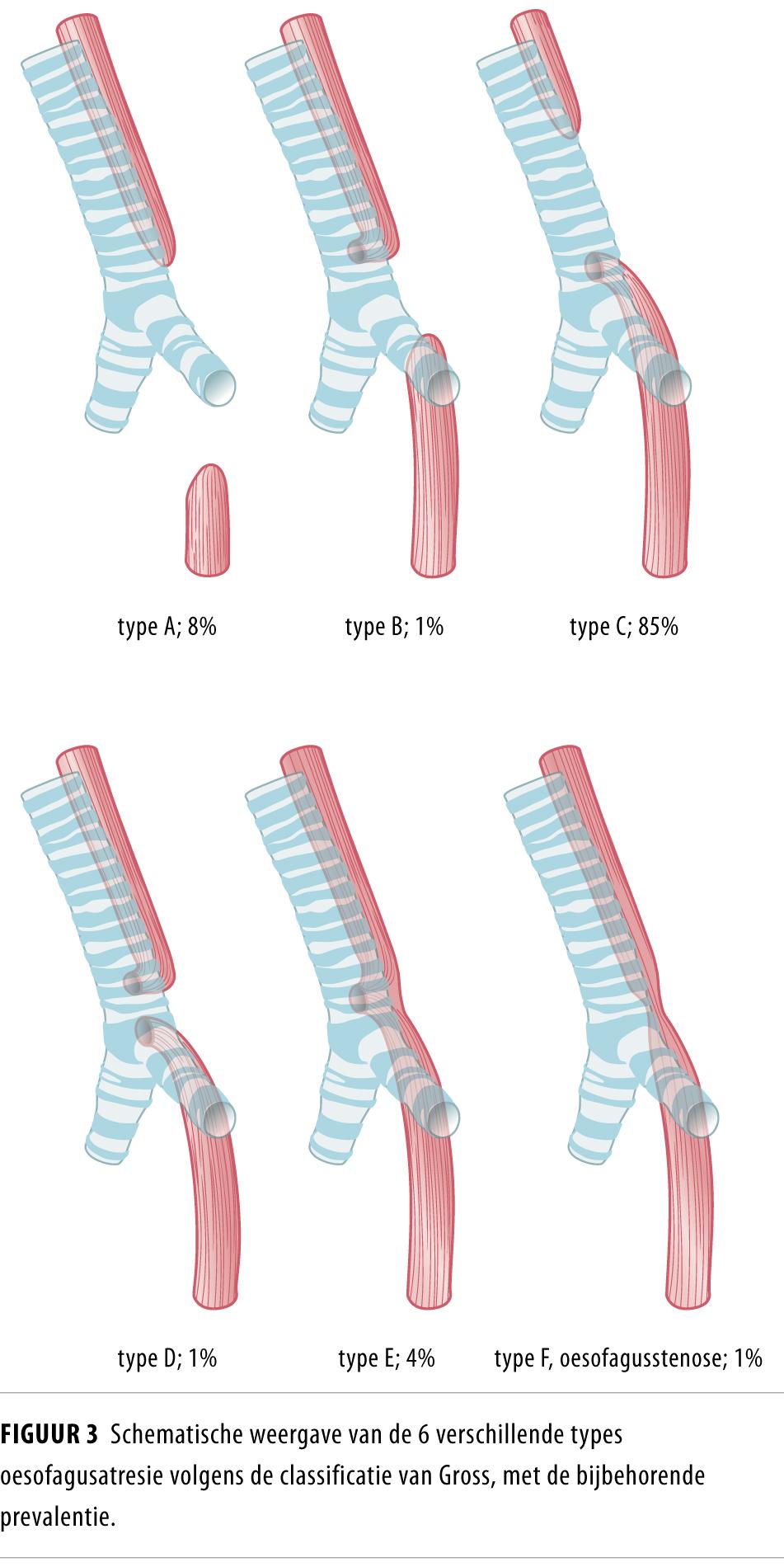
Volgens de classificatie van Gross zijn er 6 types oesofagusatresie.2,3Type C komt verreweg het meest voor, namelijk bij 85% van de patiënten. In figuur 3 staan de verschillende types schematisch weergegeven.
Antenataal zijn een polyhydramnion en weinig tot geen maagvulling redenen om aan een oesofagusatresie te denken. Deze symptomen zijn echter weinig sensitief en specifiek.4
Na de geboorte zal de patiënt, afhankelijk van het type oesofagusatresie, een ingevallen buik hebben, niets kunnen drinken, speekselvloed hebben, zich verslikken, hoesten of de kenmerkende bellen blazen.5 Complicaties als dehydratie, aspiratie of een aspiratiepneumonie en ‘apparent life-threatening events’ (ALTE’s) kunnen hiervan het gevolg zijn.
Vroege herkenning
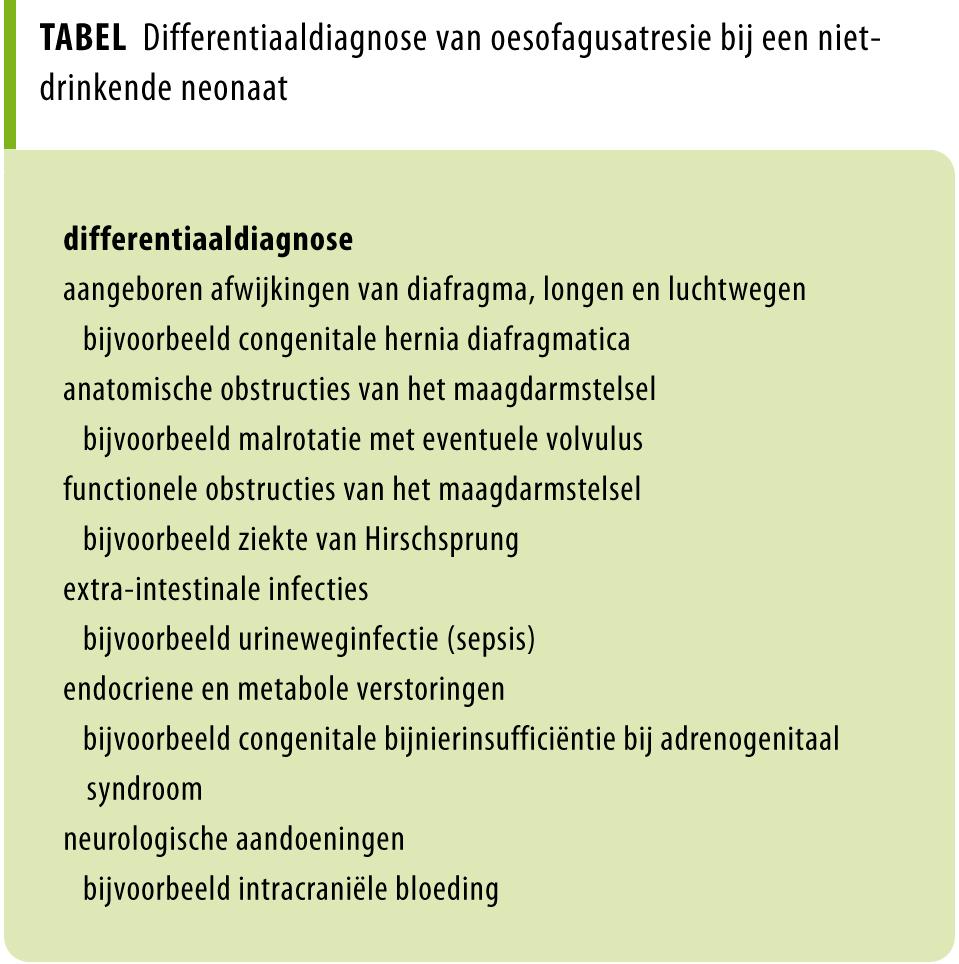
Voedingsproblemen bij pasgeborenen komen veel voor. Deze zijn meestal van voorbijgaande aard en niet bedreigend. De onschuldige vorm van voedingsproblemen wordt vaak gewijd aan misselijkheid door vruchtwateringestie of problemen met de adaptatie na de geboorte, al ontbreekt de wetenschappelijke onderbouwing hiervoor. De differentiaaldiagnose voor een niet-drinkende neonaat is echter uitgebreid en omvat – naast oesofagusatresie –meerdere spoedeisende aandoeningen (tabel).6
Wat onderscheidt nu een pasgeborene met een oesofagusatresie? Als gevolg van de blind eindigende proximale oesofagus wordt er in het geheel geen melk verdragen en hoopt het speeksel zich op. Veelal is hierbij sprake van het kenmerkende bellenblazen. Bovendien kan door de volgelopen proximale blindzak aspiratie optreden met ademhalingsproblemen tot gevolg.
Aanvullende diagnostiek
De diagnostiek bij een oesofagusatresie is relatief eenvoudig. Wanneer een stevige maagsonde wordt ingebracht, stokt deze op circa 11-12 cm van de neus.5 Een dunnere maagsonde kan op die plaats opkrullen. Wanneer dan op de thoraxfoto wordt gezien dat de neus-maagsonde hoog-thoracaal (meestal op het niveau van de 2e of 3e thoracale wervel) eindigt of opkrult, is de diagnose bevestigd. Op de buikoverzichtsfoto kan, afhankelijk van het type, het maag-darmkanaal vrij van lucht zijn (type A en B) of gevuld met lucht (type C, D, E). Een contrastonderzoek is obsoleet in verband met het risico op aspiratie.4
Dames en Heren, de hier beschreven patiënten laten zien hoe het vertraagd stellen van de diagnose ‘oesofagusatresie’ kan verlopen en welke consequenties dit kan hebben. Het onderscheiden van kinderen met een oesofagusatresie en kinderen met voedingsproblemen door andere oorzaken dient zo vroeg mogelijk te gebeuren. Dit kan door te proberen of het mogelijk is een neus-maagsonde in te brengen. Ons inziens is het inbrengen van een maagsonde dan ook geïndiceerd bij elke neonaat met ernstige voedingsproblemen vanaf de geboorte.
Leerpunten
Voedingsproblemen bij pasgeborenen komen veel voor; meestal zijn ze niet bedreigend en van voorbijgaande aard.
In Nederland worden 45-50 kinderen per jaar geboren met een oesofagusatresie.
Wanneer de pasgeborene niets kan wegslikken en als gevolg daarvan bellen blaast,is het belangrijk te denken aan een oesofagusatresie.
Oesofagusatresie kan worden onderscheiden van andere voedingsproblemen door het inbrengen van een neus-maagsonde en het vervolgens maken van een thoraxfoto: bij oesofagusatresie eindigt de maagsonde hoog thoracaal of hij krult op.
Bij iedere pasgeborene die bovengenoemde symptomen vertoont, moet een neus-maagsonde worden ingebracht en een thoraxfoto worden gemaakt.
Literatuur
Pedersen RN, Calzolari E, Husby S, Garne E. Oesophageal atresia: prevalence, prenatal diagnosis and associated anomalies in 23 European regions. Arch Dis Child. 2012;97:227-32 Medline. doi:10.1136/archdischild-2011-300597
Gross RE. The surgery of infancy and childhood. Philadelphia, WB Saunders; 1953
Clark DC. Esophageal Atresia and Tracheoesophageal Fistula. Am Fam Physician. 1999;59:910-6 Medline.
Spitz L. Oesophageal atresia. Orphanet J Rare Dis. 2007;2:24 Medline. doi:10.1186/1750-1172-2-24
Pinheiro PF, Simões e Silva AC, Pereira RM. Current knowledge on esophageal atresia. World J Gastroenterol. 2012;18:3662-72 Medline. doi:10.3748/wjg.v18.i28.3662
Van Hoek E, van Mierlo T. Verdraaid, een spugende zuigeling. Praktische Pediatrie. 2009;2:134-48.link





Reacties