artikel
Vanuit de maatschappij, overheid en zorgverzekeraars klinkt in toenemende mate de roep om normering en standaardisatie van het geneeskundig handelen. Hierdoor ‘verprotocolleert’ de zorg en neemt keuzevrijheid van zorgverleners af.
Het overheersende normeringinstrument voor regulatie en standaardisatie is epidemiologisch bewijs, oftewel ‘evidence’. Evidence bestaat uit empirische gegevens verkregen in groepen personen, bijvoorbeeld in cohortstudies of gerandomiseerde klinische trials. Veelal wordt ‘evidence-based medicine’ (EBM) uitgelegd als geneeskundig handelen waarbij besluitvorming bij een individuele patiënt is gebaseerd op het zo direct mogelijk vertalen van epidemiologisch bewijs. De epidemioloog Sackett, die aan de wieg stond van de EBM-beweging, hanteert echter een bredere omschrijving: ‘integratie van individuele klinische expertise met het best beschikbare bewijs uit epidemiologisch onderzoek’.1 Deze definitie van Sackett doet meer recht aan de praktijk. Rechtlijnige vertaling van epidemiologisch bewijs naar de klinische praktijk is vaak onmogelijk, en waar wel mogelijk doorgaans riskant.
In dit artikel beargumenteren wij dat epidemiologisch bewijs als normeringsinstrument voor individuele zorg ernstige beperkingen heeft. Tevens bespreken wij hoe epidemiologisch bewijs de zorg beter ten goede kan komen.
Bewijs
Onze bezwaren tegen het heilig verklaren van epidemiologisch bewijs bij individuele zorgverlening berust op enkele peilers: we weten nog een heleboel niet en het bewijs is niet altijd betrouwbaar en toepasbaar.
Hoeveel weten we?
Sommigen veronderstellen dat het merendeel van ons geneeskundig handelen is gebaseerd op evidence. Het tegendeel is waar, zoals de figuur laat zien. Dit geldt ook voor deeldomeinen. Bij hart- en vaatziekten bijvoorbeeld bestaat een sterke traditie van epidemiologisch onderzoek. Een analyse van Amerikaanse richtlijnen wees echter uit dat van alle aanbevelingen slechts 11% was gebaseerd op krachtig epidemiologisch bewijs. De helft werd zelfs nauwelijks door epidemiologisch onderzoek ondersteund.2 Deze analyse doet vermoeden dat epidemiologisch bewijs schaars is in andere domeinen van de geneeskunde met een minder sterke onderzoekstraditie.
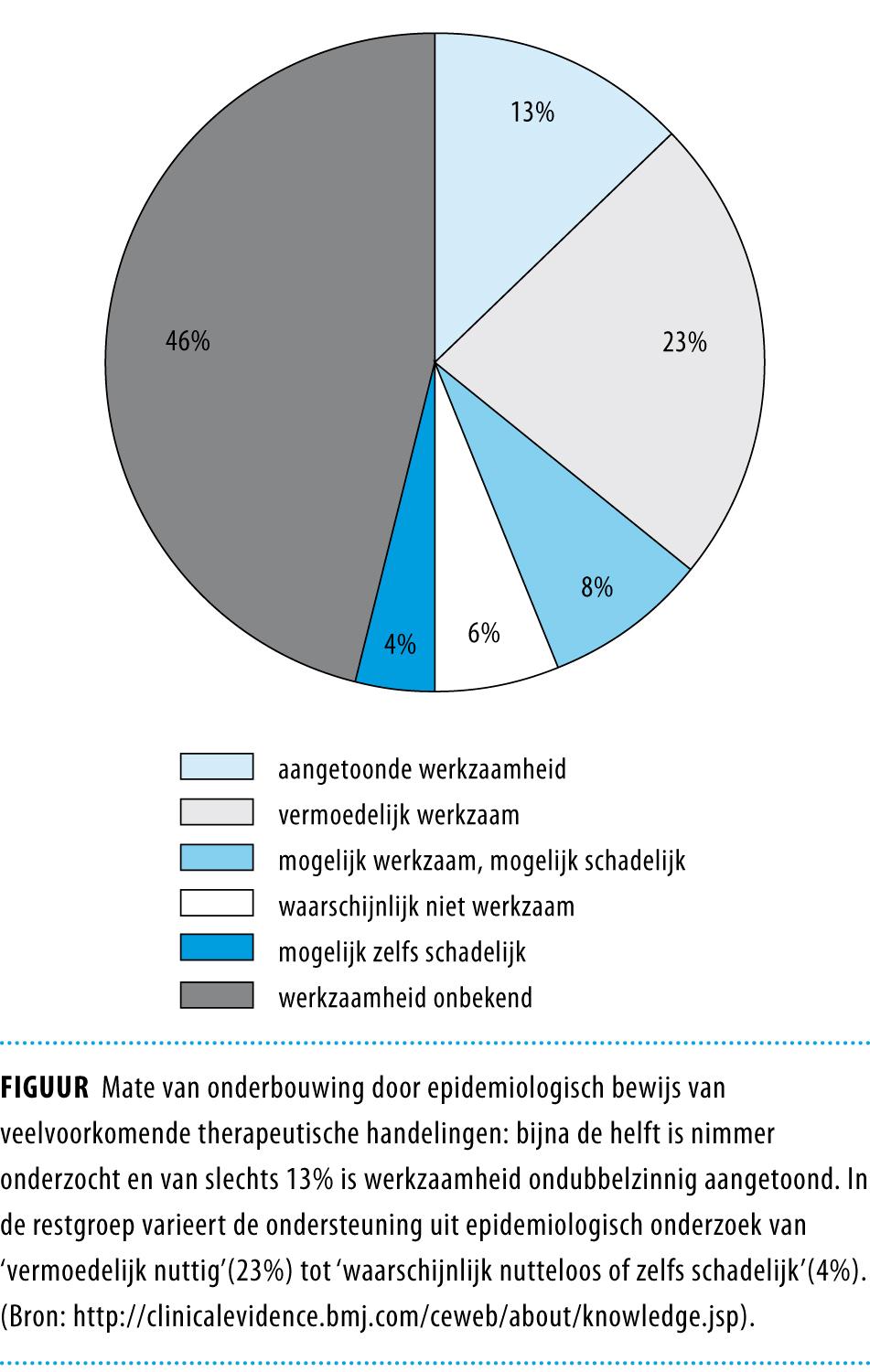
Deze bewijsschaarste heeft vele achtergronden, waaronder commerciële belangen en de lage prevalentie van veel ziektebeelden. Een verdere selectie ontstaat doordat epidemiologisch onderzoek zich meestal richt op therapeutisch handelen, waarbij schier eindeloze vergelijkingen met placebo noodzakelijke directe vergelijking van interventies vertroebelen.3 De aandacht voor farmacologische interventies verdringt ook onderzoek naar andere aspecten van therapeutisch handelen, zoals therapietrouw. Zo is er veel onderzoek naar het beste antihypertensivum, maar de kleine verschillen in effectiviteit vallen in het niet wanneer men beseft dat in de praktijk na 2 jaar ongeveer de helft van de patiënten is gestopt met het gebruik van ervan.4
Tenslotte is onderzoek naar diagnostiek schaars, wat temeer zorgelijk is omdat fouten in dit domein verantwoordelijk zijn voor meer gezondheidschade dan fouten in therapeutische besluitvorming.5
De betrouwbaarheid van epidemiologisch bewijs
‘Al weten we dan niet zo veel, wat wel onderzocht is, weten we tenminste zeker.’ Of klopt die veronderstelling ook niet? Er zijn allerlei problemen met de veronderstelling dat we ons op uitkomsten van onderzoek kunnen verlaten, waaronder beperkingen van het onderzoek zelf, publicatiebias en − misschien wel het belangrijkste − plausibiliteit van de onderzoekshypothese.
Beperkingen van het onderzoek Epidemiologisch vergelijkend onderzoek met een statistisch significant resultaat wordt doorgaans als ‘waar’ beschouwd. De uitkomst heeft echter betrekking op de data zélf, niet op de wijze waarop data tot stand zijn gekomen. Hierbij kan namelijk vertekening (‘bias’) zijn opgetreden, die men niet terugziet in de uitkomst, noch in het significantieniveau. Het hele onderzoekstraject is kwetsbaar voor bias, vanaf de formulering van de onderzoeksvraag, selectie van deelnemers en selecties in onderzoeksmethodiek, uitkomstmaat, statistische analysemethoden tot rapportage van uitkomsten.
Selectie door externen Vertekening van de ‘epidemiologische waarheid’ treedt ook op door publicatiebias: selectie tijdens peer review en publicatie in tijdschriften, veroorzaakt door een voorkeur van referenten en redacties voor prestigieuze auteurs6,7 en voor ‘positieve’onderzoeksresultaten.8
Plausibiliteit Een zelden onderkende factor in het ‘waarheidsgehalte’ van epidemiologisch onderzoek betreft plausibiliteit van de onderzoekshypothese. Indien men 2 gelijkwaardige onderzoeken vergelijkt, waarvan de ene een plausibele en de andere een niet-plausibele hypothese bevestigt, dan heeft het eerstgenoemde onderzoek toch een veel grotere kans om waar (hier te lezen als: reproduceerbaar) te zijn. Om dit te begrijpen denke men aan de analogie met de regel van Bayes in de context van diagnostiek.9 De juistheid van een diagnose hangt volgens deze regel niet alleen af van de uitslag van een diagnostische test, maar ook van de voorafkans op deze diagnose. Datzelfde geldt bij epidemiologisch onderzoek. De kans dat een onderzoeksuitkomst juist is, wordt mede bepaald door de vraag of die uitkomst aannemelijk is, onafhankelijk van het significantieniveau van de uitkomst.10 Voor het bepalen van aannemelijkheid kan men zich baseren op het aanwezige kennisfundament uit eerder onderzoek, op kennis van de fysiologie en pathofysiologie, en op klinische expertise. Het moge duidelijk zijn dat het lastig is over aannemelijkheid van hypotheses consensus te bereiken, waarmee een voedingsbodem is gelegd voor onvermijdelijke – en misschien ook wel gewenste – wisselende interpretatie van gelijke onderzoeksuitkomsten.
Waarheidsgehalte van bewijs
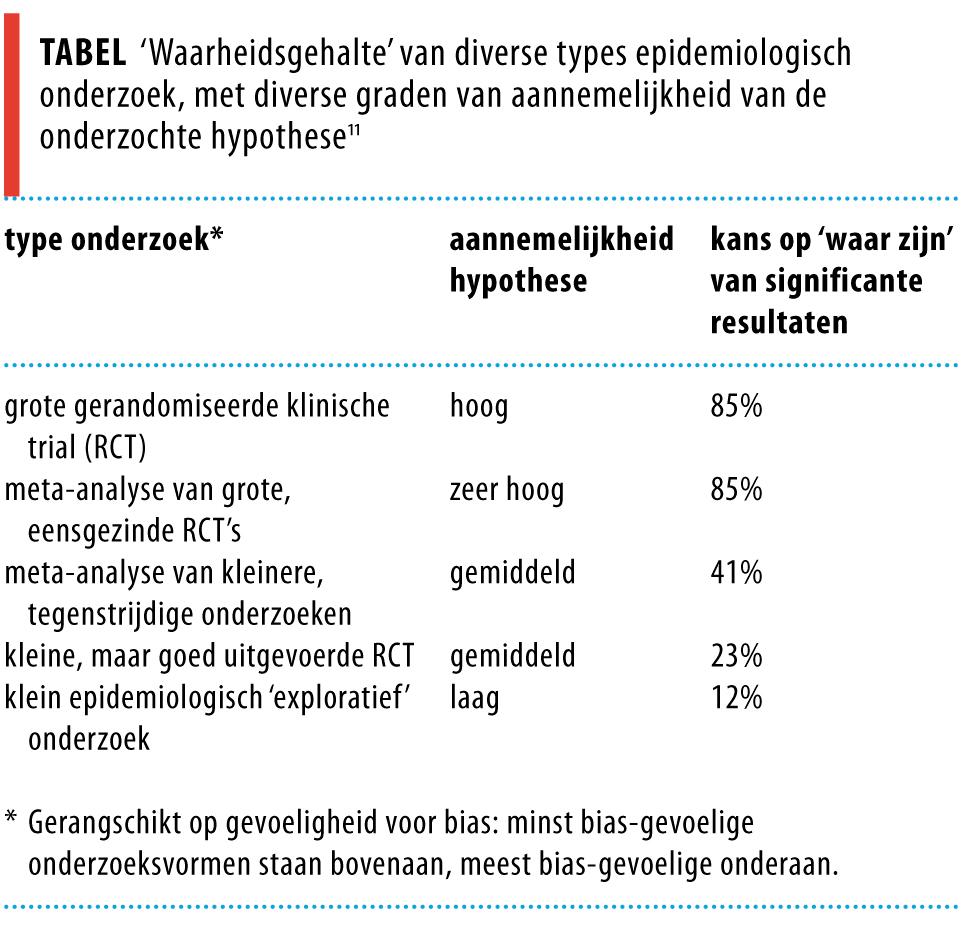
Om het ‘waarheidsgehalte’ van uitkomsten van epidemiologisch onderzoek te kennen, moeten we dus niet alleen kijken naar statistische significatie, maar vooral naar bias en plausibiliteit van de uitkomst. De epidemioloog Ioannidis heeft op basis van deze ingrediënten het gemiddelde ‘waarheidsgehalte’ van diverse types epidemiologisch onderzoek berekend.11 Het ontluisterende resultaat is samengevat in de tabel. Zelfs de vlaggenschepen van de epidemiologie, de grote klinische trials en de meta-analyses daarvan, met vaak onmetelijk hoge significantieniveaus, halen gemiddeld een ‘waarheidsgraad’ van slechts 85%. Op dit werk is kritiek gekomen, met name dat de auteur de toegevoegde waarde van replicatie van onderzoeksbevindingen onderschat.12 Het criterium van replicatie is echter, meer dan welk ‘waarheidscriterium’ dan ook, kwetsbaar voor rapportage- en publicatiebias.13 De kern van het betoog blijft overeind: het significantieniveau zegt lang niet alles over het waarheidsgehalte van de onderzoeksuitkomst.
Epidemiologisch bewijs: toepasbaarheid in de spreekkamer
Betrouwbare evidence blijkt dus een relatief schaars goed. Resteert de vraag of men, indien het epidemiologisch bewijs voorhanden is én men dit als waar zou aannemen, dit bewijs naar een individuele patiënt kan vertalen.
Een antwoord zou zijn dat het bewijs geldig is voor een patiënt met een klinisch profiel dat overeenkomt met dat van de gemiddelde deelnemer aan de trial die het bewijs aanleverde. Al lijkt dit redelijk, men realisere zich dat intensieve selectie aan de inclusie in klinische trials voorafgaat. Het merendeel (60-99,9%) van patiënten met een bepaalde aandoening komt niet in aanmerking voor deelname aan onderzoek.14 Dit zou niet erg zijn als de redenen voor exclusie geen invloed zouden hebben op de toepasbaarheid van de onderzoeksuitkomst, maar helaas is niets minder waar. Een recente analyse wees uit dat exclusiecriteria van trials veelal omstandigheden betreffen die cruciaal zijn voor extrapolatie van de onderzoeksbevindingen naar de praktijk.15 Hierdoor zijn clinici aangewezen op onzekere extrapolatie van zowel effectiviteit als bijwerkingenprofielen.
Het risico van laatstgenoemde extrapolaties wordt bijvoorbeeld geïllustreerd door een analyse naar bloedingscomplicaties van vitamine K-antagonisten. De incidentie daarvan nam exponentieel toe met het aantal exclusiecriteria van relevante trials die achteraf op een patiënt van toepassing waren.16 Een ander voorbeeld is de impact van een studie naar spironolacton bij hartfalen.17 De aangetoonde effectiviteit werd door artsen vertaald naar hun eigen patiëntenpopulatie, waarbij men zich onvoldoende rekenschap gaf van de verschillen tussen de trialpatiënten en de echte patiënten. Een forse toename van ernstige en soms fatale hyperkaliëmie was het gevolg.18
Extrapolatie van epidemiologisch bewijs naar de individuele patiënt is dus vaak problematisch. Zelfs indien de patiënt voldoet aan de inclusiecriteria van relevante trials, dan nog is het bewijs dat u juist handelt vele malen zwakker dan het bewijs dat die handeling in algemene zin de voorkeur heeft. Hier geldt dat kennis en waardering van bijzondere individuele omstandigheden, eerdere ervaringen met soortgelijke patiënten of met dezelfde individuele patiënt en de lastig te vangen component van klinische expertise de doorslag kunnen geven om van een op groepsniveau bewezen onderzocht beleid af te wijken.
Implicaties
De besproken beperkingen in de beschikbaarheid, betrouwbaarheid en individuele toepasbaarheid van epidemiologisch bewijs hebben belangrijke implicaties voor diverse domeinen van de gezondheidzorg, waarvan wij er enkele noemen.
Klinische patiëntenzorg In een tijdperk waarin evidence tot enige norm voor goede geneeskunde dreigt te worden verheven, is het belangrijk dat artsen zich bewust zijn van de beperkingen van epidemiologisch bewijs. Dit zou tenminste weerklank moeten vinden in de zorg voor individuele patiënten. Maar ook in de dialoog tussen zorgverleners is het belangrijk dat de relativiteit van epidemiologisch bewijs geëxpliciteerd wordt. De veelgehoorde opmerking ‘daar is geen bewijs voor’ is in de meeste gevallen misplaatst of zelfs ongepast, zeker als ermee wordt gesuggereerd dat van handelingen waar geen evidence voor is, zou moeten worden afgezien. Dit zou het overgrote merendeel van ons medisch handelen onmogelijk maken.
Ook in richtlijnen zijn de beperkingen van epidemiologisch bewijs belangrijk. Doorgaans is de disclaimer (‘u kunt in individuele gevallen afwijken van de aanbevelingen’ of woorden van gelijke strekking) hiervoor bedoeld. Zaak is dan wel dat de disclaimer serieus wordt genomen, zowel door richtlijngebruikers als door bijvoorbeeld overheid en verzekeraars.
Overheden en verzekeraars Met kracht dient te worden bestreden dat overheden en verzekeraars epidemiologisch bewijs gebruiken om de individuele aanspraak op zorg te reguleren. Bij strikte naleving zou dit het merendeel van het geneeskundig handelen niet-vergoedbaar maken. Hoewel dit uiteraard onrealistisch is, illustreert het dat de selectie van toegestane handelingen op basis van beschikbaarheid van evidence in essentie opportunistisch is, waarbij economische motieven een belangrijke rol zullen spelen.
Het alternatief
We willen epidemiologisch onderzoek of EBM niet in een negatief daglicht stellen. Evidence werkt kwaliteitsverhogend als norm voor ‘gemiddeld’ beleid voor een ‘gemiddelde’ patiënt. We moeten echter vermijden dat evidence als norm voor individueel beleid gaat gelden of dat de afwezigheid ervan een legitimatie wordt om van handelen af te zien.
Balans De moeilijkste vraag is welke mate van keuzevrijheid deze kijk op de geneeskunde toelaat. Louter vertrouwen op pathofysiologisch redeneren heeft in het verleden tot grote fouten geleid, die nota bene door epidemiologisch onderzoek aan het licht zijn gebracht. Klinische expertise is bovendien alles behalve waterdicht. Er dient dus altijd een balans te zijn tussen epidemiologisch bewijs en actuele context. Voor het vinden van deze balans bestaan geen spelregels, maar er is geen principiële reden waarom het niet zou kúnnen. Het toepassen van klinische expertise berust immers op, vaak verborgen, opvattingen over causaliteit.19 De validiteit daarvan hangt af van de vraag hoe goed geprobeerd is deze te weerleggen: een opvatting over causaliteit wordt plausibeler naarmate deze meer intelligente pogingen tot weerlegging heeft overleefd.
Groepsniveau Voor epidemiologisch bewijs als normeringsinstrument zou het uitgangspunt kunnen zijn dat men dit instrument hanteert voor beleid op een hoger integratieniveau dat dan van een individuele patiënt, bijvoorbeeld het niveau van een arts, groepspraktijk of ziekenhuisafdeling.20 Omdat epidemiologisch bewijs zich uitspreekt over een ‘gemiddelde patiënt’, en dus in feite over een groep patiënten, ligt het niet voor de hand het beleid per individuele patiënt op grond hiervan af te rekenen. Met andere woorden: het integratieniveau waarop zorg de maat wordt genomen, zou in overeenstemming moeten zijn met het niveau waarop epidemiologisch bewijs wordt geleverd: groepsniveau.
Zou een groot percentage van patiënten een praktijk verlaten met een beleid dat niet conform de beschikbare evidence of de algemene aanbeveling is, dan heeft de arts iets uit te leggen. Deze wijze van zorgregulatie op basis van evidence is niet alleen rechtvaardiger voor individuele patiënten, zij is ook eenvoudiger te handhaven. Mits van een aantal waarborgen voorzien, zou op deze wijze epidemiologisch bewijs toch normerend kunnen werken, waarbij onuitlegbare praktijkvariatie bestreden kan worden, zonder dat het de keuzevrijheid bij individuele patiënten te sterk reduceert. De belangrijkste voorwaarde is beschikbaarheid van adequate meetinstrumenten en criteria om te beoordelen óf, en zo ja in welke mate, een specifieke patiëntenpopulatie afwijkt van een ‘gemiddelde populatie’ en hoe deze afwijking een ander gemiddeld geneeskundig handelen rechtvaardigt. Hierbij valt voor de eerste lijn te denken aan verschillen in socio-economische achtergrond en etniciteit van patiëntenpopulaties. In de tweede lijn kunnen verwijspatronen van aanvullend belang zijn. Tertiaire zorginstellingen, die bijvoorbeeld complexe ziektegevallen behandelen, kan moeilijker met normen voor gemiddeld beleid, die uit (in algemene populaties uitgevoerd) epidemiologisch onderzoek verkregen zijn, de maat worden genomen.
Conclusie
Evidence-based medicine dreigt – door een verkeerde interpretatie van het begrip – foutief toegepast te worden om geneeskundig handelen bij een individuele patiënt te formuleren, te normeren en te toetsen. Daarvoor komt gemiddeld geleverde zorg meer in aanmerking, mits aan enkele voorwaarden wordt voldaan.
Literatuur
-
Sackett DL, Rosenberg WMC, Gray JAM, Haynes RB, Richardson WS. Evidence based medicine: what it is and what it isn’t. BMJ. 1996;312:71-72 Medline.
-
Tricoci P, Allen JM, Kramer JM, Califf RM, Smith SC Jr. Scientific Evidence Underlying the ACC/AHA Clinical Practice Guidelines. JAMA. 2009;301:831-41 Medline. doi:10.1001/jama.2009.205
-
Sox HC, Greenfield S. Comparative Effectiveness Research: A Report From the Institute of Medicine. Ann Intenal Med. 2009;151:203-5.
-
Van Wijk BL, Klungel OH, Heerdink ER, de Boer A. Rate and determinants of 10-year persistence with antihypertensive drugs. J Hypertens. 2005;23:2101-7 Medline. doi:10.1097/01.hjh.0000187261.40190.2e
-
Newman-Toker DE, Pronovost PJ. Diagnostic Errors--The Next Frontier for Patient Safety. JAMA. 2009;301:1060-2 Medline. doi:10.1001/jama.2009.249
-
Garfunkel JM, Ulshen MH, Hamrick HJ, Lawson EE. Effect of institutional prestige on reviewers’ recommendations and editorial decisions. JAMA. 1994;272:137-8 Medline. doi:10.1001/jama.272.2.137
-
Link AM. US and Non-US Submissions: An Analysis of Reviewer Bias. JAMA. 1998;280:246-7 Medline. doi:10.1001/jama.280.3.246
-
Song F, Parekh-Bhurke S, Hooper L, et al. Extent of publication bias in different categories of research cohorts: a meta-analysis of empirical studies. BMC Med Res Methodol. 2009;9:79 Medline. doi:10.1186/1471-2288-9-79
-
Vermeulen M. Dwalingen in de methodologie. XXXVI. Van ‘likelihood’-ratio’s en de regel van Bayes. Ned Tijdschr Geneeskd. 2001;145:2421-4 Medline.
-
Rawlins M. De testimonio: on the evidence for decisions about the use of therapeutic interventions. Lancet. 2008;372:2152-61 Medline. doi:10.1016/S0140-6736(08)61930-3
-
Ioannidis JP. Why most published research findings are false. PLoS Med. 2005;2:e124 Medline. doi:10.1371/journal.pmed.0020124
-
Moonesinghe R, Khoury MJ, Janssens AC. Most published research findings are false-but a little replication goes a long way. PLoS Med. 2007;4:e28 Medline. doi:10.1371/journal.pmed.0040028
-
Greenberg SA. How citation distortions create unfounded authority: analysis of a citation network. BMJ. 2009;339:b2680 Medline. doi:10.1136/bmj.b2680
-
Rothwell PM. External validity of randomised controlled trials: “To whom do the results of this trial apply? Lancet. 2005;365:82-93 Medline. doi:10.1016/S0140-6736(04)17670-8
-
Van Spall HGC, Toren A, Kiss A, Fowler RA. Eligibility Criteria of Randomized Controlled Trials Published in High-Impact General Medical Journals: A Systematic Sampling Review. JAMA. 2007;297:1233-40 Medline. doi:10.1001/jama.297.11.1233
-
Levi M, Hovingh GK, Cannegieter SC, Vermeulen M, Buller HR, Rosendaal FR. Bleeding in patients receiving vitamin K antagonists who would have been excluded from trials on which the indication for anticoagulation was based. Blood. 2008;111:4471-6 Medline. doi:10.1182/blood-2007-11-123711
-
Pitt B, Zannad F, Remme WJ, et al. The Effect of Spironolactone on Morbidity and Mortality in Patients with Severe Heart Failure. N Engl J Med. 1999;341:709-17 Medline. doi:10.1056/NEJM199909023411001
-
Juurlink DN, Mamdani MM, Lee DS, et al. Rates of Hyperkalemia after Publication of the Randomized Aldactone Evaluation Study. N Engl J Med. 2004;351:543-51 Medline. doi:10.1056/NEJMoa040135
-
Stehouwer CDA. De oorzaak ontmaskerd? Oratie. VU Boekhandel, 2001.
-
Smulders YM. Vrijheid om af te wijken. Med Contact 2008;43:1763-6.





EBM en medisch handelen
In het artikel van Smulders et al. (2010;154:892-895), staat een figuur, waaruit zou moeten blijken dat van 46% van veelvoorkomende therapeutische handelingen de werkzaamheid onbekend is. De oorsprong van de gegevens waarop deze taartgrafiek gebaseerd is, blijft enigszins onduidelijk, doordat deze op de website waarnaar verwezen wordt, niet meer te vinden is. De auteurs hebben hun copie van de figuur waarschijnlijk overgenomen uit de rubriek Ingezonden Brieven in de British Medical Journal over het onderwerp ´What to do about CAM?´(1). Blijkens het onderschrift bij hun figuur interpreteren Smulders et al. de term ´onbekend (unknown)´ als: ´nimmer onderzocht´. Helaas bestendigen zij daarmee een al lang bestaand misverstand over ´evidence based medicine´ (EBM). De vernietigende reactie op deze publicatie is hun blijkbaar ontgaan.
John Garrow, vice-voorzitter van Health Watch, noemde de interpretatie van de grafiek door George Lewith, docent in alternatieve behandelwijzen aan de Universiteit van Southampton, misleidend (1). De term onbekend bleek hier niet te betekenen: ´we weten het niet, want het is niet onderzocht in gerandomiseerd gecontroleerd onderzoek (RCT)´, maar: ´ondanks degelijk onderzoek in RCT is de effectiviteit van deze 46% nooit aangetoond!´ Ofwel, ze zijn dus zeer waarschijnlijk onwerkzaam. Bij veel van de onderzochte behandelingen in deze categorie bleek het trouwens om alternatieve behandelwijzen te gaan!
De misverstanden over de rol van EBM bij het medisch handelen hebben een lange voorgeschiedenis. In 1978 verscheen een rapport van het Amerikaanse Office of Technology Assessment (OTA), waarin stond dat van slechts 10 tot 20 procent van het medisch-praktisch handelen de werkzaamheid was aangetoond in gecontroleerd wetenschappelijk onderzoek. Deze mythe werd pas 20 jaar later ontkracht toen bleek dat dit percentage volledig gebaseerd was op een verslag (uit 1963!) van het voorschrijfgedrag van 19 huisartsen van wie gedurende 2 weken de recepten waren bekeken (2).
De vraag rijst hoe lang nu weer dit getal van 46% gaat rondzingen. Smulders et al. noemen wel de epidemioloog, David Sackett in hun artikel, maar verwijzen niet naar het richtinggevende onderzoek uit zijn groep dat uitkwam op een percentage van 82% (3). Ook miste ik een verwijzing naar het werk van de klinisch-epidemioloog Jan Vandenbroucke die veel leerzame artikelen over EBM en medisch handelen heeft gepubliceerd.
Prof. dr. Rob A.P. Koene, em. hoogleraar nierziekten UMC St Radboud
1. Garrow JS. How much of orthodox medicine is evidence based? BMJ 2007;335:951
2. Forsyth G. An enquiry into the drug bill. Medical Care1963;1:10-16
3. Ellis J, Mulligan I, Rowe J, Sackett DL. Inpatient general medicine is evidence based. The Lancet 1995;346:407-410
Epidemiologisch bewijs
De figuur is nog gewoon toegankelijk op de website. Op dezelfde site is ook enige informatie te vinden over hoe men aan de gegevens komt (http://clinicalevidence.bmj.com/ceweb/about/search_process.jsp). Toegegeven, het is niet peer-reviewed en het kan allemaal beter, maar vrijwel niemand heeft zich verder serieus beziggehouden met de vraag hoeveel van ons handelen door epidemiologisch bewijs ondersteund wordt. Hoe Garrow aan zijn informatie komt is overigens eveneens onduidelijk.
Inderdaad had 'unknown effectiveness' beter niet als 'nimmer onderzocht' kunnen worden vertaald. Elders, in de legenda, staat de correcte vertaling.
Het artikel in The Lancet van 1995 is niet strijdig met onze boodschap. Ten eerste werden hier vrijwel alleen medicamenteuze interventies onderzocht, en wel voor nauw omschreven diagnosen. Het artikel komt bij deze categorie therapeutische handelingen, waarvoor natuurlijk relatief het meeste epidemiologisch bewijs voorhanden is, tot 53% epidemiologisch vastgestelde effectiviteit in 1 of meerdere RCT's. In het hele domein van therapeutisch handelen, zeker het niet-medicamenteuze domein, zal het % lager liggen.
Men kwam tot de genoemde 82% door bij de 53% gemakshalve 32% op te tellen, afkomstig van behandelingen waarvan men de 'face validity' erg hoog vond. En dat alles bij in totaal slechts 109 therapeutische beslissingen...
Men kan over het % handelingen dat door epidemiologisch bewijs gesteund wordt lang steggelen, maar realiseer dat het slechts een deel is van ons betoog. Ook al zou 50% van al ons therapeutisch handelen door epidemiologische bewijs ondersteund worden (wat ik niet geloof, en wat nog immer niets zou zeggen over de rol van epidemiologisch bewijs in diagnostiek), dan nog gelden er vele andere beperkingen bij het vertalen van dit bewijs naar individuele patiënten.
Yvo Smulders
Practise Based Evidence
In hun artikel beargumenteren de auteurs, dat epidemiologisch bewijs als normeringsinstrument voor individuele zorg ernstige beperkingen heeft. Voor hun bezwaren tegen het heilig verklaren van epidemiologisch bewijs bij individuele zorg, hebben zij meerdere argumenten:
-Bewijsschaarste: Mate van onderbouwing door epidemiologisch bewijs van veel voorkomende therapeutische handelingen: 46% is nooit onderzocht Van slechts 13% is de werkzaamheid ondubbelzinnig aangetoond
-Betrouwbaarheid: Bij grote RCT’s is de kans op “waar zijn” van significante resultaten 85%, evenals bij meta-analyses van RCT’s.
Bij kleinere onderzoeken duikt de kans op “waar zijn” flink onder de 50%.
-Extrapolatie van evidence naar de patient in de praktijk:
Het merendeel (60-99,9%) van patiënten met een bepaalde aandoening komt niet in aanmerking voor deelname aan onderzoek. Hierdoor zijn wij aangewezen op onzekere extrapolatie van zowel effectiviteit als bijwerkingenprofielen.
Wanneer we met deze getallen gaan rekenen, zullen we de conclusie moeten trekken dat de beschikbare evidence en daarmee de daarop beruste richtlijnen, slechts zelden zomaar kunnen worden geëxtrapoleerd naar de individuele patient.
De aanbeveling van de auteurs is dan ook schokkend inadequaat. Ondanks dat in het artikel de beperkingen van EBP genadeloos worden blootgelegd, blijven de auteurs in hetzelfde denkkader hangen met de aanbeveling dat artsen worden afgerekend op het percentage patiënten dat de praktijk verlaat met een beleid dat niet conform de beschikbare evidence of de algemene aanbeveling is. Een dergelijk percentage zou volgens redelijke berekeningen over het algemeen ver beneden de 10 moeten liggen!
Als huisarts behandel ik enkel individuele patiënten. Ik ben er beducht voor, dat ik aan het eind van het jaar moet kiezen tussen het behandelen van mijn patient naar beste kunnen, of het behalen van mijn statistisch behandelquotum. Vergelijk deze situatie met de eis in de VS, dat kinderartsen in opleiding op statistische gronden minstens 5 gevallen van kindermishandeling per jaar moeten melden.
We weten allemaal hoe het is afgelopen met de statisticus die door een rivier waadde met een gemiddelde diepte van 1 meter….
En dan heb ik het nog niet eens over de administratieve belasting die deze aanbeveling op zou leveren!
De conclusie die we uit dit artikel moeten trekken is veel verstrekkender. Wetenschappelijk onderzoek is de fundering waarop onze reguliere handelswijze is gebaseerd! Nu blijkt dat onze fundering niet stevig genoeg is om ons te dragen, is het zaak te gaan uitzoeken hoe wij deze kunnen versterken.
Ik zou ervoor willen pleiten dat er meer onderzoek gedaan wordt vanuit de praktijk. In plaats van vergroten van de administratieve belasting om te controleren of we de huidig beschikbare evidence wel in voldoende mate toepassen, zouden we vaker kunnen controleren of de behandeling die wij een patient hebben voorgeschreven, wel heeft gewerkt. Naast(!) EBP, zou ik het begrip PBE, practise based evidence, willen invoeren. Hiermee bedoel ik het verzamelen en bundelen van feedback van onze patiënten, zijnde effect, bijwerkingen en uitvoerbaarheid van de voorgeschreven behandeling. De extra administratieve belasting die dit kost, komt direct ten goede aan de patient, de ervaring van de betreffende arts en de gehele beroepsgroep. Andere voordelen van het invoeren van PBE zijn: onderzoek wordt meer praktijkgericht; er is meer aandacht voor specifieke subgroepen van patiënten; er is meer aandacht voor regionale verschillen (denk aan resistentiepatronen) en er kan meer aandacht zijn voor uitzonderingen: waarom reageert deze patient niet op de behandeling die bewezen effectief zou moeten zijn? Kunnen we gezamenlijk een groep patiënten definiëren waarbij we van te voren weten dat een bepaalde behandeling bij hen niet effectief zal zijn?
Graag zou ik, naast mijn werk in de praktijk, willen (mee)werken aan het verstevigen van het fundament van de reguliere geneeskunde, middels het ontwikkelen van methodes voor het verzamelen, interpreteren en implementeren van PBE, zodat we in de toekomst onze patiënten nog beter van dienst kunnen zijn. Wie sluit zich aan?
Annette K Offringa-Hup
Huisarts, Westervoort.